Suivez-nous sur les réseaux sociaux !
Sommaire du chapitre :
Dernières publications
Publications
Chapitre 3 – Maladie coronaire
Auteurs : D. Angoulvant, G. Franck, G. Lemesle, J.-S. Hulot, F. Ivanes, J.-B. Michel, E. Miquelestorena-Standley, A. Nitenberg, F. Vincent
Introduction
La maladie coronaire, à l’origine de l’ischémie myocardique et de l’infarctus du myocarde, est l’une des premières causes de décès dans le monde. Elle résulte très majoritairement de l’athérosclérose, processus dégénératif de la paroi artérielle à l’origine de perturbations aiguës et/ou chroniques de l’apport de sang véhiculant nutriments et oxygène au muscle cardiaque. En France, la maladie coronaire touchait 1 467 300 personnes en 2013 (âge moyen 71,2 ans, 65,7 % d’hommes). En pratique clinique, on distingue la maladie coronaire stable, ou syndrome coronaire chronique, et les syndromes coronaires aigus qui constituent les deux formes symptomatiques de la même maladie. Les connaissances concernant l’anatomie et la physiologie coronaire ainsi que ceux concernant la physiopathologie de l’athérosclérose sont des préalables indispensables à la compréhension des symptômes, signes cliniques, de la démarche diagnostique et des thérapeutiques indiquées chez les patients porteurs de maladie coronaire.
Anatomie : vascularisation du cœur
Les artères du cœur sont disposées en couronne autour du cœur, d’où leur nom d’artères coronaires (A. Paré, 1561). Les artères coronaires sont le plus souvent au nombre de deux, l’artère coronaire droite et l’artère coronaire gauche. Elles sont connectées au niveau de la portion initiale de l’aorte, à environ 1 cm au-dessus des sigmoïdes aortiques. Leur débit au repos représente à peu près 5 % du débit cardiaque (voir chapitre 1, Vascularisation du cœur).
Contrairement à la plupart des autres artères de l’organisme, elles sont essentiellement perfusées durant la diastole ventriculaire.
Artères coronaires
Distribution habituelle
Artère coronaire droite
L’artère coronaire droite est connectée au niveau du sinus de l’aorte, dénommé sinus coronaire droit par les cliniciens. Son trajet présente un premier segment court oblique en avant et à droite, un deuxième segment où elle longe le bord inférieur de l’atrium droit qui la recouvre dans le sillon coronaire, puis un troisième segment où elle rejoint la face postérieure du cœur au niveau de la croix des sillons. Elle se termine en se divisant en deux branches terminales : l’artère interventriculaire postérieure et l’artère rétroventriculaire. Ses branches collatérales sont des branches ascendantes atriales droites et des branches descendantes (marginales dites du bord droit) ventriculaires droites.
Artère coronaire gauche
L’artère coronaire gauche est connectée au niveau du sinus de l’aorte (sinus coronaire gauche). Son trajet initial, appelé tronc commun, est le plus souvent très court, de 1 à 2 cm, entre tronc pulmonaire et auricule gauche. Elle se divise en une artère interventriculaire antérieure et une artère circonflexe.
Artère interventriculaire antérieure
L’artère interventriculaire antérieure naît du tronc commun de l’artère coronaire gauche, chemine dans le sillon interventriculaire antérieur et se termine dans le sillon interventriculaire postérieur après avoir contourné l’incisure cardiaque. Elle donne des branches ventriculaires droites courtes et fines, des branches ventriculaires gauches (diagonales) et des artères septales antérieures essentiellement et postérieures variables en fonction de sa terminaison dans le sillon interventriculaire postérieur.
Artère circonflexe
L’artère circonflexe naît du tronc commun de l’artère coronaire gauche, chemine dans le sillon coronaire gauche (sillon auriculoventriculaire), contourne le bord gauche du cœur et se termine vers la croix des sillons, parfois en donnant une artère interventriculaire postérieure (on parlera alors de dominance gauche). Ses branches collatérales sont les artères ascendantes atriales gauches et les artères descendantes ventriculaires (communément appelées marginales ou latérales).
Variations
Des variations de l’importance relative des deux artères coronaires sont fréquentes. On considère que l’artère coronaire dominante est celle qui se prolonge dans le sillon interventriculaire postérieur en fournissant une artère interventriculaire postérieure. Si c’est la coronaire droite on parle alors de dominance droite, si c’est l’artère circonflexe on parle alors de dominance gauche. On distingue ainsi trois situations en termes de distribution du réseau coronaire : coronaires droites dominantes (fréquence d’environ 48 %), coronaires gauches dominantes (fréquence d’environ 18 %) et distributions équilibrées (fréquence d’environ 34 %).
Une autre variation est l’absence de tronc commun de la coronaire gauche avec pour conséquence une connexion séparée de l’artère interventriculaire antérieure et l’artère circonflexe au niveau du sinus coronaire gauche. Les deux ostia coronaires sont souvent très rapprochés avec un aspect dit « en canon de fusil ».
Les anomalies de connexion des artères coronaires correspondent généralement à une artère coronaire qui se connecte d’un sinus autre que son sinus coronaire habituel. Il peut s’agir de l’artère coronaire droite qui naît du sinus coronaire gauche ou de l’artère coronaire gauche (ou de l’une de ses branches de division) au lieu du sinus coronaire droit. L’artère de connexion anormale va rejoint son trajet normal et cela peut avoir des conséquences physiopathologiques, en particulier lorsque la coronaire se positionne entre l’artère pulmonaire et l’aorte (risque de compression à l’effort notamment et donc de développement d’une ischémie myocardique).
Territoires vasculaires
La distribution dans les différents territoires myocardiques des artères coronaires (fig. 3.1) permet de comprendre la topographie des infarctus myocardiques et certaines de ses complications (cf. infra, Sémiologie) en fonction de l’artère siège de la thrombose aiguë :
- l’artère interventriculaire antérieure vascularise la paroi antérieure du ventricule gauche et le septum interventriculaire ;
- les artères diagonales vascularisent la paroi latérale du ventricule gauche ;
- les artères marginales vascularisent la paroi latérale haute du ventricule gauche ;
- l’artère circonflexe vascularise la paroi latérale basse et de manière variable la paroi inférieure du ventricule gauche (en fonction de la dominance du réseau coronaire) ;
- l’artère coronaire droite vascularise le ventricule droit et la paroi postérieure et inférieure du ventricule gauche (en fonction de la dominance du réseau coronaire).
________________________________________________________________________________
Figure 3.1. Vue antérieure du système artériel coronaire.
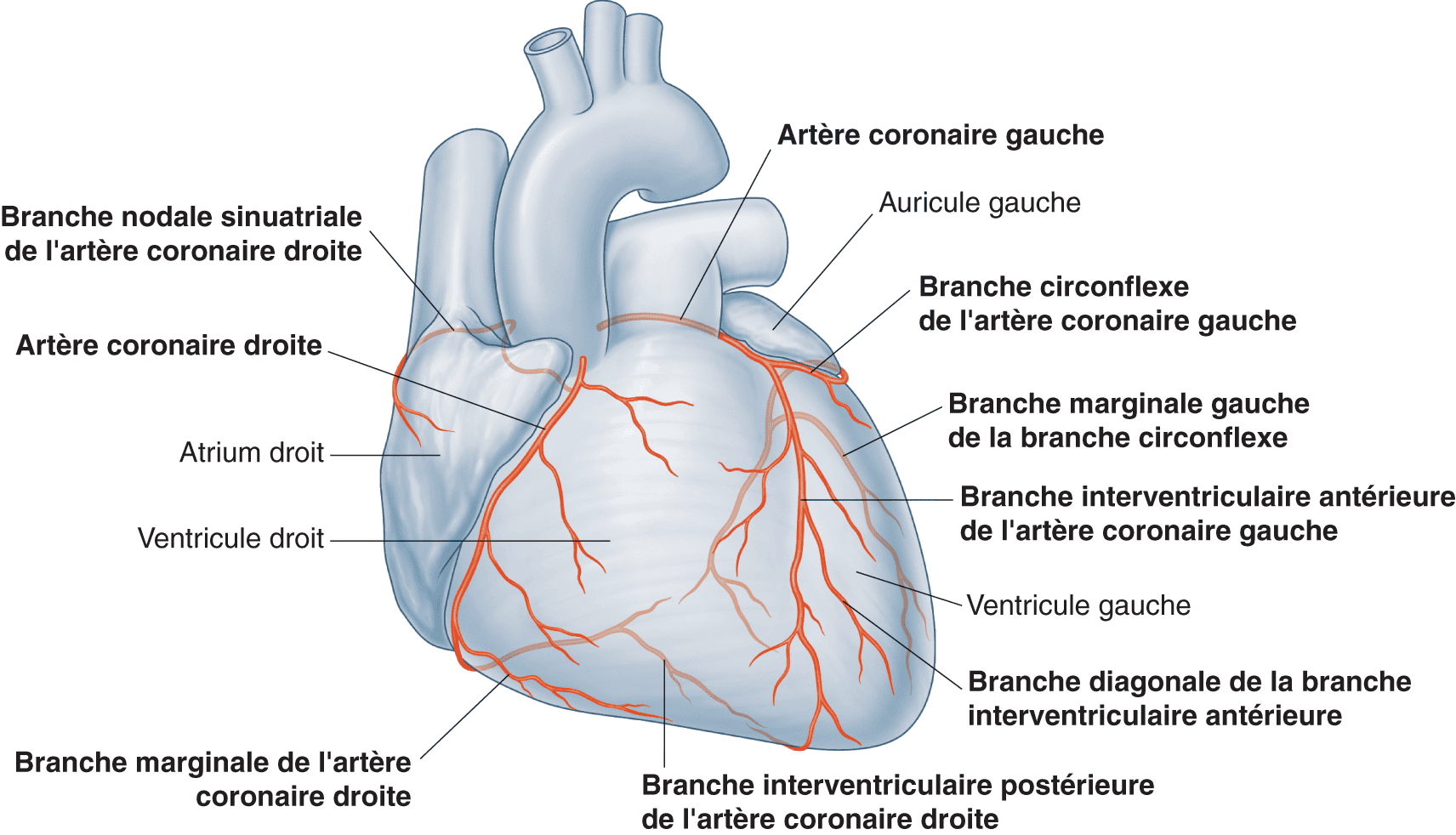
Source : Drake RL, Vogl AW, Mitchell AWM. Gray’s Anatomie pour les étudiants. 2e édition. Paris : Elsevier ; 2010.
________________________________________________________________________________
Il est important de connaître la vascularisation de certaines zones spécialisées du myocarde car les complications cliniques résultant d’une obstruction de ces artères sont potentiellement très sévères et peuvent nécessiter une intervention rapide. La vascularisation du tissu nodal dont l’atteinte peut entraîner des troubles de la conduction et celle des muscles papillaires ou piliers des ventricules dont l’atteinte peut entraîner une insuffisance valvulaire atrio-ventriculaire (mitrale ou tricuspide) que l’on observe dans certains infarctus :
- l’artère du nœud sino-atrial provient le plus souvent (67 %) de l’artère atriale droite supérieure, branche de l’artère coronaire droite. Elle provient parfois de l’artère atriale gauche supérieure (26 %), branche de l’artère circonflexe. Plus rarement (7 %), la vascularisation provient de l’artère atriale droite et de l’artère atriale gauche ;
- le nœud atrio-ventriculaire est vascularisé par l’artère du nœud atrio-ventriculaire issu le plus souvent des artères septales inférieures, dépendant de l’artère coronaire droite dans 48 % des cas, de l’artère coronaire gauche dans 18 % des cas et des deux artères dans 34 % des cas ;
- les artères vascularisant les muscles papillaires de la valve tricuspide proviennent de la deuxième artère septale antérieure qui dépend de la coronaire gauche pour le muscle papillaire antérieur (artère de la bandelette ansiforme et de la branche droite du faisceau de His) et pour les muscles papillaires septaux. Le muscle papillaire postérieur est vascularisé par une branche de l’artère interventriculaire postérieure (issue de la coronaire droite le plus souvent) ;
- les artères vascularisant les muscles papillaires de la valve mitrale proviennent des artères septales antérieures (qui dépendent de l’artère coronaire gauche) pour le muscle papillaire antérieur et de l’artère interventriculaire postérieure (branche de l’artère coronaire droite) pour le muscle papillaire postérieur.
Anastomoses artérielles
Lors des injections artérielles cadavériques, on observe des anastomoses entre les deux systèmes coronaires (droit et gauche), essentiellement dans la cloison interventriculaire, mais les constatations nécropsiques lors des infarctus du myocarde montrent que, fonctionnellement, les artères du cœur se comportent habituellement comme des artères terminales dont l’obstruction entraîne une ischémie et/ou une nécrose cardiaque en aval. Il faut noter, cependant, que chez les patients porteurs de maladie coronaire chronique, on observe parfois le développement d’anastomoses (de suppléance) entre les branches distales des artères coronaires droites et gauches (branches collatérales) qui peuvent influencer les symptômes, voire la taille d’infarctus en cas de sténose et/ou d’occlusion aiguë coronaire.
Veines du cœur
Les veines du cœur sont réparties en trois systèmes :
- le sinus coronaire, qui naît de la grande veine du cœur : il présente un trajet de 2 à 3 cm dans le sillon coronaire et se jette dans l’atrium droit. Les veines collatérales affluentes sont : la veine moyenne du cœur (ou interventriculaire postérieure), la petite veine du cœur, la veine oblique de l’atrium (Marshall) ;
- les veines antérieures du cœur (Galien) issues du ventricule droit, qui se terminent dans l’atrium droit ;
- les veines minimes du cœur (Thébésius), qui naissent dans l’épaisseur des parois du cœur et se jettent directement dans les cavités cardiaques.
Lymphatiques du cœur
Les lymphatiques se regroupent en deux réseaux principaux : un réseau lymphatique sous-endocardique développé surtout au niveau des ventricules et un réseau sous-épicardique. Des nœuds lymphatiques épicardiques ont été décrits. Les deux réseaux lymphatiques sont drainés par deux troncs collecteurs :
- le tronc collecteur gauche, qui naît sur la face postérieure du cœur puis rejoint la face postérieure du tronc pulmonaire pour se terminer dans les nœuds lymphatiques intertrachéobronchiques ;
- le tronc collecteur droit, qui naît dans le sillon interventriculaire postérieur et suit le trajet de l’artère coronaire droite pour rejoindre les nœuds lymphatiques médiastinaux antérieurs.
Embryologie et histologie des artères coronaires
Embryologie des artères coronaires
Embryologiquement, les artères coronaires ne naissent pas de l’aorte mais se connectent à celle-ci dans un second temps. Leur développement est un mécanisme complexe qui reste incomplètement élucidé. L’hypothèse actuelle implique une interaction entre des cellules endothéliales dérivées de l’épicarde et des cellules myocardiques aboutissant à leur transformation en cellules mésenchymateuses par un mécanisme de transition épithélio-mésenchymateuse. Ces cellules mésenchymateuses sont à l’origine d’ébauches vasculaires apparaissant entre l’épicarde et le myocarde après la quatrième semaine de vie, et fusionnant pour former un réseau vasculaire. Aux environs de la sixième semaine, deux ébauches vasculaires issues de ce réseau pénètrent dans l’aorte, créant ainsi les ostia coronaires, droit et gauche. La maturation de ces vaisseaux est par la suite favorisée par l’exposition à la pression sanguine systémique.
Les anomalies du développement des coronaires sont variées : anomalies de l’origine, anomalies du trajet épicardique, et fistules coronaires. Les anomalies de l’origine correspondent à la connexion d’une artère coronaire vers le sinus controlatéral, à la connexion d’une artère coronaire vers une autre artère coronaire ou, plus rarement, à la connexion d’une artère coronaire vers l’artère pulmonaire (responsable d’un infarctus du myocarde à la naissance). Certaines anomalies du trajet peuvent être associées à une anomalie de l’origine (exemple du trajet inter-aorto-pulmonaire en cas d’implantation du tronc coronaire gauche dans le sinus droit). Enfin, des fistules coronaires, liées à une connexion anormale entre une artère coronaire et une cavité cardiaque ou un gros vaisseau, peuvent être observées.
Histologie des artères coronaires
Les artères coronaires sont des artères musculaires qui se connectent au niveau de l’aorte ascendante. Elles sont constituées de trois couches de dedans en dehors : l’intima, la média et l’adventice.
Intima
L’intima est une couche dont l’épaisseur varie avec l’âge : initialement fine, elle sera modifiée et épaissie par de la fibrose avec le vieillissement. Elle est constituée d’un endothélium souligné par une lame basale et par un tissu conjonctif sous-endothélial.
L’endothélium est composé d’une couche de cellules endothéliales aplaties, hautement spécialisées, tapissant la surface du vaisseau et comportant de nombreuses connexions les unes avec les autres.
Ces cellules ont différentes fonctions telles que la sécrétion de facteurs modulant le calibre vasculaire, et de facteurs modulant la coagulation. Elles assurent également des fonctions de transport grâce à un mécanisme de pinocytose ou, encore, ont la capacité d’exprimer des molécules d’adhésion induites par les cytokines.
La lame basale est composée de collagène, de protéoglycanes et de protéines telles que la laminine et la fibronectine.
Le tissu conjonctif sous-endothélial est composé d’une matrice extracellulaire dans laquelle sont disposés des fibres collagènes, des fibres élastiques, quelques fibroblastes et des cellules myointimales. Cette composition est liée au rôle nutritif mais également mécanique de ce tissu conjonctif, permettant le glissement de l’endothélium sur les couches sous-jacentes.
Média
La média correspond à la couche moyenne de la paroi artérielle. Dans les artères coronaires elle est principalement constituée de plusieurs couches concentriques de cellules musculaires lisses permettant d’adapter le calibre artériel aux besoins métaboliques du myocarde. Quelques fibres de collagène et des fibres élastiques sont dispersées entre les cellules musculaires. Ces fibres élastiques se concentrent et s’organisent en deux limitantes élastiques cernant la média : la limitante élastique interne, proéminente, d’aspect crénelé en microscopie optique en raison d’artefacts de contraction, située entre l’intima et la média et empêchant l’occlusion de l’artère ; et la limitante élastique externe, située entre la média et l’adventice, souvent moins bien définie et moins visible dans les artères coronaires que dans les artères de grand calibre.
Avec l’âge, une fibrose médiale peut apparaître, de même que des altérations de la limitante élastique interne.
Adventice
L’adventice est une couche mal limitée, difficile à distinguer du tissu adipeux épicardique dans lequel les artères sont situées. Elle est constituée d’un tissu conjonctif fait de fibres de collagène et de fibres élastiques, et renferme des adipocytes, des vasa vasorum et des fibres nerveuses végétatives innervant le muscle lisse de la média.
Physiologie de la circulation coronaire
Le myocarde est un muscle strié dont la particularité, qu’il partage avec le diaphragme, est de n’être jamais au repos. La circulation coronaire est la circulation nourricière du myocarde. La finalité de celle-ci est d’apporter au myocarde les nutriments et l’oxygène (O2) destinés à son métabolisme qui est aérobie. Ce métabolisme produit les très importantes quantités d’ATP nécessaires à l’activité mécanique. La consommation d’O2 du myocarde est dépendante de trois paramètres : la fréquence cardiaque, la pression systolique et la contractilité du myocarde.
L’extraction d’O2 du sang artériel par le myocarde est quasi maximale chez un sujet au repos. Le sang veineux coronaire est le plus désaturé en O2 de tout l’organisme, environ 5 ml d’O2 pour 100 ml de sang ce qui fait que la différence artérioveineuse (DAV) en O2 est très élevée, environ 14 ml d’O2 pour 100 ml de sang. Il n’y a donc quasiment pas de réserve d’extraction d’O2 du sang artériel, et par conséquent, toute augmentation de la demande en O2 par le myocarde, lors d’un effort physique par exemple, ne pourra être pourvue que par une augmentation du débit coronaire.
Ce débit est délivré par les artères coronaires, droite et gauche, situées à la surface du cœur (cf. anatomie). Ces artères donnent des branches perforantes qui pénètrent la paroi myocardique et se divisent en petites artères et artérioles qui circulent parallèlement à la surface du cœur avant de se terminer par des capillaires qui circulent entre les myocytes.
Le débit coronaire est rythmé par la contraction du myocarde. Au niveau de la paroi du ventricule gauche le débit est à 80 % diastolique. Pour la paroi du ventricule droit, il se répartit à égalité entre la diastole et la systole (fig. 3.2A). Au repos, le débit coronaire est d’environ 0,8 à 1 ml/min par gramme de myocarde pour le ventricule gauche et de 0,6 à 0,7 ml/min par gramme de myocarde pour le ventricule droit. Quelles que soient les conditions, repos ou exercice, le débit coronaire chez un sujet normal représente environ 5 % du débit cardiaque soit, chez un adulte de taille moyenne dont le débit cardiaque est au repos de 5 l/min, 250 ml/min, ce qui correspond à une consommation en O2 de 35 ml par minute.
________________________________________________________________________________
Figure 3.2. Débit sanguin coronaire au cours du cycle cardiaque.
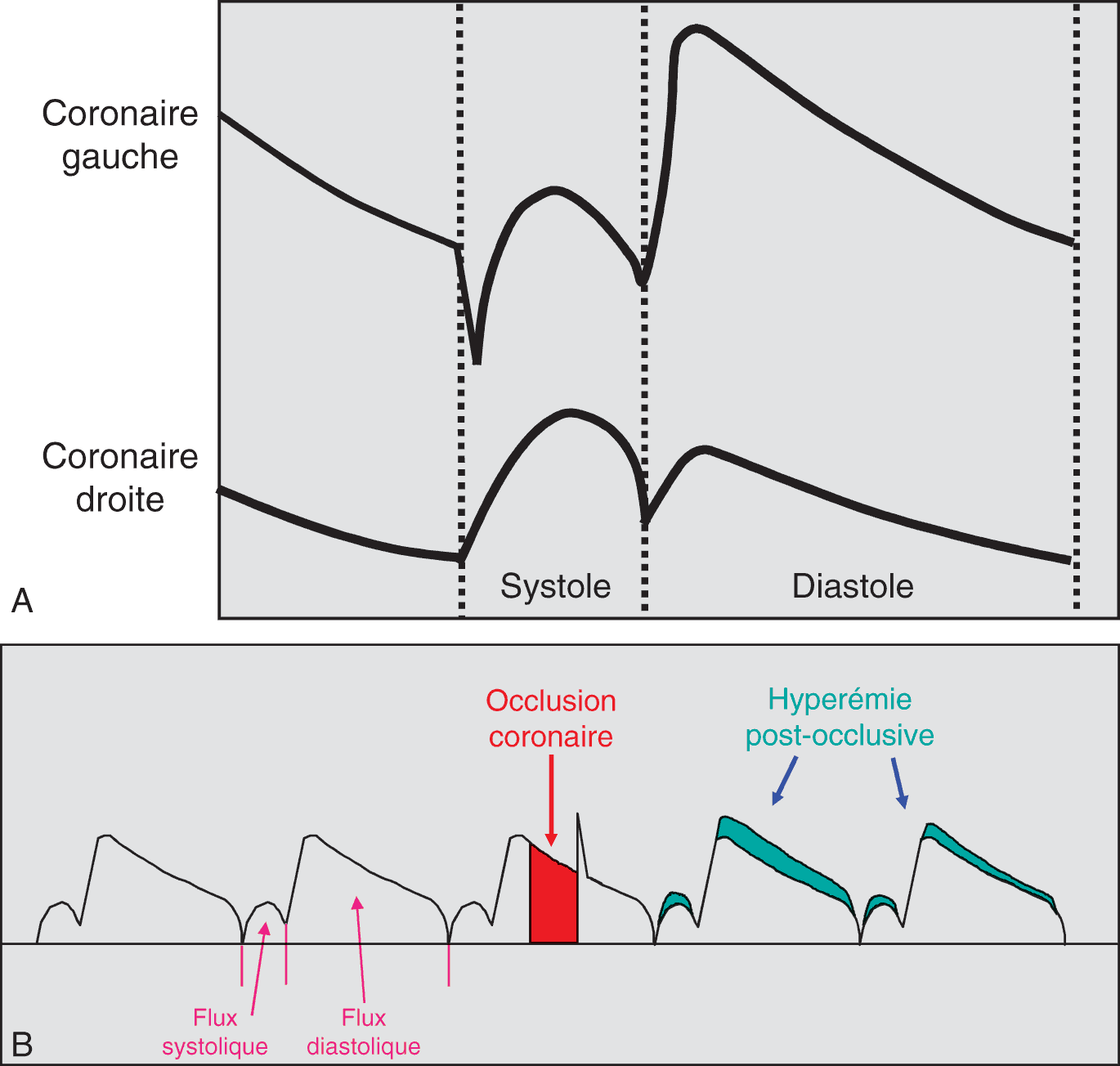
En abscisse, le temps. En ordonnée, le débit coronaire.
(A) On voit que le débit de la coronaire gauche est maximal en début de diastole. Ce débit est adapté aux besoins métaboliques du myocarde, et cette adaptation est très rapide, se faisant pratiquement de battement à battement. (B) Lorsque l’on interrompt le flux coronaire gauche pendant une diastole (occlusion coronaire, zone rouge), le déficit de débit est compensé par une augmentation des flux coronaire systolique et diastolique lors des battements suivants (hyperémie post occlusive, zone verte).
________________________________________________________________________________
Adaptation du débit coronaire à la demande métabolique du myocarde : la vasomotricité coronaire
Au sens physique du terme, le débit coronaire n’est pas régulé car il n’y a pas de capteur de débit au niveau des artères. Ce débit est adapté aux besoins métaboliques du myocarde et cette adaptation est très rapide, se faisant pratiquement de battement à battement. Lorsque l’on interrompt le flux coronaire diastolique pendant une diastole, le déficit de débit est compensé par une augmentation des flux coronaires systoliques et diastoliques lors des battements suivants (fig. 3.2B).
L’adaptation du débit coronaire à la demande en O2 du myocarde se fait principalement au niveau de la microcirculation coronaire (petites artères et artérioles coronaires). Elle est sous la dépendance de trois acteurs qui affectent la vasomotricité coronaire et qui peuvent se suppléer les uns aux autres (fig. 3.3) :
- le métabolisme du myocarde ;
- l’endothélium coronaire ;
- le système nerveux autonome.
________________________________________________________________________________
Figure 3.3. Régulation de la vasomotricité coronaire.
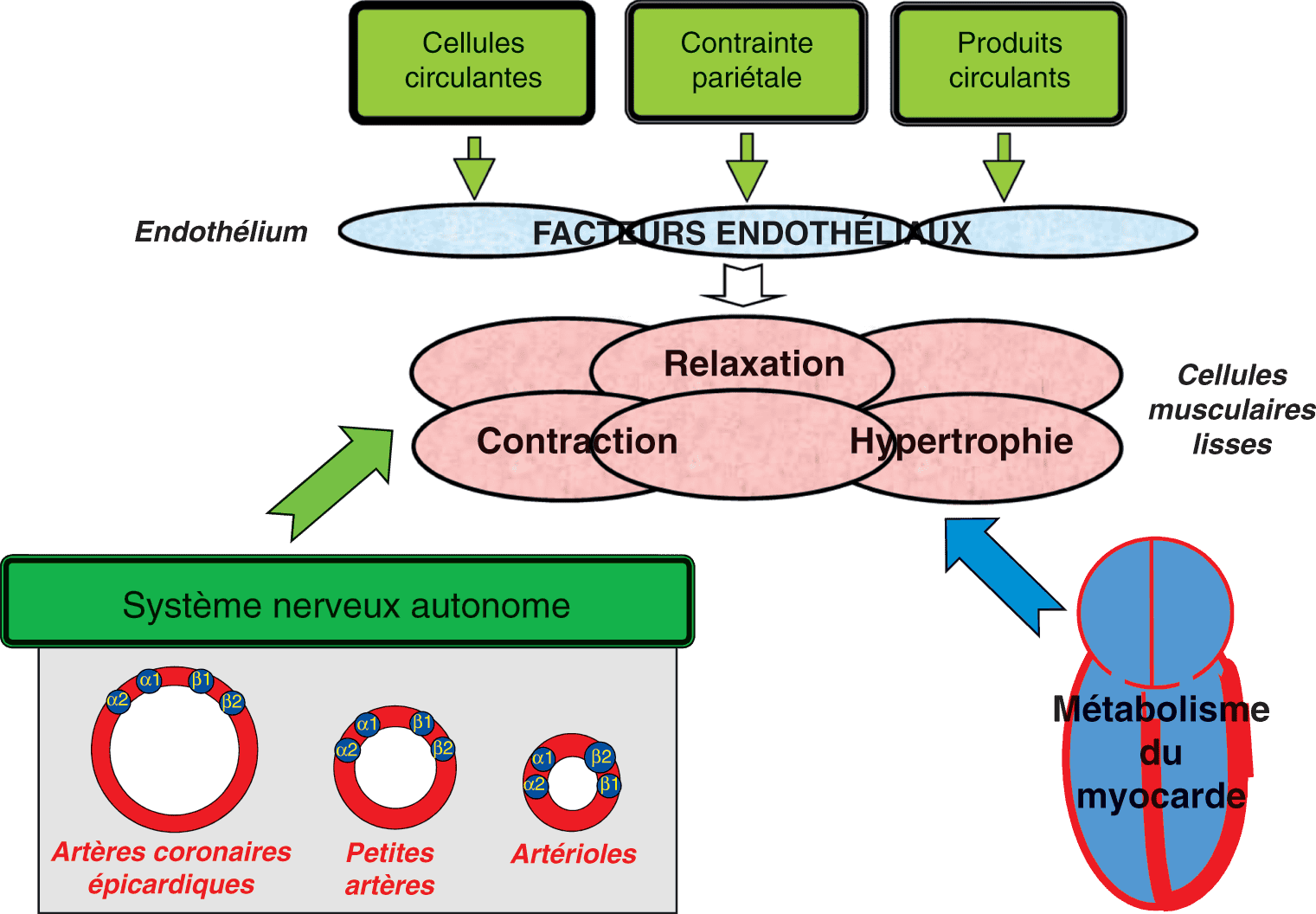
La vasomotricité coronaire (contraction, relaxation) est sous la dépendance de tois acteurs qui peuvent se suppléer les uns les autres : le métabolisme du myocarde, l’endothélium coronaire, et le système nerveux autonome. Elle permet l’adaptation du débit coronaire à la demande en oxygène du myocarde. Métabolisme du myocarde.
________________________________________________________________________________
L’adénosine a longtemps été considérée comme le médiateur physiologique entre l’activité du myocarde (demande en O2) et la vasomotricité coronaire (débit coronaire). L’adénosine est la plus puissante des substances vasodilatatrices coronaires, terme ultime de la dégradation de l’adénosine triphosphate (ATP). Elle agit directement sur les cellules musculaires lisses des artérioles coronaires (vasodilatation endothélium indépendante) et sur l’endothélium vasculaire en stimulant la NO-synthase et la production de monoxyde d’azote (NO) qui induit une relaxation des cellules musculaires lisses (vasodilatation endothélium dépendante).
L’augmentation de l’activité mécanique du myocarde est responsable d’une augmentation du métabolisme du myocarde et de la consommation d’ATP à l’origine d’une augmentation de la production d’adénosine. L’adénosine ainsi produite va agir au niveau des cellules musculaires lisses des artérioles coronaires induisant une vasodilatation qui permet en retour une augmentation du débit coronaire et de l’apport en O2. Cette augmentation du débit coronaire est ainsi parfaitement adaptée à la quantité d’adénosine produite ; « la boucle est ainsi bouclée ».
Cependant, l’adénosine ne semble pas être le bon candidat pour expliquer à elle seule l’adaptation du débit coronaire à la demande métabolique du myocarde. Des travaux expérimentaux suggèrent que la concentration en adénosine dans le sang veineux coronaire et dans l’espace interstitiel au contact des artérioles coronaires n’atteint jamais le seuil nécessaire à une vasodilatation coronaire. On a également montré expérimentalement que l’inactivation de l’adénosine n’empêche pas l’augmentation du débit coronaire lorsque la demande métabolique du myocarde augmente. Enfin, lorsque les myocytes sont correctement approvisionnés en O2, l’adénosine est réutilisée pour la synthèse d’ATP et ne diffuse pas dans le secteur extracellulaire. Elle ne peut donc induire une vasodilatation.
Un autre produit du métabolisme du myocarde, formé à partir des radicaux libres de l’oxygène (O2-), le péroxyde d’hydrogène H2O2, peut induire une vasodilatation coronaire.
Quoi qu’il en soit, aucun de ces mécanismes ne peut expliquer une adaptation rapide du débit coronaire à la demande métabolique, mais ils peuvent être impliqués dans des conditions pathologiques.
Endothélium vasculaire
L’endothélium coronaire produit une substance relaxante des cellules musculaires lisses de la paroi vasculaire et une vasodilatation des vaisseaux. Cette substance est le monoxyde d’azote (NO). La synthèse de NO est due à la stimulation d’une NO-synthase constitutive qui répond à une entrée de calcium dans la cellule endothéliale. Le NO diffuse vers les cellules musculaires lisses sous-jacentes dont il provoque la relaxation par deux mécanismes :
- une hyperpolarisation de la membrane liée à l’augmentation de la perméabilité au potassium ;
- une activation de la guanylate cyclase qui, via la production de GMP cyclique (GMPc), entraîne à la fois une sortie de calcium de la cellule et un recaptage du calcium par le réticulum sarcoplasmique, ce qui diminue la concentration en calcium libre intracellulaire et la formation des ponts entre l’actine et la myosine.
L’endothélium synthétise et libère de nombreuses autres substances vasomotrices :
- soit vasodilatatrices : prostacycline (PGI2), endothelial derived hyperpolarizing factor (EDHF) ;
- soit vasoconstrictrices : endothéline-1 (ET-1), thromboxane A2 (TXA2), angiotensine II, etc.
La vasomotricité coronaire endothélium-dépendante peut être modulée par de nombreux intervenants : le système nerveux autonome, les myocytes par l’intermédiaire de l’adénosine, le sang qui véhicule de nombreuses substances, les plaquettes qui libèrent plusieurs produits vasomoteurs lors de leur activation (sérotonine, ATP et ADP, thromboxane A2 [TXA2]), la contrainte mécanique tangentielle (vitesse d’écoulement) et radiaire (pression intravasculaire).
Là encore, même si l’endothélium coronaire est impliqué dans la vasomotricité coronaire, rien ne permet de voir en son action un facteur déterminant de l’adaptation rapide du débit coronaire.
Système nerveux autonome
Le système nerveux autonome intervient dans le contrôle de la vasomotricité coronaire par différentes voies :
- le système orthosympathique agit par voie neurogène et par voie sanguine. Les terminaisons nerveuses orthosympathiques au contact des vaisseaux coronaires libèrent de la noradrénaline. Les catécholamines circulantes libérées par la médullosurrénale (noradrénaline et surtout adrénaline) sont véhiculées jusqu’aux vaisseaux coronaires par voie sanguine ;
- le système parasympathique agit sur la circulation coronaire de deux manières en sachant que cette voie est physiologiquement peu importante. Les terminaisons nerveuses au contact des terminaisons nerveuses orthosympathiques libèrent de l’acétylcholine qui a un effet dépresseur sur la libération de la noradrénaline (récepteurs muscariniques M). Les terminaisons nerveuses au contact des vaisseaux coronaires libèrent l’acétylcholine qui stimule la NO synthase endothéliale (récepteurs muscariniques) ;
- enfin, il existe au niveau de la circulation coronaire, mêlées aux voies orthosympathiques, des fibres nerveuses non-adrénergiques et non-cholinergiques qui libèrent des médiateurs chimiques capables de moduler la vasomotricité coronaire (neuropeptide Y, vaso-intestinal peptide [VIP]).
La réponse vasculaire à la stimulation sympathique dépend de la densité de chacun des types de récepteurs et du rapport des différents types récepteurs au niveau des cellules musculaires lisses, en sachant que les récepteurs α-adrénergiques induisent une contraction (vasoconstriction) et que les récepteurs β-adrénergiques induisent une relaxation (vasodilatation). La distribution des récepteurs adrénergiques varie des artères coronaires épicardiques aux artérioles coronaires.
Chez le sujet normal, la densité des différents types de récepteurs est peu élevée dans les artères épicardiques et le rapport entre les différents types de récepteurs est équilibré. L’injection intracoronaire d’un stimulant des récepteurs α-adrénergiques est sans effet sur le calibre des artères coronaires épicardiques. Dans les petites artères coronaires, il y a une prédominance de récepteurs β1- et β2-adrénergiques et dans les artérioles coronaires, il y a une forte densité et une très large dominance de récepteurs β2-adrénergiques. L’injection intracoronaire d’un stimulant des récepteurs α-adrénergiques est sans effet sur le débit coronaire (pas d’effet sur la microcirculation coronaire). La perfusion de noradrénaline induit une dilatation dose-dépendante des artérioles coronaires qui est bloquée par le propranolol, un antagoniste non sélectif des β-récepteurs (bêtabloquant). En revanche, le practolol, un antagoniste sélectif des récepteurs β1-adrénergiques est sans effet significatif sur la dilatation artériolaire. Cette dernière étant bloquée par la butoxamine, un antagoniste sélectif des récepteurs β2-adrénergiques qui sont donc les médiateurs de cette vasodilatation.
Au total, le système orthosympathique est le meilleur candidat pour expliquer l’adaptation rapide du débit coronaire à la demande métabolique du myocarde. En effet, toute élévation du métabolisme périphérique, que ce soit l’exercice, la digestion, l’émotion, etc. stimule le système orthosympathique. Si les autres mécanismes sont potentiellement efficaces, ils sont beaucoup trop lents pour expliquer la réponse quasi immédiate de la circulation coronaire aux stimuli périphériques. Ils peuvent toutefois suppléer le système nerveux autonome, c’est le cas dans la transplantation cardiaque où le greffon n’est pas innervé.
Distribution de l’oxygène et des nutriments au myocarde
La vasomotricité coronaire est la condition nécessaire pour délivrer au myocarde le débit sanguin dont il a besoin pour son métabolisme. Mais c’est la circulation capillaire coronaire qui est le lieu de la distribution des nutriments et de l’O2 aux myocytes. La qualité des apports de l’O2 aux myocytes dépend du volume des capillaires (qui détermine la surface d’échange avec les tissus et le volume de sang qui participe aux échanges) et de la distance entre les capillaires (distance de diffusion de l’O2 vers les mitochondries). Chez l’adulte, la distance intercapillaire est d’environ de 20 μm et chez le sujet au repos, environ un capillaire sur quatre est ouvert. Lorsque le débit coronaire augmente, le nombre de capillaires ouverts augmente.
Débit coronaire de base et notion de réserve de débit coronaire
Chez un sujet normal, le débit coronaire basal est une fonction croissante de la pression coronaire. En effet, l’augmentation de la pression coronaire est liée à l’augmentation de la pression dans le ventricule gauche nécessaire à l’augmentation de la pression dans l’aorte. Cette augmentation de la pression dans le ventricule gauche entraîne obligatoirement une augmentation de la consommation d’O2 par le myocarde et donc du débit coronaire.
La vasodilatation maximale de la circulation coronaire par diverses substances permet d’évaluer la capacité maximale d’augmentation du débit coronaire pour une pression de perfusion coronaire donnée, c’est ce qu’on appelle la réserve de débit coronaire. Chez le sujet normal, pour des pressions de perfusion coronaire moyennes comprises entre 50 et 130 mmHg, la réserve de débit coronaire est comprise entre 3,5 et 4,5 (fig. 3.4).
________________________________________________________________________________
Figure 3.4. Reserve de débit coronaire.
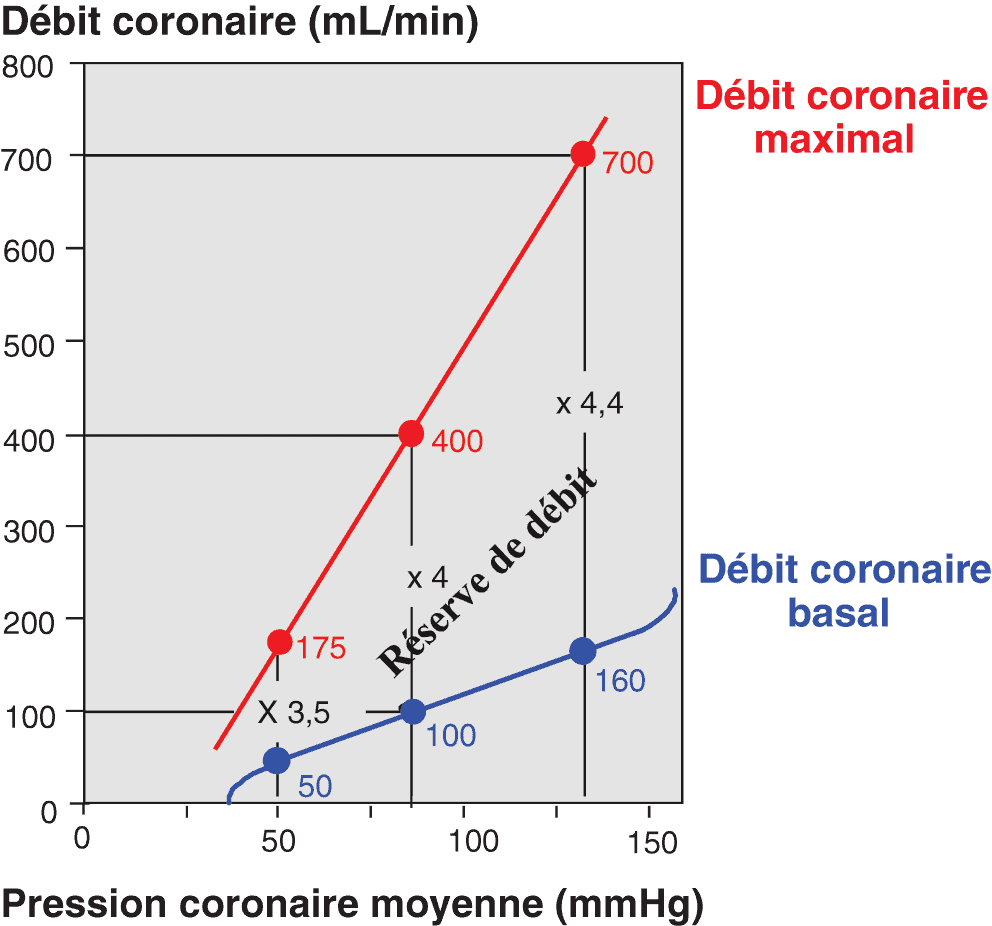
La réserve de débit coronaire correspond à la capacité maximale d’augmentation du débit coronaire pour une pression de perfusion donnée. Celle-ci est obtenue lorsque l’on induit une vasodilatation maximale de la circulation coronaire par diverses substances. Chez le sujet normal, pour des pressions de perfusion coronaire moyennes comprises entre 50 et 130 mmHg, la réserve de débit coronaire est comprise entre 3,5 et 4,5.
________________________________________________________________________________
En résumé
L’apport de l’O2 et des nutriments au myocarde dépend de très nombreux paramètres (fig. 3.5) :
- le contenu en O2 du sang artériel détermine la quantité d’O2 qui va participer aux échanges tissulaires. Il dépend de la pression partielle en O2 dans le sang artériel (échanges respiratoires) et du contenu en hémoglobine ;
- le débit coronaire qui dépend de la pression aortique (pression motrice) et de la contre-pression exercée par la contraction du myocarde ;
- la fréquence cardiaque qui détermine la durée de la diastole et le débit cardiaque ;
- le calibre des artères coronaires épicardiques (vaisseaux de conductance) et la vasomotricité de celles-ci ;
- le nombre, le calibre, et la vasomotricité des petites artères et des artérioles coronaires (vaisseaux de résistance) ;
- la distance intercapillaire déterminée par la taille des myocytes et le nombre de capillaires ouverts, le volume des capillaires (diamètre et longueur) qui détermine la quantité de sang participant aux échanges, la vitesse d’écoulement du sang qui détermine le temps de transit capillaire.
________________________________________________________________________________
Figure 3.5. Régulation de l’apport en oxygène et nutriments au myocarde.
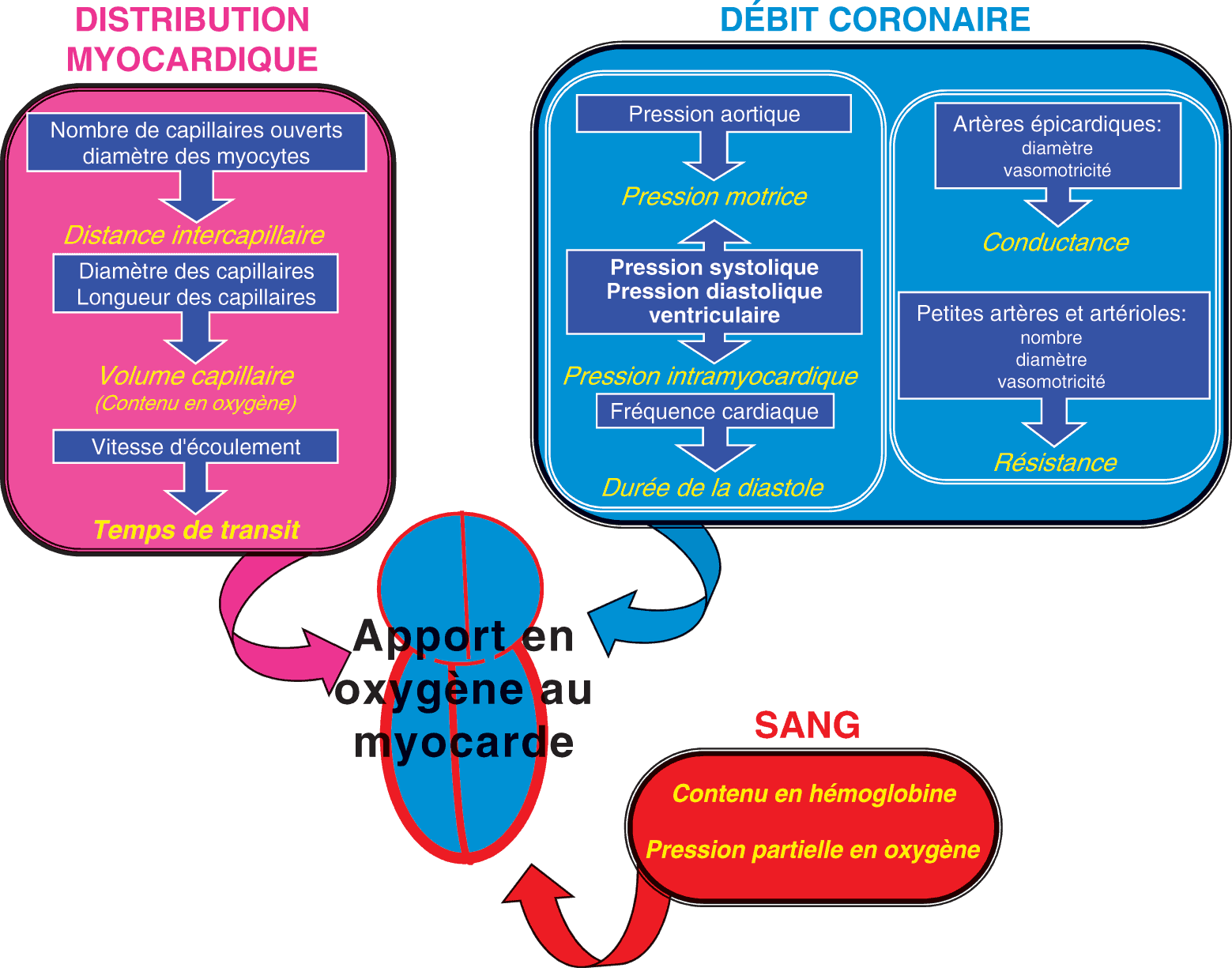
L’apport de l’oxygène et des nutriments au myocarde dépend de très nombreux paramètres. (1) Le contenu en oxygène du sang artériel qui dépend de la pression partielle en oxygène dans le sang artériel et du contenu en hémoglobine. (2) Le débit coronaire qui dépend de la pression aortique (pression motrice) et de la contre pression exercée par la contraction du myocarde. (3) La fréquence cardiaque qui détermine la durée de la diastole. (4) Le calibre des artères coronaires épicardiques et leur vasomotricité. (5) Le nombre, le calibre, et la vasomotricité des petites artères et des artérioles coronaires. (6) La distance intercapillaire déterminée par la taille des myocytes et le nombre de capillaires ouverts, le volume des capillaires (diamètre et longueur) détermine la quantité de sang participant aux échanges et la vitesse d’écoulement du sang détermine le temps de transit capillaire.
________________________________________________________________________________
Physiopathologie de l’ischémie myocardique
L’ischémie myocardique survient lorsqu’il existe une inadéquation entre les besoins et les apports en O2 du myocarde. Cette situation est classiquement rencontrée en cas de maladie coronaire (sténose serrée ou occlusion). Elle peut également être rencontrée dans d’autres circonstances : tachycardie prolongée, dysfonction microvasculaire, hypoxie liée à une insuffisance respiratoire aiguë, troubles du transport de l’O2 (intoxication au monoxyde de carbone, hémoglobinopathie). Dans le cadre de ce chapitre, nous ne décrirons que l’ischémie myocardique résultant de la maladie coronaire.
Effet d’une sténose coronaire
Quand une artère coronaire est rétrécie par une plaque d’athérome, l’autorégulation coronaire tend initialement à normaliser le débit de perfusion en aval de la sténose en réduisant les résistances des vaisseaux plus distaux (vasodilatation). Cependant, lorsque la sténose devient sévère (> 70 % du diamètre de l’artère coronaire), elle s’associe à une diminution du débit de perfusion en aval de la sténose. L’expérience de Gould (fig. 3.6) montre les conséquences du % de rétrécissement artériel sur le flux coronaire au repos (courbe du bas) et à l’effort (courbe du haut). Au repos, le flux coronaire n’est significativement diminué qu’à partir de 90 % de sténose coronaire alors qu’à l’effort la diminution du flux coronaire susceptible d’entraîner une ischémie apparaît des 70 % de sténose (cf. Angor d’effort).
________________________________________________________________________________
Figure 3.6. Conséquences d’une sténose coronaire sur la réserve de flux coronaire.
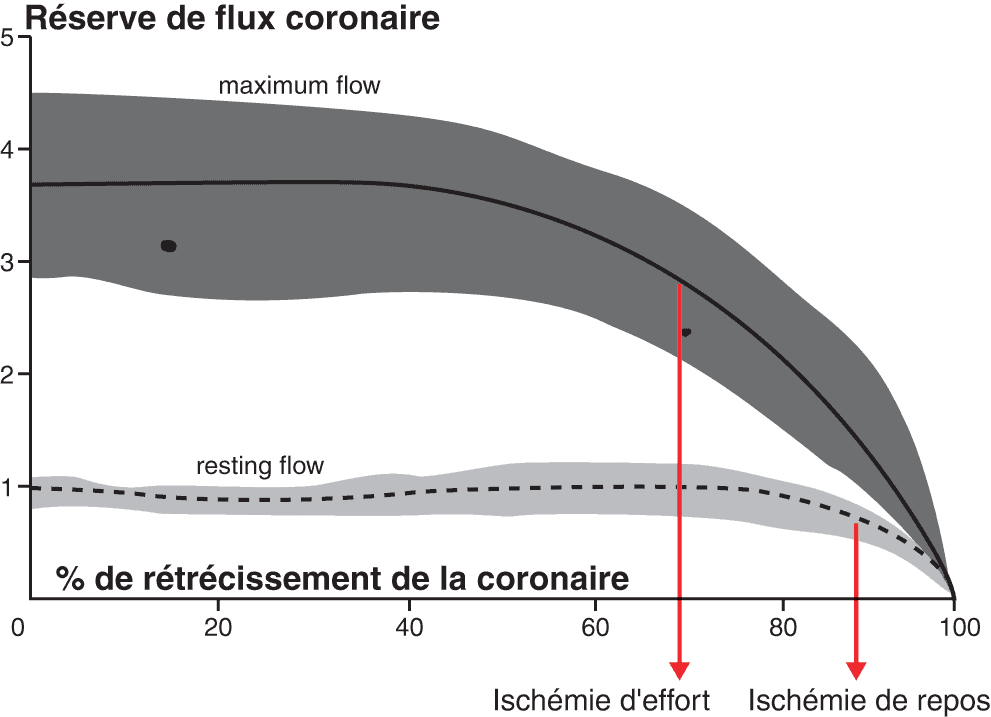
Au repos « resting flow », le flux coronaire diminue avec le degré de rétrécissement de la coronaire, entraînant une ischémie à partir d’une sténose diminuant de 90 % la lumière artérielle. À l’effort « maximum flow », le flux coronaire diminue, entraînant une ischémie à partir d’une sténose diminuant de 70 % la lumière artérielle.
Source : d’après Gould KL et al. Physiologic basis of assessing critical coronary stenosis. Instantaneous flow response and regional distribution during coronary hyperemia as measures of coronary flow reserve. Am J Cardiol 1974 ; 33:87-94.
________________________________________________________________________________
Occlusion coronaire aiguë
L’occlusion coronaire aiguë complique le plus souvent une lésion athéroscléreuse sous-jacente avec formation d’un thrombus au niveau d’une plaque rompue.
Le spasme coronaire peut également mimer une occlusion coronaire ou s’y associer.
Lorsque se produit l’occlusion aiguë, le débit sanguin s’arrête dans les vaisseaux en aval de l’occlusion. La zone du muscle cardiaque vascularisée par cette artère se retrouve en situation d’ischémie aiguë et ne va plus se contracter normalement.
Si l’occlusion persiste (entre 15 et 60 minutes), les cellules myocardiques nécrosent (meurent) dans cette région dénommée « zone d’infarctus » (cf. nécrose du myocarde).
Facteurs favorisant ou limitant l’ischémie myocardique
L’importance des conséquences de l’ischémie myocardique et la taille de la zone infarcie vont dépendre de l’importance du territoire vascularisé par l’artère coronaire occluse (zone à risque), de la durée de l’occlusion (qui peut être raccourcie par une intervention thérapeutique) et de l’existence de circulation collatérale pouvant permettre de maintenir une partie des apports en oxygène à la zone infarcie.
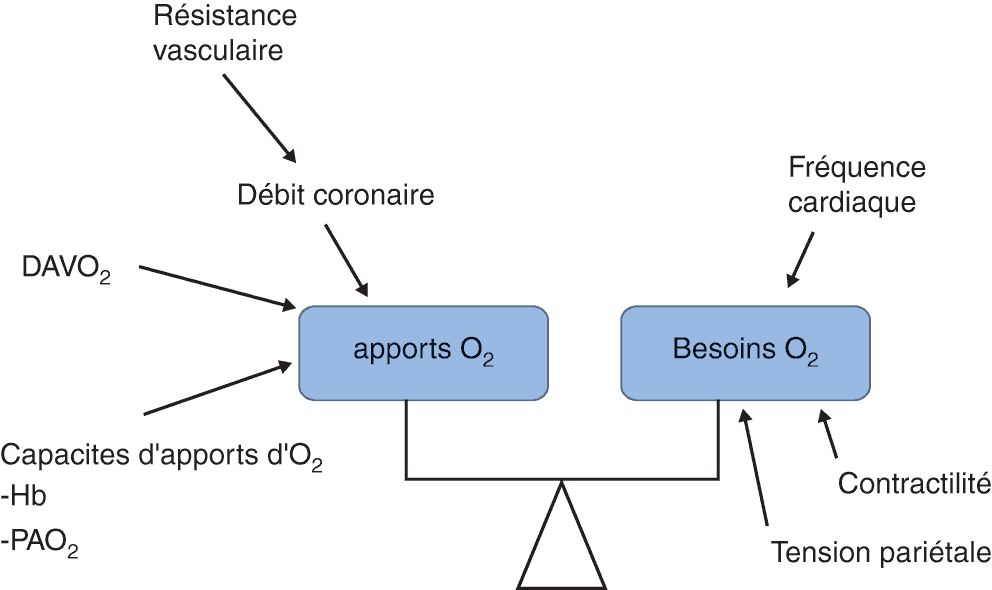
L’ischémie myocardique sera favorisée par toutes les situations qui augmentent les besoins en oxygène du myocarde (fig. 3.7) ; inversement, les traitements limitant ces facteurs seront potentiellement anti-ischémiques.
________________________________________________________________________________
Figure 3.7. Adaptation des apports aux besoins en oxygène du myocarde.
________________________________________________________________________________
Cascade ischémique : les conséquences de l’ischémie myocardique aiguë
La survenue d’une ischémie myocardique dans un territoire du myocarde entraîne une succession de phénomènes pathologiques appelés « cascade ischémique ». La cascade ischémique verra intervenir successivement :
- la sténose coronaire peut entraîner une diminution de la perfusion du myocarde (qui peut être mise en évidence par scintigraphie myocardique) ;
- altération du métabolisme myocardique avec diminution de la synthèse d’ATP et du fonctionnement des échangeurs membranaires (qui peut être mise en évidence par tomographie avec émission de positons) ;
- altération de la fonction mécanique (relaxation et contraction) du myocarde ischémique (qui peut être mise en évidence à l’échographie) ;
- troubles de l’électrogénèse visible sur l’électrocardiogramme ;
- douleur angineuse.
La cascade n’est pas toujours complète et la douleur angineuse n’est finalement présente que dans moins d’un tiers des épisodes ischémiques. On parle alors d’ischémie myocardique silencieuse. L’arrêt de l’effort déclencheur d’ischémie entraînera une normalisation des anomalies constituant la cascade ischémique.
Ischémie chronique
En cas d’ischémie chronique liée à des sténoses coronaires très serrées et multiples, des anomalies régionales puis globales de contraction du muscle cardiaque peuvent apparaître (myocarde « hibernant » encore viable et dont la fonction se normalise après le rétablissement de la perfusion coronaire). L’ischémie myocardique représente, surtout chez le sujet âgé, la cause la plus fréquente d’insuffisance cardiaque. C’est pour cette raison que la maladie coronaire est systématiquement recherchée en présence d’insuffisance cardiaque car son traitement peut permettre de restaurer une fonction myocardique normale.
Nécrose du myocarde
En cas d’ischémie prolongée on observe une nécrose du myocarde (infarctus). Il s’agit d’une destruction irréversible du muscle cardiaque puisqu’il n’existe pas de processus de régénération efficace. Le myocarde nécrosé sera remplacé par de la fibrose qui est non contractile. La taille d’infarctus est le principal facteur pronostic de ces patients. Plus la taille d’infarctus est importante, plus le patient risque de décéder rapidement. De plus, les autres territoires myocardiques non détruits pendant l’infarctus devront s’adapter pour maintenir une activité contractile. Dans certains cas, cette adaptation s’accompagne à moyen termes de déformations et de perte de fonction des autres territoires (c’est le phénomène de remodelage délétère) qui favorise l’apparition d’une insuffisance cardiaque.
Athérothrombose : de la formation des plaques à leurs complications
L’athérosclérose et l’athérothrombose coronaires sont les principales causes de l’infarctus du myocarde, première cause de mortalité dans les pays industrialisés (deuxième cause en France derrière le cancer) et première cause d’insuffisance cardiaque secondaire.
L’athérome chez l’homme est un processus pathologique chronique se développant sur de nombreuses années et débutant dès la plus jeune enfance. Il n’est pas spécifique des artères coronaires mais touche tout le système artériel. Il est particulièrement fréquent au niveau des artères coronaires du fait de l’hémodynamique spécifique des vaisseaux coronaires décrite plus haut (fig. 3.8), et particulièrement grave du fait de ses conséquences sur la vitalité et la contractilité du tissu myocardique d’aval, en particulier au niveau du ventricule gauche dont la fonction est indispensable à la vie de l’organisme humain dans sa totalité. L’athérome est une pathologie du système artériel à haute pression. Il n’est observé ni dans les veines, ni dans les artères pulmonaires également à basse pression.
________________________________________________________________________________
Figure 3.8. Hémodynamique systolo-diastolique de la circulation coronaire.
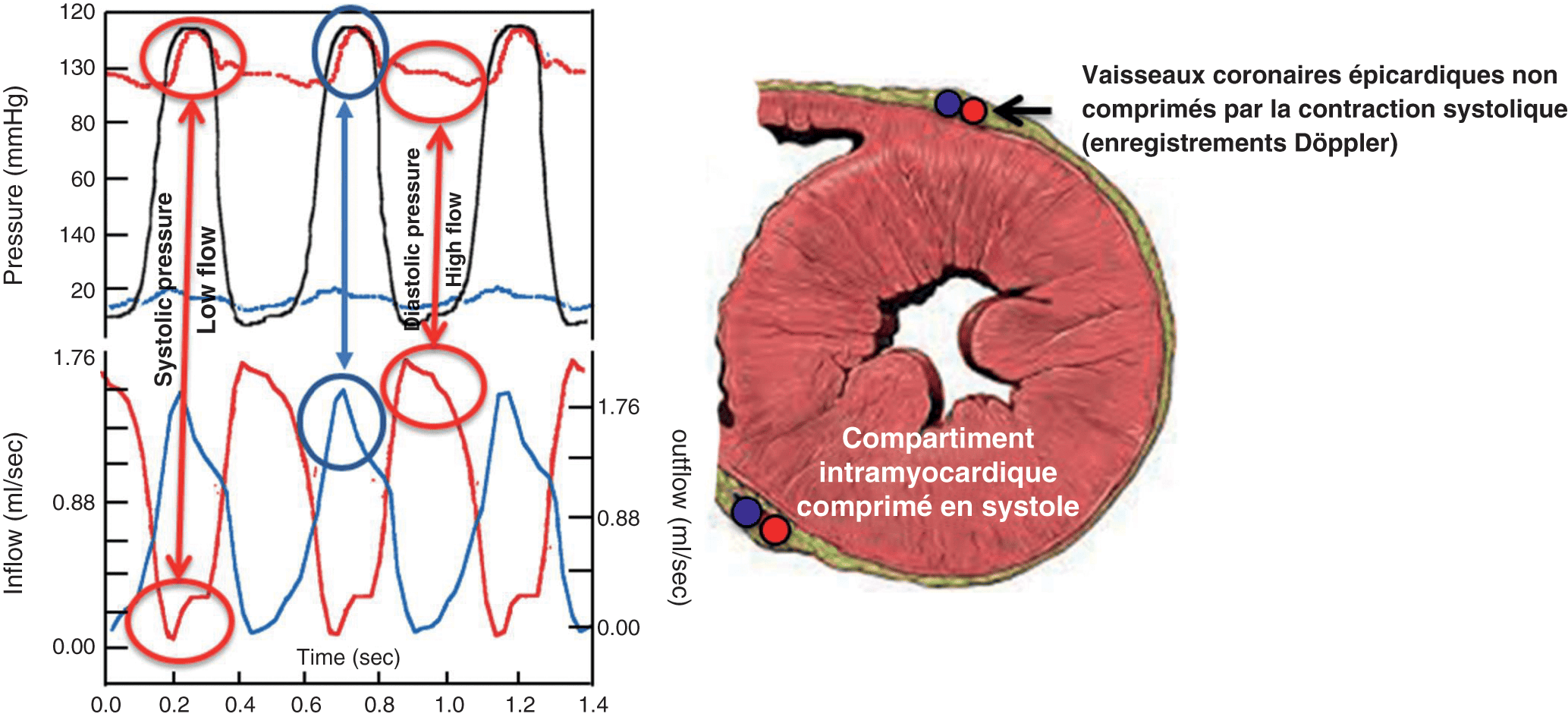
Enregistrement simultané des courbes de pression aortique et intraventriculaire gauche et des courbes de vitesse (effet Doppler) dans l’artère (rouge) et la veine (bleu) coronaire gauche épicardique. Le flux artériel entrant est nul en systole et maximal en diastole. Le flux veineux sortant est inversé, nul en diastole et maximal en systole. La vitesse de flux veineux sortant est proportionnelle à la vitesse de contraction VG (contractilité). La circulation intramyocardique se comporte comme une éponge essorée en systole, remplie en diastole. Cette hémodynamique spécifique explique la sensibilité particulière des artères coronaires à l’athérome.
Source : Chadwick RS, Tedgui A, Michel JB, Ohayon J, Levy BI. Am J Physiol. 1990 Jun ; 258(6 Pt 2):H1687-98.
________________________________________________________________________________
Le développement de l’athérome chez l’homme est initialement en rapport avec l’hémodynamique : le gradient de pression entre le sang artériel circulant (120/80 mmHg) et la pression interstitielle de l’adventice artérielle (10 mmHg), génère une conductance hydraulique (soluble) radiale transpariétale, faible au regard de la conductance longitudinale (circulation). Cette conductance radiale transpariétale entraîne avec elle les composés plasmatiques solubles dont les lipoprotéines, macromolécules circulantes transportant lipides, cholestérol et phospholipides, éléments constitutifs vitaux, structurants des membranes cellulaires, sur un squelette protéique appelé apolipoprotéines. Les lipoprotéines de faible densité (low density lipoprotein [LDL]) interfèrent via leur composant protéique (apo-B) durant ce transport radial transpariétal avec les glycosaminoglycans (GAG) sécrétés par les cellules musculaires lisses (CML). Cette interaction apo-B/GAG aboutit à l’accumulation de lipides, en particulier de cholestérol sous-endothélial, formant la lésion initiale de l’athérome ou strie lipidique (fig. 3.9).
________________________________________________________________________________
Figure 3.9. Strie lipidique d’une coronaire humaine disséquée (adventicectomie).
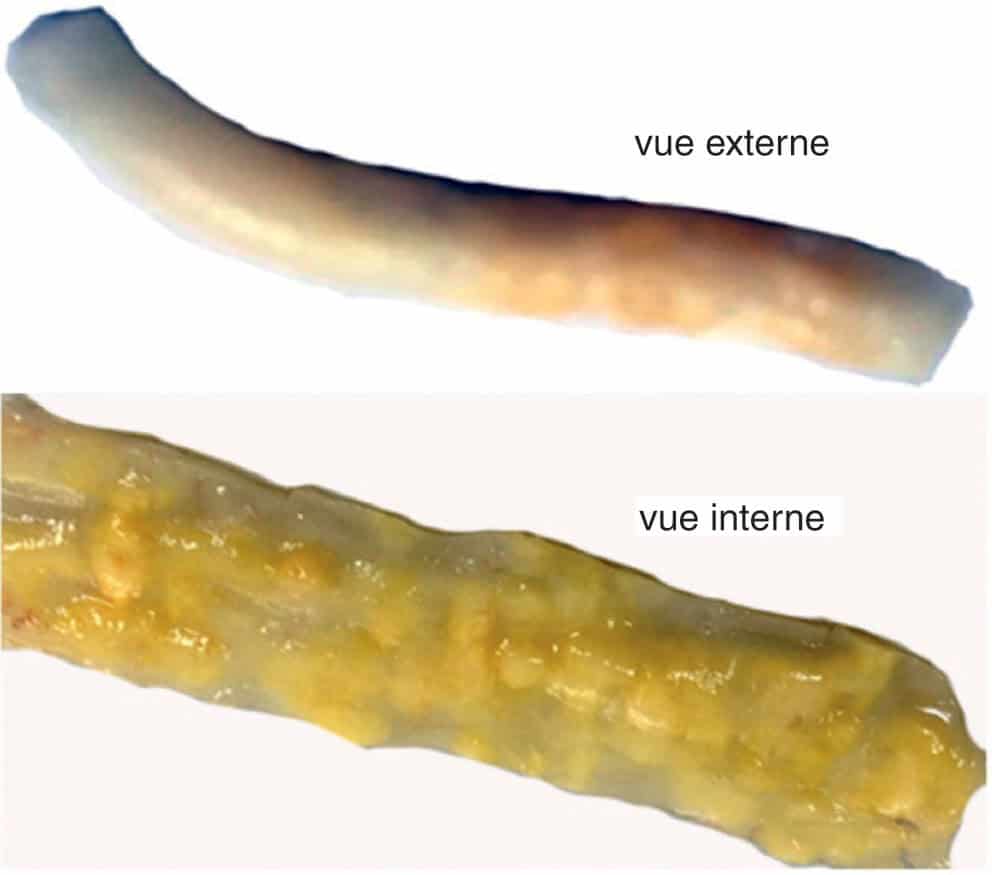
Source : Jean-Baptiste Michel.
________________________________________________________________________________
La strie lipidique constitue la lésion initiale de l’athérome. La photo présente une vue externe et une vue interne de l’endartère. La coloration jaune correspond aux dépôts lipidiques oxydés.
Chez l’homme, ces stries lipidiques initiales se développent préférentiellement au niveau des bifurcations artérielles pour des raisons hémodynamiques (flux, shear stress, etc.). Ces dépôts lipidiques sous-endothéliaux vont rapidement s’oxyder. Les CML sous endothéliales et quelques macrophages captent ces lipides par un mécanisme d’endocytose, aboutissant à la formation de cellules spumeuses surchargées de vacuoles lipidiques oxydantes. Chez l’homme, la majorité des cellules spumeuses sont des CML (fig. 3.10, partie droite).
________________________________________________________________________________
Figure 3.10. Deux processus physiopathologiques distincts aboutissent à deux types de plaques d’athérosclérose.
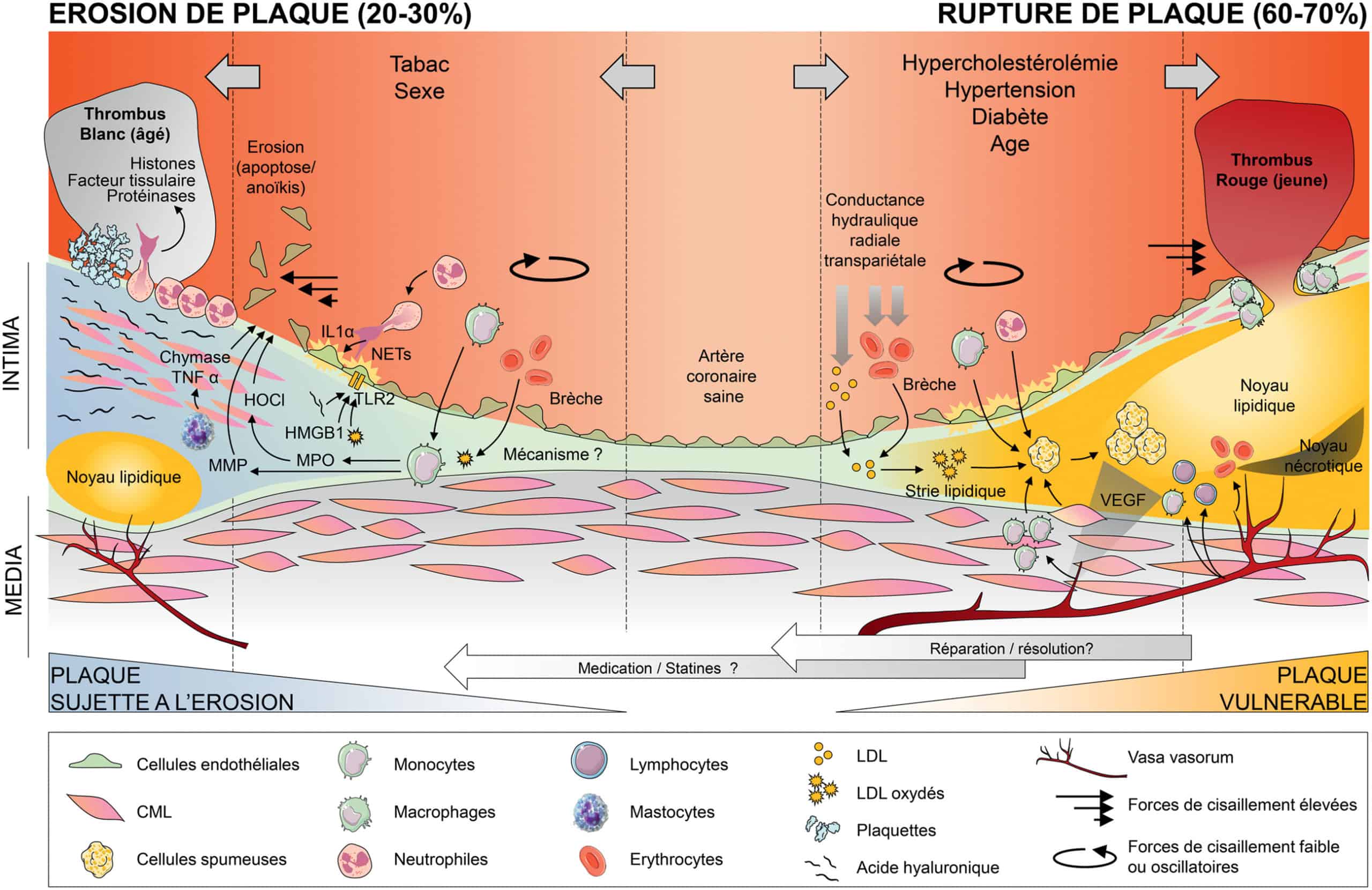
À droite de la figure est schématisée la formation de la plaque vulnérable, dont la complication (rupture) est responsable de 60 à 70 % des événements coronaires aigus. Cette plaque se forme à partir de l’accumulation de macromolécules bioactives comme les lipoprotéines dans l’espace sous-endothélial grâce à la conductance hydraulique radiale transpariétale. L’hémodynamique a également pour conséquence la formation de brèches endothéliales dans lesquelles peuvent s’engouffrer de nombreux éléments sanguins et notamment des globules rouges, cargo important de cholestérol membranaire. L’accumulation précoce du cholestérol dans la paroi constitue la strie lipidique, dans laquelle le cholestérol va s’oxyder et être capté par les CML et les monocytes/macrophages. Ces derniers se transformeront en cellules spumeuses, composantes essentielles à la formation du noyau lipidique dans le fibro-athérome. L’activation des cellules endothéliales en réponse à l’hémodynamique ou à l’agression locale causée par les brèches ou l’oxydation des lipoprotéines se traduit par une augmentation de l’expression de molécules d’adhérence, qui facilitent l’adhérence, l’arrêt et la transmigration de cellules inflammatoires, un processus rendu possible uniquement dans les régions dans lesquelles les forces de cisaillement sont les plus faibles. Le recrutement de cellules inflammatoires constitue une facette importante du développement de l’athérosclérose, et amplifie le processus de formation de la plaque athéromateuse. L’angiogenèse centripète qui se met en place en réponse au gradient de VEGF secrété par les CML va permettre un recrutement massif de cellules de l’immunité innée ou adaptative, ainsi que de l’hémorragie intraplaque, accélérant le processus pathologique. La plaque vulnérable, fragilisée par une chappe fibreuse excessivement fine, incapable de contenir les contraintes mécaniques causées par les forces de cisaillement très fortes liées à son bombement, peut rompre et causer la formation immédiate d’un thrombus rouge riche en fibrine.
À gauche de la figure sont schématisées la formation et la complication de la plaque sujette à l’érosion, responsable de 20 à 30 % des événements coronaires aigus. Comparées aux plaques vulnérables, elles contiennent des cellules musculaires lisses plus abondantes ainsi qu’une matrice extracellulaire riche en protéoglycanes et en acide hyaluronique. Par ailleurs, les plaques sujettes à l’érosion sont faiblement inflammatoires, moins chargées en lipides et dépourvues de zone nécrotique dans plus de la moitié des cas. Lorsqu’une zone nécrotique est présente, elle ne communique jamais avec la lumière artérielle dont elle est séparée par une chape fibreuse plus épaisse que dans la plaque vulnérable. Si les mécanismes qui conduisent à la formation de cette plaque sont inconnus, certains facteurs de risque comme le tabac et le sexe féminin pourraient promouvoir son développement, dans un contexte de cholestérolémie modérée.
Certains éléments initiateurs communs à la plaque vulnérable pourraient également être impliqués, comme la formation de brèches, l’entrée d’éléments sanguins et la rétention de LDL. Les mastocytes résidents favorisent l’apoptose des cellules endothéliales via la chymase et le TNFα, ainsi que la desquamation des cellules endothéliales luminales en activant les métalloprotéases matricielles (MMP) matricielles grâce à leurs protéases. Les macrophages résidants synthétisent quant à eux la myélopéroxydase, qui favorise la production d’acide hypochloreux (HOCl), un inducteur d’apoptose endothéliale. La perturbation du flux sanguin qui caractérise les segments artériels sujets à l’érosion entraîne également l’activation des cellules endothéliales luminales, et l’augmentation de récepteurs de danger comme le TLR2 (récepteur de type Toll). Certains éléments matriciels retrouvés dans la plaque sujette à l’érosion, comme l’acide hyaluronique de faible poids moléculaire, les éléments inhérents à sa formation comme les LDL oxydés ou l’HMGB1 ont la capacité de se lier au TLR2 des cellules endothéliales, favorisant un état d’activation perpétuel de ces cellules et promouvant le recrutement chronique de cellules de l’inflammation innée et particulièrement les neutrophiles. Localement, la mort rapide et abondante des neutrophiles provoque la formation de filets extracellulaires (ou NETs) cytotoxiques, qui participent à l’amplification du processus inflammatoire en maturant des cytokines pro-inflammatoires comme l’interleukine (IL)-1α, ou en provoquent directement la mort des cellules endothéliales via le complément. Localement, l’augmentation des forces de cisaillement liée au bombement progressif de la plaque favorise l’érosion d’un endothélium déjà en souffrance, exposant le collagène sous-endothélial, ce qui conduit à l’agrégation et l’activation plaquettaire, le recrutement de davantage de neutrophiles et la formation très progressive d’un thrombus blanc organisé et riche en plaquettes, n’entraînant pas nécessairement de signes cliniques à court terme mais dont la persistance et l’évolution entraînent un syndrome coronaire aigu.
________________________________________________________________________________
La deuxième étape du processus pathologique correspond à la réponse de la paroi artérielle à cette agression lipidique. Celle-ci se fait sous forme d’une migration et d’une prolifération de CML venant recouvrir la lésion lipidique initiale formant une chape fibromusculaire recouvrant la strie lipidique, ou cœur lipidique, la séparant de la circulation et de l’endothélium, bombant classiquement dans la lumière artérielle. C’est ce bombement qui peut être responsable du phénomène de sténose artérielle (par réduction du diamètre de la lumière artérielle). Contrairement aux stries lipidiques plus précoces, le cœur lipidique devient acellulaire par mort progressive des CML, libérant du cholestérol extracellulaire et formant des cristaux. Cette étape est appelée fibro-athérome ou plaque initiale.
Alors que la média artérielle est normalement avasculaire, ces étapes initiales initient un processus d’angiogenèse centripète, de l’adventice externe vers la plaque intimale. Les artérioles adventitielles vont pousser en dedans en réponse à un gradient de VEGF (vascular endothelial growth factor) secrété par les CML stimulées par des médiateurs lipidiques intimaux. Une fois la plaque atteinte, cette néo-angiogenèse, va être responsable de saignements dans la plaque, ou hémorragies intraplaques. Ce phénomène va faire basculer la plaque des stades initiaux, essentiellement lipidiques et asymptomatiques, vers une biologie plus complexe, plus riche en protéases et autres médiateurs pro-inflammatoire, responsables du phénomène de ruptures de plaques qui peut conduire à la formation d’un thrombus plus ou moins obstructif dans la lumière artérielle. C’est le phénomène d’athérothrombose. Ces hémorragies intraplaques répétées peuvent également se résorber en partie aggravant le degré de sténose sans nécessairement conduire à une rupture de plaque. De même, les ruptures de plaques peuvent cicatriser par migration et prolifération des CML sur le thrombus, aggravant également le degré de sténose. Enfin, le thrombus initial peut être rapidement et complètement obstructif entraînant une occlusion complète de l’artère à l’origine d’une ischémie aiguë puis d’une nécrose du territoire d’aval (myocarde, cerveaux, rein, etc.). Il s’agit là de la complication la plus grave.
Contrairement aux accidents carotidiens, les accidents coronaires ne sont pas tous en rapport avec des ruptures de plaques. Du fait de l’hémodynamique spécifique de ce territoire, le flux entrant en diastole est élevé, créant des forces de friction (cisaillement) importantes sur la face luminale des artères, en particulier au niveau des bifurcations, créant un phénomène d’érosion. Dans ce cas, l’endothélium est abrasé par le flux entrant, découvrant le collagène sous endothélial, générant localement un agrégat plaquettaire, pouvant rapidement évoluer vers une thrombose complète (fig 3.10, partie gauche).
Sémiologie clinique
La maladie coronaire symptomatique est un continuum allant de l’angor stable au syndrome coronaire aigu (SCA). Le maître symptôme est la douleur thoracique angineuse.
Face à une symptomatologie thoracique, il est indispensable de savoir reconnaître rapidement non seulement les signes en faveur d’une douleur angineuse mais aussi ceux des autres urgences cardiovasculaires ou non cardiovasculaires pour orienter rapidement la prise en charge du patient.
Examen clinique
Interrogatoire
Avec l’interprétation de l’électrocardiogramme, l’interrogatoire est l’étape la plus importante dans le diagnostic étiologique d’une douleur thoracique.
Il permet de recueillir les facteurs de risque cardiovasculaires (voir chapitre 2) et de préciser les caractéristiques de la douleur thoracique. Il permet également de recueillir les éventuels symptômes en faveur d’une autre localisation de l’athérosclérose (artériopathie oblitérante des membres inférieurs par exemple).
Douleur angineuse
L’angor ou angine de poitrine ou douleur thoracique angineuse est la traduction clinique de l’ischémie myocardique, quelle que soit son étiologie. Elle a été décrite pour la première fois en 1768 par Héberden en comparaison avec la brûlure de l’angine au niveau de la gorge.
La douleur thoracique résulte d’un excès de nociception par une stimulation excessive des récepteurs périphériques mis en jeu par des processus lésionnels (ischémie, inflammation, etc.) ou par des stimulations mécaniques (fracture, distension viscérale, etc.). Les fibres afférentes conduisant les douleurs du thorax sont classées en deux catégories : les fibres somatiques et les fibres viscérales. Leur stimulation produit des douleurs distinctes. La paroi, composée du derme, des muscles et de la plèvre pariétale, est innervée par des fibres somatiques convergeant vers la corne postérieure du dermatome correspondant et qui se projettent dans le cortex sur une aire miroir. La douleur est précisément localisée par le cortex au lieu de la stimulation. Les fibres viscérales proviennent des organes internes : cœur, vaisseaux, œsophage, poumon et plèvre viscérale. Les fibres d’un même organe convergent vers la corne postérieure de la moelle, lieu d’intégration et de contrôle des messages nociceptifs, sur plusieurs étages en se croisant. Elles n’ont pas de distribution métamérique. À chaque métamère, elles rejoignent les fibres somatiques qui elles ne proviennent que d’un seul niveau. Ce phénomène est plus connu sous le nom de « convergence viscérosomatique ». Les fibres empruntent ensuite les voies ascendantes communes extralemniscales vers les structures supraspinales thalamiques puis corticales. Il n’existe donc pas de somatotopie topographique viscérale dans le cortex. Seuls les territoires cutanés, musculaires et articulaires du métamère sont représentés. Ainsi, la projection métamérique médullaire du cœur, située entre C8 et D5, explique qu’une douleur coronaire puisse être ressentie au cou, à la mâchoire, ou vers le ou les membres supérieurs. La douleur pariétale (cutanée, articulation, muscles) est le plus souvent superficielle, précise, bien localisée à l’endroit de la pathologie. La douleur viscérale est beaucoup plus complexe et parfois trompeuse. Elle est en général diffuse, profonde, mal localisée, pouvant irradier dans des territoires souvent éloignés. Son intensité n’est pas toujours proportionnelle à la gravité du processus pathologique sous-jacent.
La douleur thoracique angineuse typique possède les deux caractéristiques suivantes :
- type : sensation de constriction, de serrement, de pesanteur, de lourdeur en barre ou plus rarement de brûlure ;
- localisation : son siège est le plus souvent médiothoracique rétrosternal et irradie vers l’épaule gauche (ou vers les deux épaules), le cou et le maxillaire inférieur et la face interne du bras gauche (ou vers les deux bras).
La douleur thoracique angineuse peut également être atypique si elle ne comporte pas les éléments précédemment cités :
- caractéristiques : simple inconfort thoracique, blockpnée (sensation de dyspnée avec blocage respiratoire non douloureux) ; signes digestifs (éructation, nausées, douleur épigastrique) ;
- localisation : latéro-thoracique droite, irradiation vers l’épaule droite ou vers la face interne du bras droit, ou dans le dos.
Les femmes, les patients âgés et les patients diabétiques sont plus susceptibles de présenter une symptomatologie angineuse atypique.
Angor stable
Le terme angor stable (syndrome coronaire chronique dans la nouvelle nomenclature proposée dans les recommandations de la Société Européenne de Cardiologie) regroupe les causes suivantes : sténose coronaire épicardique athéromateuse (le plus classique), angor par dysfonction microvasculaire, et angor vasospastique.
L’angor stable est une douleur thoracique angineuse qui a les trois caractéristiques supplémentaires suivantes :
- déclenchée par des facteurs favorisant l’ischémie myocardique : l’effort principalement, l’émotion, le stress, le froid, la période postprandiale (effort de digestion) ;
- soulagée par le repos et/ou les dérivés nitrés ;
- de durée brève (quelques minutes et classiquement < 10–15 minutes).
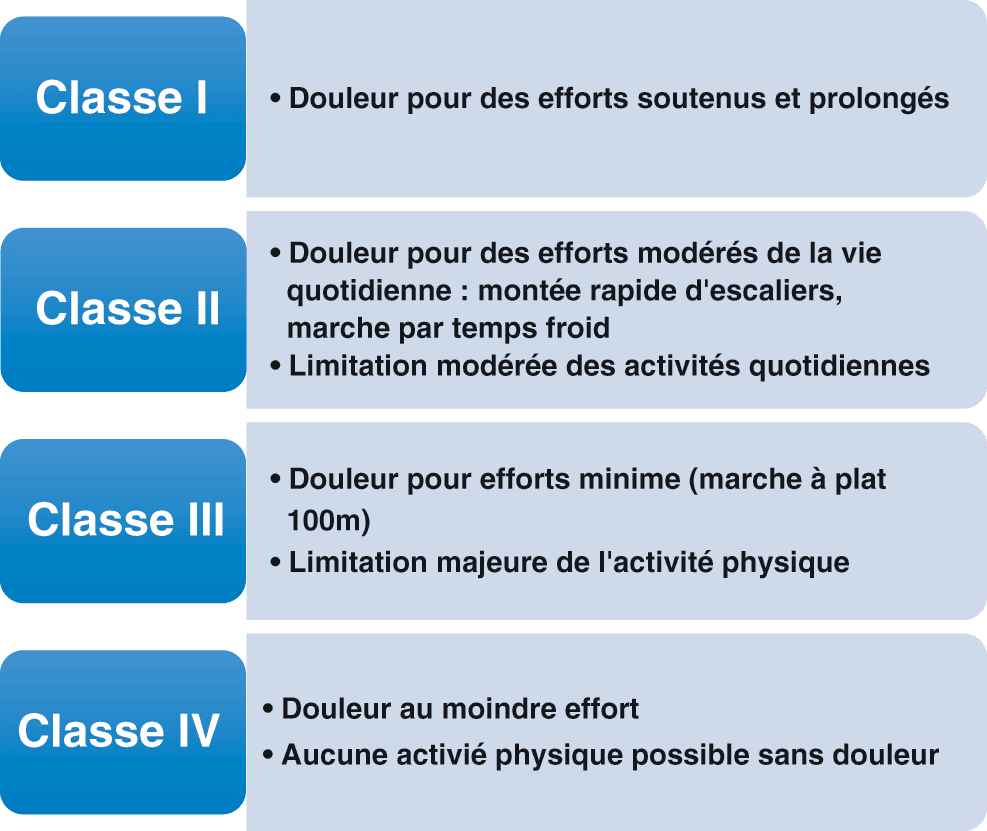
Le seuil ischémique (déséquilibre entre les besoins et les apports en O2 au myocarde) est défini par le niveau d’effort pour lequel l’angor survient (périmètre de marche par exemple). Dans l’angor stable, ce seuil ischémique ne se modifie pas d’un jour sur l’autre et la douleur apparaît donc toujours pour le même niveau d’effort. Ce seuil ischémique est stable dans le temps (quelques jours ou quelques semaines) mais il peut s’aggraver par progression de la sténose coronaire conséquence de l’athérosclérose sur plusieurs mois. Le seuil ischémique permet de définir la sévérité de l’angor. La classification de la Société canadienne de cardiologie (CCS) permet d’évaluer la sévérité de l’angor stable (fig. 3.11). Initialement et classiquement, l’angor stable débute par une douleur thoracique angineuse pour des efforts importants (≥ CCS1).
________________________________________________________________________________
Figure 3.11. Classification de la société cardiovasculaire canadienne de la sévérité de l’angor stable.
________________________________________________________________________________
Syndrome coronaire aigu (SCA), de l’angor instable à l’infarctus
Le plus souvent (mais pas toujours), il est la traduction clinique d’une ischémie myocardique aiguë déclenchée par la diminution brutale des apports myocardiques en O2 suite à la formation aiguë d’un thrombus intra-coronaire totalement occlusif ou non (cf. physiopathologie de l’ischémie myocardique).
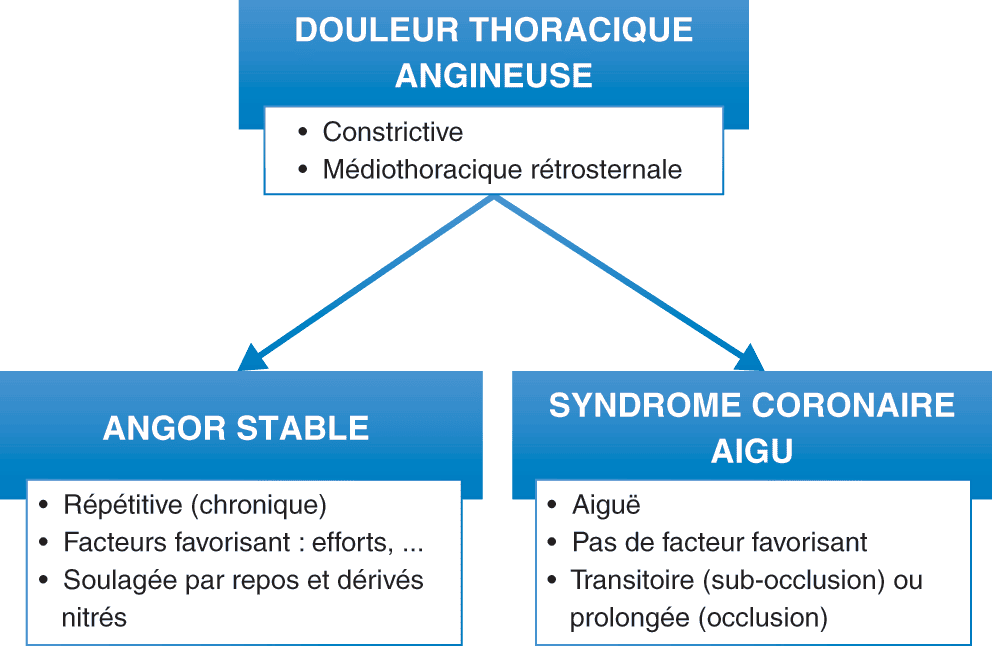
Il s’agit d’une douleur thoracique angineuse qui a les caractéristiques supplémentaires suivantes (fig. 3.12) :
- survenue aiguë ;
- pas de facteur favorisant car survient la plupart du temps au repos. Cependant, l’effort, l’émotion, le stress peuvent favoriser la rupture de plaque athéromateuse coronaire et générer un SCA ;
- non soulagée (ou seulement partiellement) par les dérivés nitrés ;
- durée :
- transitoire (quelques minutes) en cas de sub-occlusion coronaire ou d’occlusion transitoire,
- prolongée en cas d’occlusion coronaire permanente ;
- signes associés (inconstants) :
- sueurs,
- nausées, vomissements, douleur épigastrique (fréquent dans l’infarctus de topographie inférieure).
________________________________________________________________________________
Figure 3.12. Douleur thoracique, angor stable versus syndrome coronaire aigu.
________________________________________________________________________________
On classe également dans les SCA les douleurs angineuses qui ont les caractéristiques suivantes :
- angor crescendo : douleur angineuse d’intensité et de sévérité croissante (qui surviennent pour des efforts de plus en plus faibles (≥ CCS3) sur une courte période de temps (< 4 semaines). Elles traduisent la diminution rapide du seuil ischémique ;
- angor de novo : douleur thoracique angineuse d’apparition récente chez un patient préalablement asymptomatique, se répétant et d’emblée invalidante. L’absence de recul ne permet pas, dans cette situation, de savoir si le patient présente un angor stable (absence d’évolution sur plusieurs semaines ou mois) ou un angor instable (crescendo, progression rapidement progressive des symptômes). Il est donc par défaut classé instable ;
- angor de repos ou spontané : douleur thoracique angineuse mais survenant au repos et de durée prolongée, plusieurs minutes.
Le SCA n’est pas un diagnostic (à la différence de l’angor instable ou de l’infarctus du myocarde) mais un tableau syndromique qui permet d’initier la prise en charge des patients suspects de souffrir soit d’un angor instable soit d’un infarctus du myocarde avec ou sans sus décalage du segment ST. La douleur thoracique n’en est qu’un des éléments. L’électrocardiogramme (ECG) et la troponine font partie intégrante du raisonnement diagnostique face à un SCA. Quand la troponine reste normale, on parle d’angor instable ; quand elle est augmentée, on parle d’infarctus du myocarde.
Électrocardiogramme
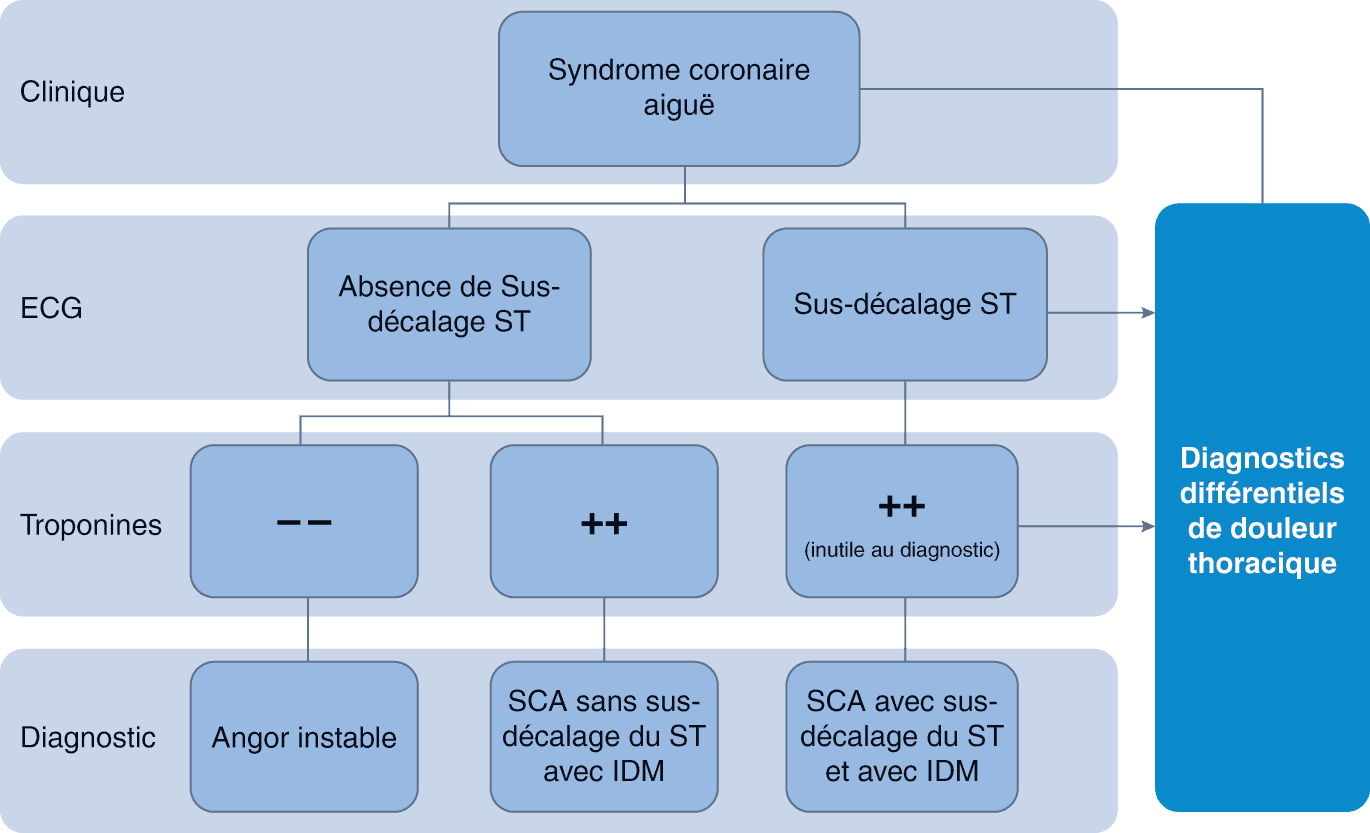
L’interprétation de l’ECG (qui doit être réalisé < 10 minutes après le contact du patient avec un médecin ou une structure de soin) permettra de distinguer deux entités (fig. 3.13) :
- le SCA avec sus-décalage du segment ST (également appelé SCA ST + ou STEMI pour ST-segment elevation myocardial infarction), le sus-décalage devant être résistant à l’administration de dérivés nitrés sous la langue. Attention, l’apparition d’un bloc de branche gauche aigu à la même valeur qu’un sus-décalage du segment ST et permet également de retenir le diagnostic de STEMI. Il est, classiquement, causé par une occlusion coronaire totale et persistante dans le temps. La troponine sera toujours élevée et on peut donc affirmer le diagnostic d’infarctus du myocarde sur les données de la clinique et de l’ECG ;
- le SCA sans sus-décalage du segment ST (également appelé SCA ST- ou NSTEMI pour non ST-segment elevation myocardial infarction) dans lequel l’ECG peut avoir les caractéristiques suivantes : ECG normal, ondes T négatives, ondes T positives anormalement amples et symétriques, sous-décalage du segment ST, etc. (tout sauf un sus-décalage du segment ST). Il est, classiquement, causé par une obstruction coronaire partielle ou une occlusion complète très transitoire. Exceptionnellement, l’occlusion coronaire peut être totale et persistante sans sus-décalage du segment ST (notamment en cas d’atteinte d’une petite branche coronaire du réseau circonflexe). La persistance des symptômes et notamment de la douleur thoracique est alors un argument fort. En l’absence de sus-décalage du segment ST, seuls les dosages répétés de la troponine permettront de faire la différence entre un angor instable et un infarctus du myocarde sans sus décalage du segment ST (SCA ST- troponine + ou NSTEMI pour non ST-segment elevation myocardial infarction).
________________________________________________________________________________
Figure 3.13. Algorithme diagnostique et classification des syndromes coronaires aigus.
________________________________________________________________________________
L’ECG participe aux diagnostics différentiels : péricardite aiguë, embolie pulmonaire, etc.
Biomarqueurs
Les biomarqueurs de souffrance myocardique principal sont la troponine I ou T, spécifique du myocarde. Ils ne sont pas utiles pour le diagnostic de SCA avec sus-décalage du segment ST qui est un diagnostic clinique et électrocardiographique, comme mentionné ci-dessus (la troponine sera toujours élevée, son intérêt est uniquement d’évaluer la taille de l’infarctus et le pronostic).
Ils sont utiles en cas en cas de SCA sans sus-décalage du segment ST pour distinguer (fig. 3.13) :
- l’angor instable qui est un SCA sans infarctus du myocarde (troponines négatives) ;
- l’infarctus du myocarde sans sus-décalage du segment ST (NSTEMI).
Les biomarqueurs peuvent également orienter vers des diagnostics différentiels : myocardite, cardiopathie de stress (Tako-Tsubo), embolie pulmonaire, etc.
________________________________________________________________________________
Important : La troponine est spécifique du myocarde mais n’est pas spécifique de la cause coronaire de la souffrance myocardique.
________________________________________________________________________________
Examen physique
L’examen physique est souvent normal. Il doit permettre d’affiner le niveau de risque cardiovasculaire du patient en mesurant le niveau de la pression artérielle, la fréquence cardiaque, des signes cliniques d’athérome périphérique (souffle vasculaire, absence de pouls périphériques, troubles trophiques, etc.) ou d’hypercholestérolémie familiale (xanthomes tendineux, xanthélasma, etc.).
En cas de SCA, les signes de gravité traduisant les complications du SCA doivent être recherchés :
- souffle à l’auscultation cardiaque (insuffisance mitrale aiguë, communication inter-ventriculaire) ;
- signes d’insuffisance cardiaque et de choc cardiogénique (signes d’hypoperfusion périphérique), classification de Killip (fig. 3.14).
________________________________________________________________________________
Figure 3.14. Classification Killip.

________________________________________________________________________________
L’examen physique doit être complet et doit également systématiquement rechercher les diagnostics différentiels.
Diagnostics différentiels : douleurs thoraciques d’origine non coronaire
L’acronyme PPIED permet de mémoriser les causes les plus fréquentes de douleurs thoraciques non coronaires, cardiovasculaires ou non. À cela, il faut rajouter les causes digestives qui irradient au thorax, les causes pariétales et la cause psychogène.
Pulmonaire (pneumopathie, pneumothorax, pleurésie)
Ce sont des douleurs latéro-thoraciques persistantes et prolongées. Elles sont augmentées par les mouvements respiratoires profonds et atténuées par des mouvements respiratoires superficiels. Elles sont souvent d’origine pleurale. Elles peuvent révéler une pneumopathie aiguë et/ou une pleurésie.
Péricardite aiguë
La douleur de la péricardite aiguë est une douleur d’intensité variable, de type « pleural », renforcée par l’inspiration, la toux, les changements de position et atténuée par la position assise et l’antéflexion. Elle irradie fréquemment vers les muscles trapèzes. Il faut rechercher un syndrome viral accompagnant ou précédant les symptômes.
Le diagnostic peut être retenu en présence de deux critères sur les quatre suivants :
- douleur thoracique évocatrice ;
- frottement péricardique (majoré à l’antéflexion) ;
- épanchement péricardique visible en échocardiographie ;
- ECG évocateur : sus-décalage du segment ST concave, diffus, sans miroir ; sous-décalage du segment PQ ; microvoltage en cas d’épanchement péricardique abondant.
Embolie pulmonaire (voir chapitre 7.3)
Une douleur latéro-thoracique de type pleurale peut révéler une embolie pulmonaire. Les autres signes associés à rechercher sont une dyspnée d’apparition récente, une toux, des signes de thrombose veineuse des membres inférieurs, ainsi que des facteurs favorisant la maladie thromboembolique veineuse (alitement, absence de prophylaxie anti-thrombotique en post-chirurgie, cancer évolutif, etc.). C’est un diagnostic souvent difficile car l’examen clinique et les examens complémentaires de base peuvent être normaux ou montrer des signes non spécifiques.
L’ECG inscrira souvent une simple tachycardie et dans les cas d’EP grave un aspect S1Q3, un bloc de branche droit et des ondes T négatives en V1-V3.
Dissection aortique aiguë (voir chapitre 7.1)
Il s’agit d’une douleur thoracique très intense, brutale, transfixiante et décrite comme une déchirure intra-thoracique. Il est impératif d’évoquer ce diagnostic devant une douleur thoracique aiguë. Il faut rechercher les autres signes évocateurs que sont une asymétrie tensionnelle, l’abolition d’un ou plusieurs pouls périphériques, une ischémie aiguë de membre ou un souffle diastolique d’insuffisance aortique de novo. L’ECG est classiquement normal et il s’agit d’une urgence chirurgicale pour les dissections intéressant la partie proximale de l’aorte thoracique.
________________________________________________________________________________
Attention : Dans certains cas, une dissection aortique proximale peut s’étendre aux coronaires et générer un authentique SCA avec signes ECG.
________________________________________________________________________________
Douleurs thoraciques atypiques
Les autres causes de douleurs thoraciques sont :
- spasme œsophagien ;
- reflux gastro-œsophagien ;
- ulcère gastro-duodénal ;
- autres douleurs d’origine digestive et hépatique. Ce sont des douleurs abdominales en rapport avec une cholécystite, une colique hépatique, ou une pancréatite aiguë. Chacune de ces douleurs, avec ses caractères propres, peut irradier dans le thorax, jusqu’au niveau apical et thoraco brachial.
Deux points sont importants à retenir :
- d’une part, ces douleurs peuvent simuler un angor ou s’intriquer avec d’authentiques douleurs angineuses dont elles constituent le facteur déclenchant ;
- d’autre part, l’hépatalgie d’effort (cf. chapitre 5), qui est une gêne en barre douloureuse de l’épigastre à l’hypochondre droit, peut simuler un angor bas situé par son lien avec les efforts, notamment les efforts de marche, et par sa survenue postprandiale. La constatation d’une hépatomégalie douloureuse à la pression douce de l’hypochondre droit et d’une turgescence spontanée des jugulaires permet aisément de la rattacher à un foie cardiaque.
Algies précordiales d’origine « psychogène »
Elles sont extrêmement fréquentes mais demeurent néanmoins un diagnostic d’élimination.
Ces douleurs sont de localisations très variables d’un épisode à l’autre et d’un interrogatoire à l’autre, fréquemment punctiformes et désignées par le sujet du bout d’un doigt, transfixiantes en « coup d’aiguille » ou « coup de poignard » ; ou parfois plus largement étalées, de topographie latéro-thoracique gauche ou droite, avec ou sans irradiation au bras correspondant où la gêne prend volontiers l’aspect d’un engourdissement ou d’un fourmillement. Le caractère flou et erratique de la douleur, l’absence de tout lien avec l’effort, l’ancienneté des douleurs qui se répètent depuis de nombreuses années sans qu’aucun événement coronaire ne soit venu compliquer cette histoire sont très évocateurs d’une origine psychogène. La durée de ces douleurs est souvent soit excessivement courte (quelques secondes), soit excessivement prolongées durant plusieurs heures sans qu’il n’existe aucun argument clinique, biologique ou ECG pour un infarctus du myocarde.
Douleurs d’origine musculo-squelettiques, ostéo-articulaires et neuropathiques
Discopathie cervicale : ce sont des douleurs cervicobrachiales, non influencées par la marche mais reproduites par un mouvement de la tête ou du cou en rapport avec une pathologie vertébrale cervicale.
Les costo-chondrites ou syndrome de Tietze sont des douleurs para-sternales réveillées par la palpation d’une articulation chondro-costale et ont une haute valeur prédictive négative pour écarter une étiologie coronaire.
Les névralgies aiguës ou post-zostériennes sont de topographie métamérique et de caractéristiques neuropathiques à type de brûlures, de piqûres, de décharges électriques et peuvent concerner la région thoracique. L’inspection cutanée doit donc être systématique et la systématisation du trajet douloureux toujours recherchée à l’examen clinique d’une douleur thoracique.
Dans tous les cas, le doute doit profiter au patient et il est préférable d’évoquer, de rechercher, et d’éliminer le cas échéant une urgence cardiovasculaire (urgence qui met en jeu le pronostic vital à court terme) avant de rechercher un autre diagnostic.
Examens complémentaires
Les examens complémentaires viennent en complément de l’analyse clinique qui doit toujours se situer en amont de leur prescription.
Leur prescription doit tenir compte de leur valeur diagnostique (sensibilité, spécificité, valeurs prédictives positive et négative) pour le problème médical à résoudre, des risques auxquelles ils exposent (liés essentiellement à l’utilisation d’agents de contraste et au caractère invasif ou non de l’examen) et de leur coût (tableau 3.1).
Tableau 3.1. Principaux examens complémentaires en cardiologie.
| Examens | Irradiation | Produit de contraste | Risques liés à l’acte | Coût |
| Biologie : Ddimères, Troponine, BNP… | 0 | 0 | 0 | + |
| ECG, Holter | 0 | 0 | 0 | + |
| Échocardiographie-Doppler | 0 | ± (rare : non iodé) | 0 si transthoracique | ++ |
| Épreuve d’effort | 0 | 0 | ± | + |
| Radiographie thoracique | ++ | 0 | 0 | + |
| Scintigraphie cardiaque ou pulmonaire | ++ | + (traceurs isotopiques) | ± | +++ |
| IRM cardiaque | 0 | + (gadolinium) | ± | +++ |
| Scanner coronaire | +++ | +++ (iodé) | + (allergie) | ++ |
| Coronarographie | +++ | +++ (iodé) | +++ | +++ |
L’intérêt des examens complémentaires et leurs risques doivent être exposés au patient. Celui-ci doit habituellement lire et signer un consentement éclairé avant la réalisation de ceux-ci notamment pour les examens invasifs. Le consentement écrit n’est pas nécessaire pour la réalisation d’un électrocardiogramme de repos, d’un enregistrement de type Holter ou d’une échocardiographie transthoracique simple puisque ces examens n’exposent pas à des risques particuliers.
ECG de repos
L’ECG de repos (toujours 18 dérivations dans la maladie coronaire) du patient coronarien est enregistré le plus souvent en dehors des symptômes (tracé « inter-critique ») plus rarement lors d’un épisode douloureux thoracique (tracé « per-critique »).
ECG inter-critique
Le tracé ECG inter-critique est le plus souvent normal même en cas d’atteinte coronaire sévère. Il peut cependant parfois montrer des anomalies appelées troubles de repolarisation. Il s’agit le plus souvent d’ondes T négatives. Plus rarement, on peut observer des ondes Q séquellaires d’un infarctus ancien. Dans ce cas précis, et en cas d’évolution anévrismale de cet infarctus, il peut persister un sus-décalage du segment ST dans les dérivations en regard de la zone infarcie.
ECG per-critique
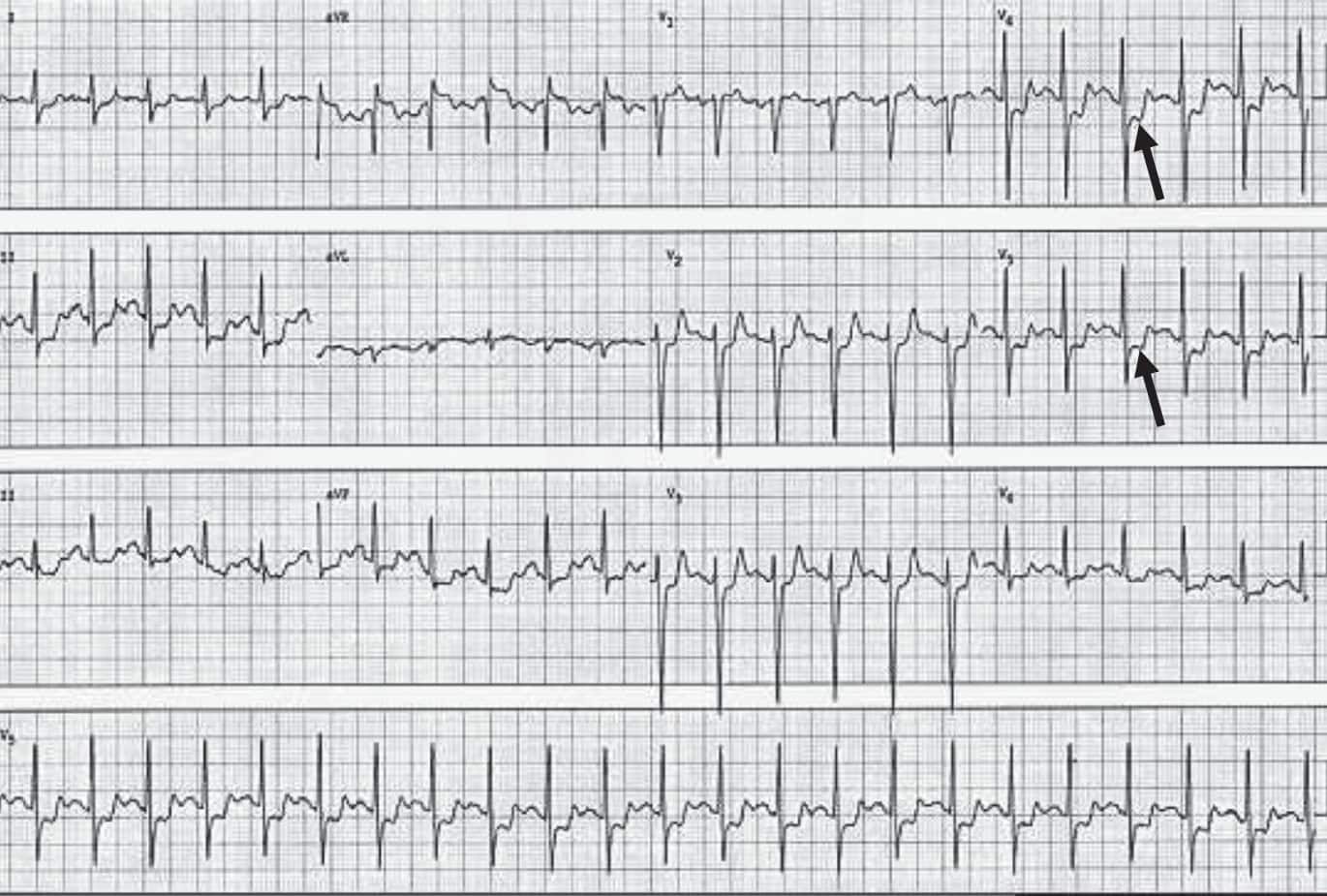
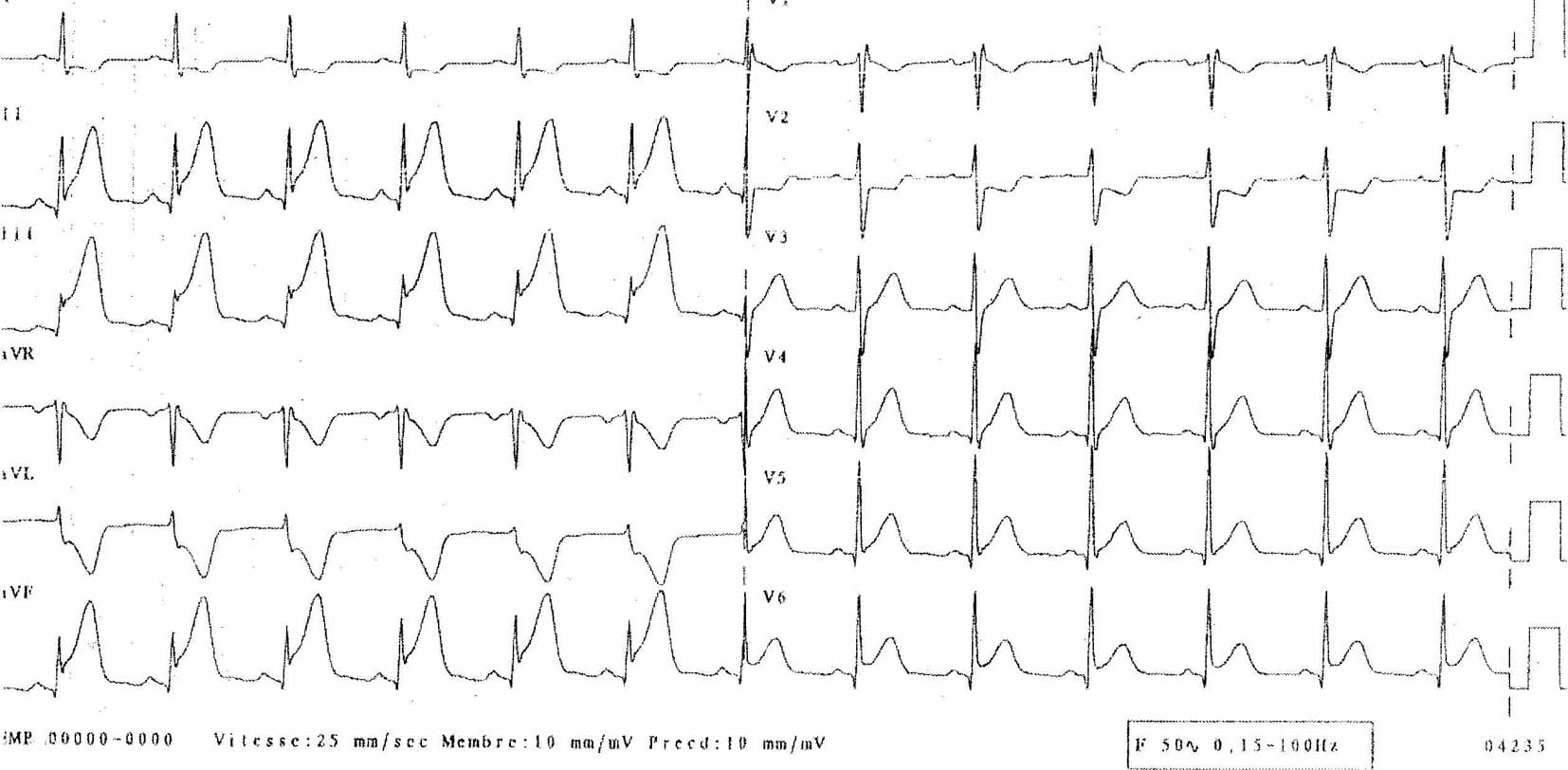
Le tracé ECG per-critique montre fréquemment des modifications de la repolarisation notamment du segment ST dans plusieurs dérivations : sous-décalage de ST le plus souvent (fig. 3.15) ou un sus-décalage de ST per-critique, convexe, en dôme, témoignant d’une ischémie transmurale et classiquement associé à des images en miroir (sous-décalage de ST dans les dérivations opposées qu’il faut systématiquement rechercher) évoquant d’emblée le diagnostic d’infarctus du myocarde avec sus-décalage de ST ou STEMI (onde de Pardee) (fig. 3.16).
________________________________________________________________________________
Figure 3.15. Sous-décalage de ST per-critique net en V4 et V5 notamment (flèches).
________________________________________________________________________________
Figure 3.16. Infarctus inférolatéral aigu avec sus-décalage de ST (net sus-décalage de ST en DII, DIII, aVF, V5, V6).
________________________________________________________________________________
L’évolution de l’ECG dans l’infarctus du myocarde aigu avec sus-décalage du segment ST suit une séquence caractéristique schématisée dans la figure 3.17.
________________________________________________________________________________
Figure 3.17. Évolution de l’ECG dans l’infarctus du myocarde aigu avec sus-décalage du segment ST (STEMI).
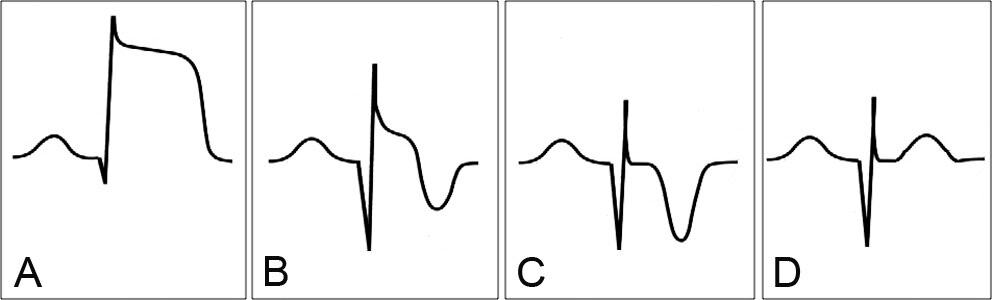
A. Dès les premières minutes suivant l’occlusion artérielle, onde T géante rapidement suivie d’un sus-décalage du segment ST englobant la fin du QRS et l’onde T : c’est la classique onde de Pardee. B. Dans les premières heures, apparition progressive de l’onde Q correspondant à la progression de la nécrose, tandis que le sus-décalage du segment ST régresse et que l’onde T se négative. C. Lorsque le processus de nécrose s’achève : stabilisation de l’onde Q, avec normalisation du segment ST et négativation complète de l’onde T. D. Enfin, dans les semaines qui suivent la phase aiguë, normalisation progressive de l’onde T qui se repositive. Ne reste alors que l’onde Q large et profonde, cicatrice indélébile de l’infarctus (pouvant cependant parfois disparaître à distance).
________________________________________________________________________________
La distribution de ces anomalies sur l’ECG diffère selon l’artère coronaire responsable de l’ischémie myocardique, comme indiqué dans le tableau 3.2.
Tableau 3.2. Correspondances usuelles entre territoires myocardiques, artères coronaires et ECG dans le SCA avec sus-décalage du segment ST (STEMI).
| Territoires myocardiques | Artères coronaires correspondantes | Dérivations ECG |
| Antérieur étendu (face antérieure du VG et deux tiers du septum interventriculaire) | Artère interventriculaire antérieure (et artères diagonales et septales) | V1, V2, V3, V4, voire jusqu’en V5, V6 |
| Antérieurs plus limités | V1, V2 (septal), V3, ou V4 (apical) | |
| Inférieur ± latéral | Coronaire droite et/ou artère circonflexe | D2, D3, VF, ± V5, V6 voire V7 |
| Ventricule droit | Coronaire droite | V3R, V4R |
Holter-ECG
Le holter-ECG est l’enregistrement continu de l’électrocardiogramme pendant 24 heures le plus souvent (ou plus en fonction de la fréquence des symptômes), ensuite analysé par système informatique. Surtout utilisé pour détecter des troubles du rythme paroxystiques, il peut permettre d’enregistrer des variations paroxystiques du segment ST qui peut sous-décaler ou sus-décaler de manière transitoire pendant une période plus ou moins brève. Cette information est de très grande valeur si elle est contemporaine d’une douleur thoracique perçue par le patient.
En pratique, cet examen n’est quasiment jamais utilisé pour faire le diagnostic de coronaropathie mais davantage pour documenter les rythmes cardiqaues.
Épreuve d’effort
Le fonctionnement du cœur est profondément modifié par l’effort physique et de nombreuses anomalies ne se démasquent qu’à l’occasion d’un effort. Ceci justifie la réalisation d’explorations fonctionnelles à l’effort, ou épreuve d’effort.
Principe
Il s’agit de faire réaliser au sujet un effort d’intensité croissante soit sur une bicyclette ergométrique dont on augmente progressivement la charge du pédalage, soit sur un tapis roulant dont on augmente par paliers la vitesse et/ou la pente. La durée des paliers est variable, généralement de deux à trois minutes Cet examen se fait sous la surveillance du cardiologue et de l’infirmière présents dans la salle pendant l’examen et au minimum les six premières minutes de récupération après l’effort.
Indications
Les indications retenues pour la maladie coronaire sont :
- le diagnostic de l’origine coronaire de douleurs thoraciques plus ou moins évocatrices d’angor. Dans ce cas, l’épreuve d’effort a une sensibilité diagnostique optimale si l’effort permet d’atteindre la fréquence cardiaque maximale théorique (FMT = 220 – âge ; par exemple pour 70 ans, la FMT = 220 – 70 soit 150/min). Cet examen est de valeur limitée puisque sa sensibilité est de 65 % et sa spécificité est de 80 % environ. Ceci explique la nécessité fréquente de recourir à d’autres investigations paracliniques couplant effort (ou stress pharmacologique) et imagerie (échocardiographie d’effort, échocardiographie sous stress pharmacologique, scintigraphie myocardique, IRM de stress) pour résoudre cette question diagnostique ;
- l’évaluation fonctionnelle après mise en œuvre de mesures thérapeutiques (médicamenteuse ou revascularisation coronaire).
Critères d’évaluation
Dans la maladie coronaire, le diagnostic positif en faveur d’une ischémie myocardique est habituellement le constat à l’effort d’un sous-décalage du segment ST horizontal ou descendant, supérieur à 1 mm, mesuré 80 millisecondes après la fin du complexe QRS (point J), habituellement dans plusieurs dérivations contiguës (souvent en V5, V6, parfois les dérivations inférieures mais moindre spécificité) accompagné ou non d’un angor (fig. 3.18). Ce sous-décalage du ST n’a aucune valeur localisatrice (pas d’information sur la coronaire atteinte).
________________________________________________________________________________
Figure 3.18. Épreuve d’effort.
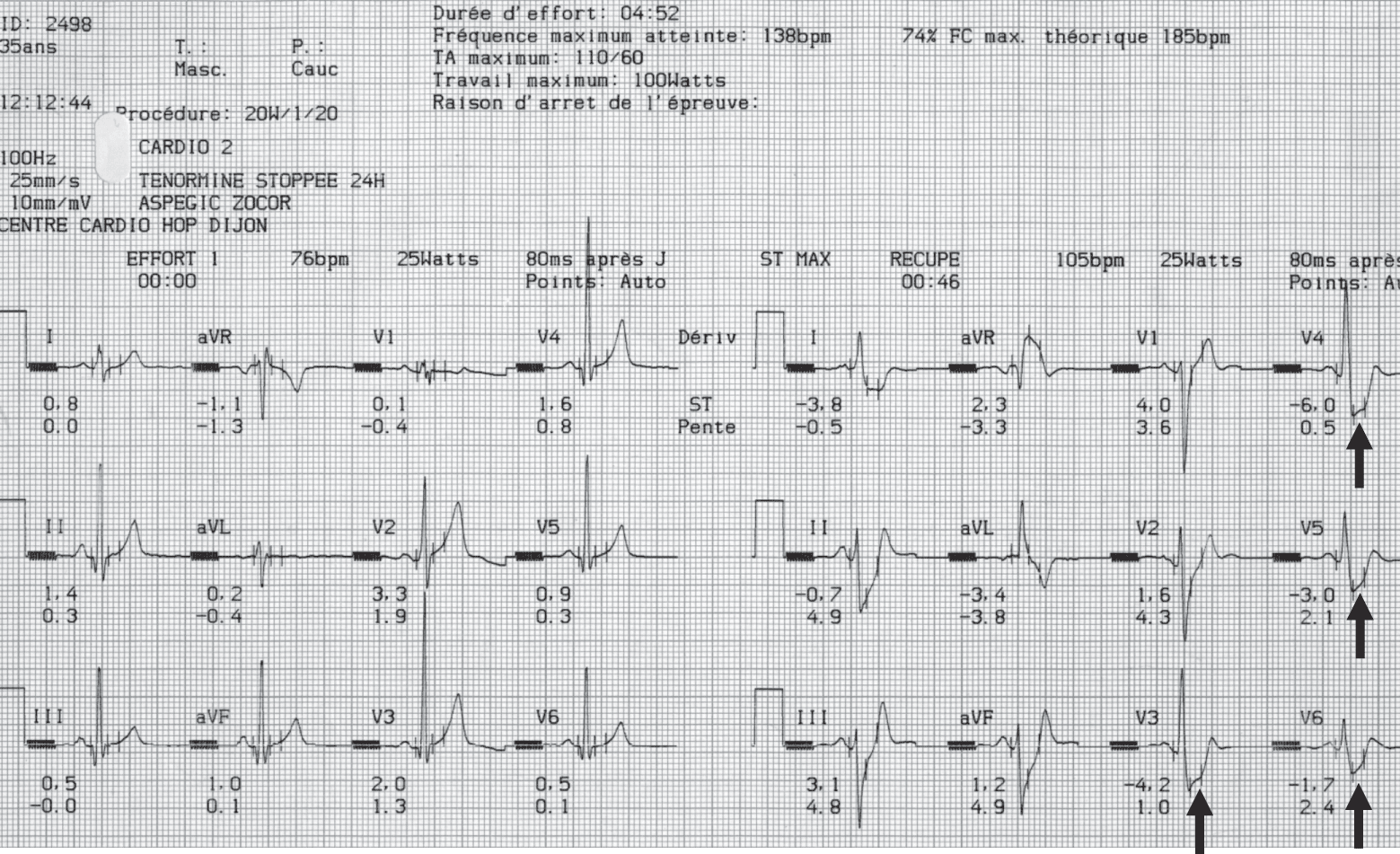
À gauche tracé de repos. À droite sous-décalage de ST pendant l’effort (net de V3 à V6, bien que légèrement ascendant : flèches). Le patient était atteint d’une sténose du tronc coronaire gauche.
________________________________________________________________________________
Le test est négatif si la fréquence cardiaque atteint au moins 85 % de la FMT sans angor ni sous-décalage de ST et litigieux en cas de douleurs thoraciques angineuses sans modification de l’ECG. Le test est non diagnostique, s’il reste négatif mais que le patient n’a pas atteint une fréquence cardiaque suffisante pour conclure (< 85 % de la FMT).
Les critères de mauvais pronostic sont l’apparition de symptômes ou de modifications électriques pour une faible charge d’effort, une chute de la pression artérielle de plus de 10 mmHg au pic de l’effort, la persistance des symptômes et des modifications de l’électrocardiogramme à distance de l’arrêt de l’effort, ou la survenue de troubles du rythme ventriculaire sévères.
Échocardiographie
Cet examen d’imagerie par ultrasons est indispensable et indiqué au repos dans le cadre du suivi du patient coronarien. L’échocardiographie transthoracique (ETT), disponible, non irradiante, de faibles coûts, est l’examen réalisé habituellement en première intention. Elle n’a pas de valeur fonctionnelle lorsqu’elle n’est pas couplée à un stress (effort ou pharmacologique) mais peut mettre en évidence des anomalies de la cinétique segmentaire, c’est-à-dire les zones de myocarde se contractant peu ou pas du tout en systole – ce qui suggère une ischémie myocardique évolutive chez un patient présentant des douleurs thoraciques dans un contexte de syndrome coronaire aigu ou une séquelle de nécrose chez un patient ayant des antécédents d’infarctus –, ou de la cinétique globale, ou une dysfonction des valves atrioventriculaires (mitrale surtout évoquant une dysfonction valvulaire) pouvant faire suspecter l’existence d’une maladie coronaire évolutive et/ou passée.
L’échocardiographie transœsophagienne (ETO) n’a pas d’indication dans l’évaluation de la maladie coronaire sauf en cas de suspicions de complication hémodynamique, et doit être remplacée par une autre technique d’imagerie en cas d’impossibilité de réaliser un examen par voie transthoracique.
Tests d’ischémie couplés à une imagerie
L’échocardiographie de stress, la scintigraphie myocardique, et l’IRM de stress sont des examens non ou peu invasifs et performants. Ils sont très fréquemment utilisés pour confirmer ou non le diagnostic de maladie coronaire probable (et son type, ischémie, infarctus, zone myocardique viable, etc.), préciser son pronostic et poser une indication thérapeutique.
Principes
Ces enregistrements externes du fonctionnement cardiaque utilisent des principes physiques différents : ultrasons pour l’échographie, traceurs isotopiques pour la scintigraphie et résonance magnétique pour l’IRM.
La scintigraphie myocardique nécessite l’injection d’un traceur isotopique à tropisme myocardique, marqué le plus souvent avec du technétium 99m. En échocardiographie, on peut utiliser un produit de contraste ultrasonore, afin d’améliorer la visualisation des contours endocardiques, notamment chez les patients les moins échogènes. L’IRM est le plus souvent couplée à l’injection d’un produit de contraste non iodé appelé gadolinium.
Ces examens sont également couplés à un stress myocardique : effort (scintigraphie, échocardiographie de stress) ou stimulations pharmacologiques (échocardiographie sous perfusion de dobutamine à dose croissante, scintigraphie myocardique après injection de dipyridamole, IRM sous dobutamine ou dipyridamole, etc.).
Indications et résultats au cours de la maladie coronaire
Les principales informations recherchées sont :
- l’existence de zones d’ischémie ou de nécrose myocardique et leur étendue (pourcentage de myocarde concerné), et la mise en évidence d’une viabilité myocardique au sein d’une zone infarcie (réserve contractile) ;
- les paramètres de fonction myocardique segmentaire et globale, notamment fraction d’éjection du ventricule gauche (FEVG), volumes ventriculaires gauches… ;
Le tableau 3.3 permet de s’orienter dans le choix des examens demandés.
Tableau 3.3. Orientation pour la prescription de l’imagerie dans la maladie coronaire.
| Question(s) clinique(s) | ETT | Isotopes | Scanner | IRM |
| Sténose coronaire | 0/+ | 0 | ++ | + |
| Ischémie | ++ (ETT de stress) | ++ | + ? | ++ |
| Nécrose | ++ (ETT de stress) | ++ | + | +++ |
| Viabilité | ++ (ETT de stress) | ++ | + | +++ |
| FEVG | ++ | +++ | ++ | +++ |
| Volumes VG | ++ | ++ | ++ | +++ |
| Complications aiguës | +++ | 0 | ++ | + |
| Diagnostics différentiels :
– myocardite – péricardite liquidienne – dissection aortique – embolie pulmonaire |
++++
++ (ETO) ++ |
+ ?0
0 ++⁎ |
0 ?++
+++ +++ |
++++++
+++ 0 ? |
⁎ En utilisant un traceur de perfusion pulmonaire : micro-agrégats d’albumine marqués au technétium 99m. ETT, écho-Doppler cardiaque transthoracique ; ETO, écho-Doppler transœsophagien.
En combinant les examens usuels de repos et de stress, il est possible de proposer une analyse des différents segments du myocarde ventriculaire gauche, comme résumé de manière schématique dans le tableau 3.4.
Tableau 3.4. Analyse schématique du résultat des examens de repos et de stress.
| État du myocarde | Sain et normalement perfusé | Nécrosé | Ischémique | Viable
(« hibernant ») |
| Contraction de repos⁎ | Normale | Nulle dans la zone atteinte | Souvent diminuée dans la zone atteinte | Faible ou nulle dans la zone atteinte |
| Perfusion myocardique isotopique au repos | Normale | Pas de fixation dans la zone atteinte | Souvent faible et retardée | Souvent faible et retardée dans la zone |
| Perfusion IRM au repos
– images précoces – images tardives (10 minutes) |
Normale
Pas de fixation du gadolinium |
Faible ou absente
Fixation tardive du gadolinium fréquente |
Faible dans la zone atteinte | Faible dans la zone
Faible fixation de gadolinium |
| Contraction de stress⁎ | Augmentée | Nulle dans la zone atteinte | Variable
Se dégrade sous forte stimulation |
Présente sous faible stimulation |
| Perfusion myocardique isotopique de stress | Normale | Nulle dans la zone atteinte | Diminuée dans la zone atteinte | Peut s’améliorer |
⁎ Étudiées en échocardiographie, voire en angiographie isotopique, en tomoscintigraphie synchronisée ou en IRM (vidéo 3.1).
Étudiées en échocardiographie, voire en angiographie isotopique, en tomoscintigraphie synchronisée ou en IRM (vidéo 3.1).
Quelques exemples iconographiques font l’objet des fig. 3.19 à 3.26.
________________________________________________________________________________
Figure 3.19. Scintigraphie myocardique synchronisée à l’ECG. La perfusion myocardique, appréciée par la distribution du traceur, est homogène au repos.
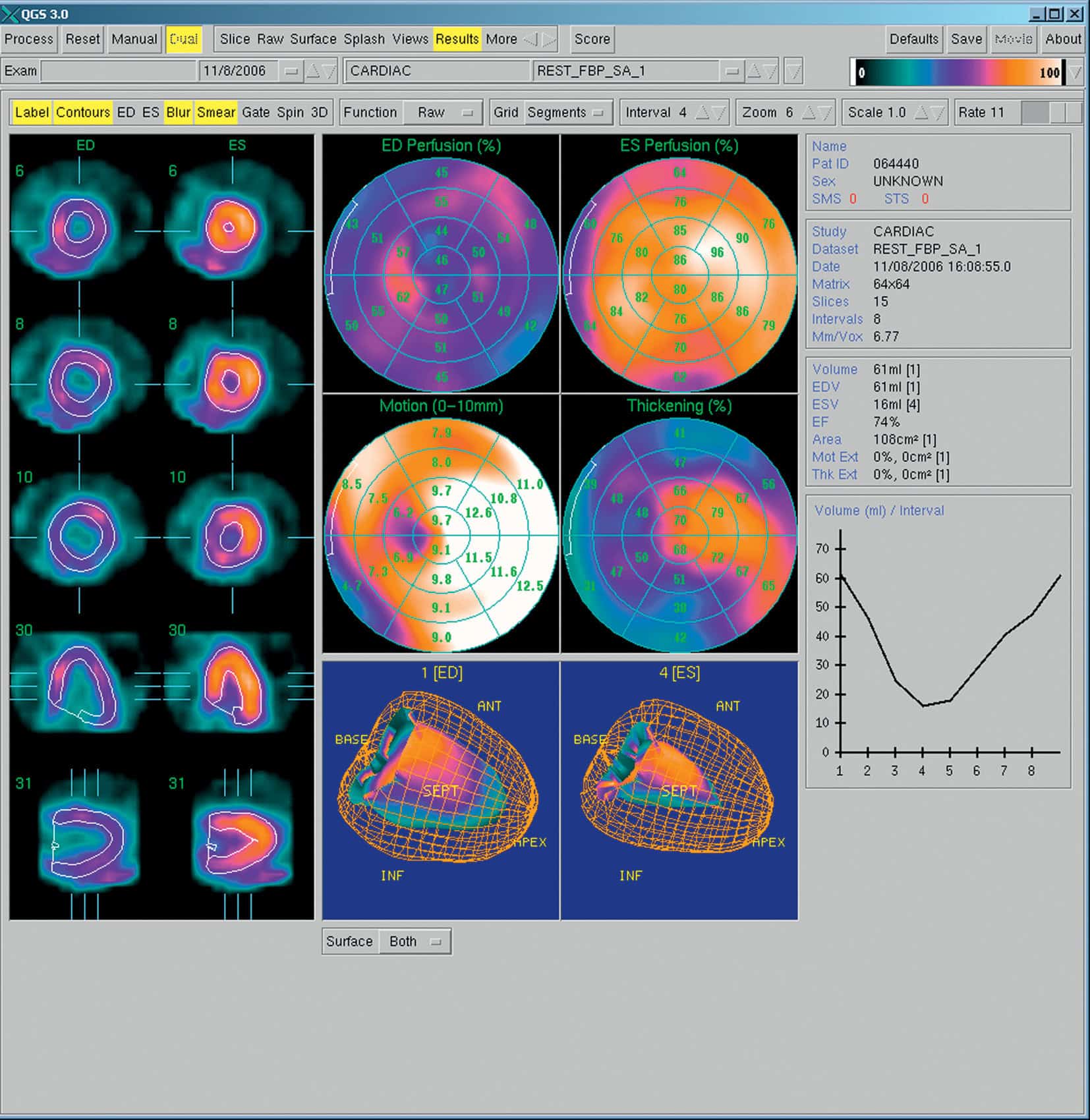
________________________________________________________________________________
Figure 3.20. Scintigraphie myocardique. Aspect de séquelle de nécrose dans le territoire inférieur (flèches).
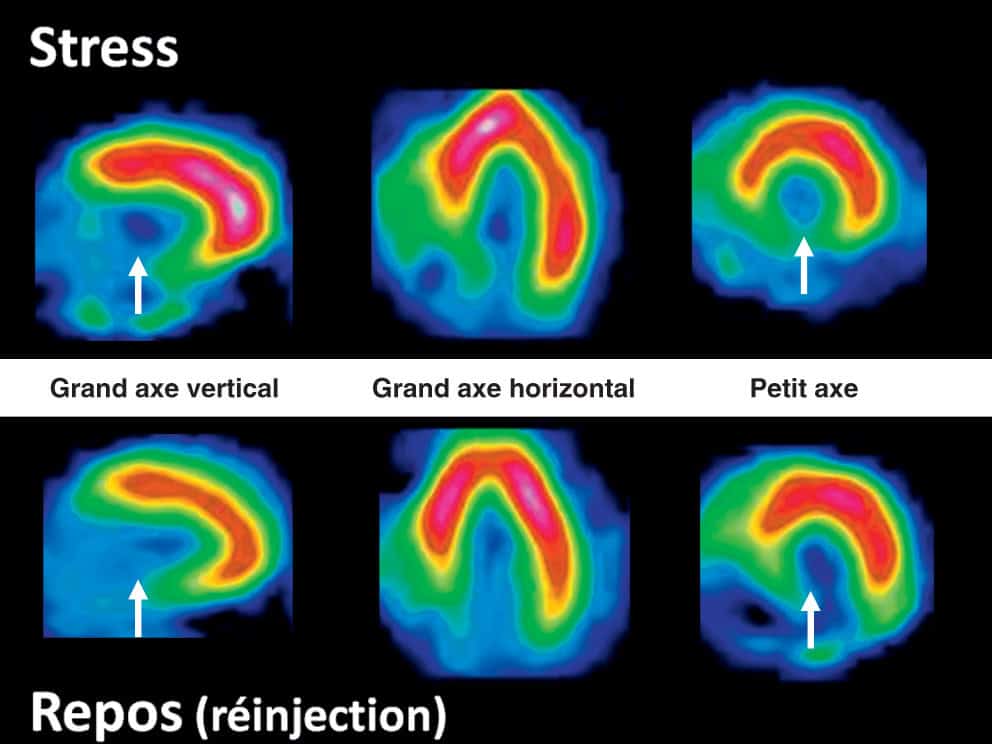
Pas de fixation du traceur dans la zone en post-stress comme au repos : images quasi identiques.
________________________________________________________________________________
Figure 3.21. Scintigraphie myocardique. Ischémie myocardique dans le territoire apical.
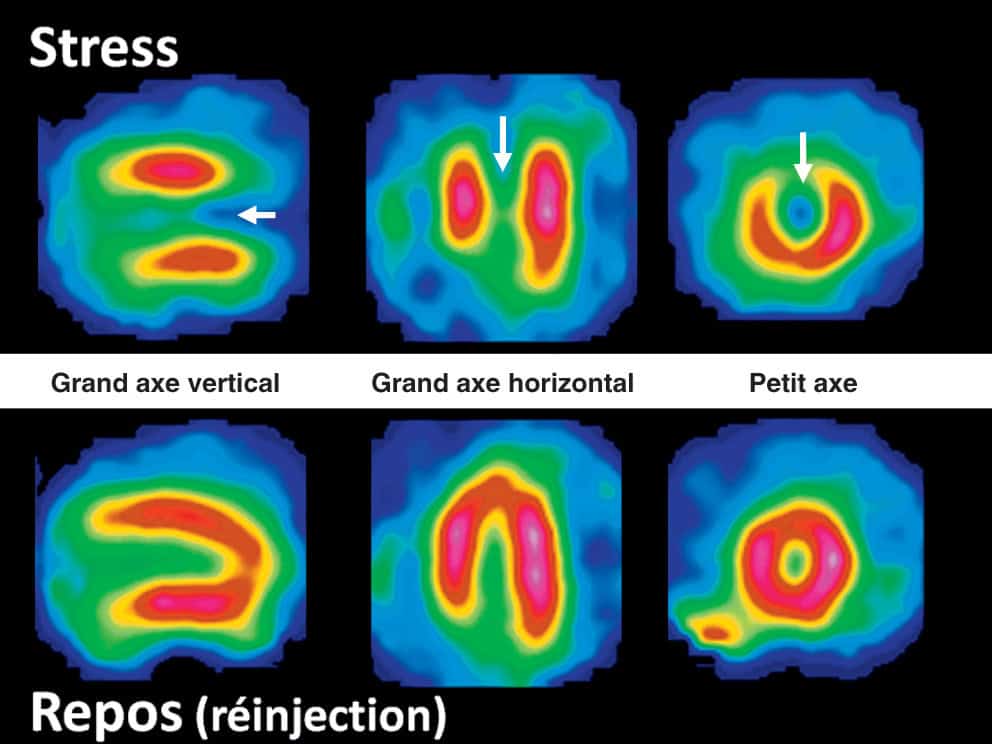
Pas de fixation en post-stress (flèches) dans la zone, mais fixation au repos.
________________________________________________________________________________
Figure 3.22. Scanner coronaire.
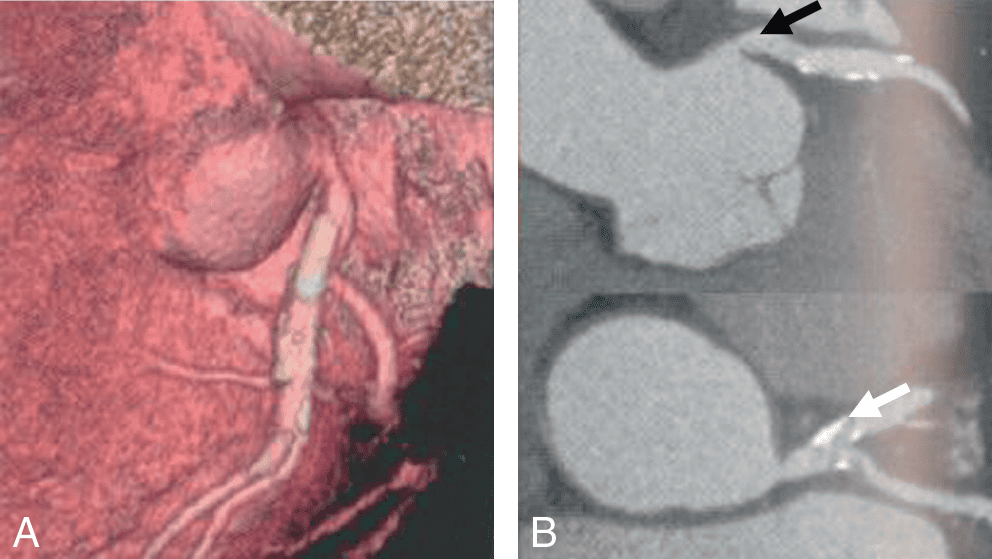
Sténose de l’ostium du tronc coronaire gauche (flèche noire). Noter les calcifications pariétales (flèche blanche).
Source : Vignaux O. Imagerie cardiaque : scanner et IRM. 2e édition. Paris : Elsevier-Masson ; 2011.
________________________________________________________________________________
Figure 3.23. Échographie transthoracique.
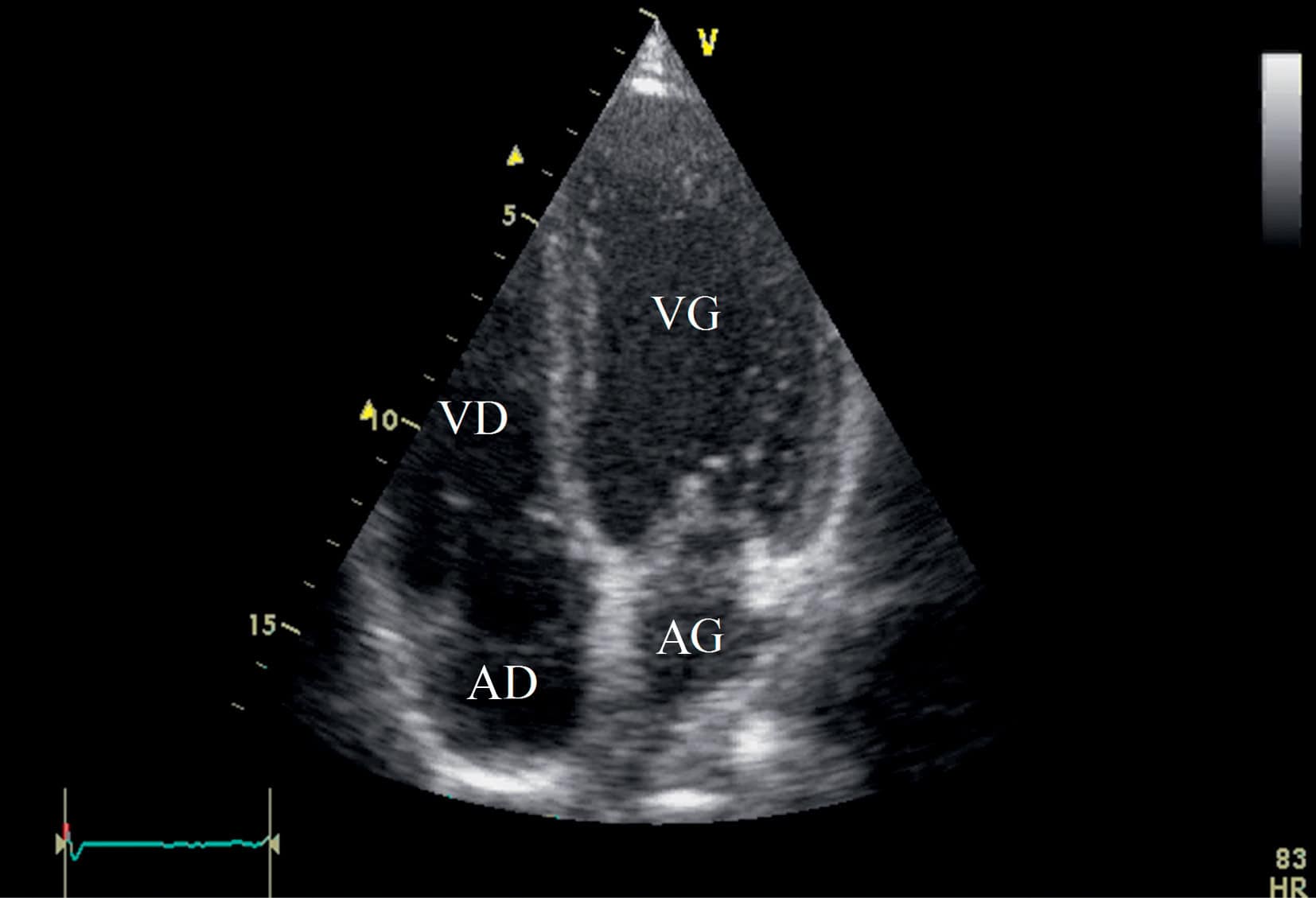
Incidence « 4 cavités » par voie apicale.
AD, atrium droit ; AG, atrium gauche ; VD, ventricule droit ; VG, ventricule gauche.
________________________________________________________________________________
Figure 3.24. Échographie transthoracique. Mesure de la FEVG par la méthode de Simpson biplan.
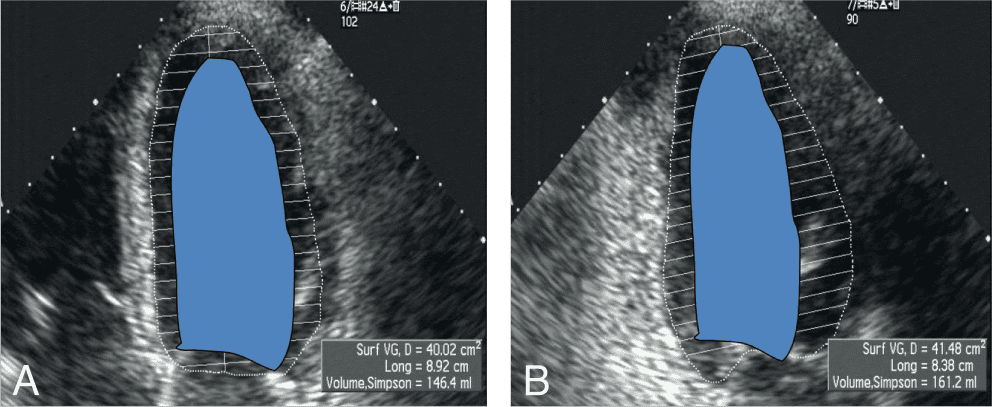
A. Incidence « 4 cavités » par voie apicale. B. Incidence « 2 cavités » par voie apicale.
________________________________________________________________________________
Figure 3.25. Angiographie isotopique : mesure de la FEVG, ici très abaissée à 14 %.
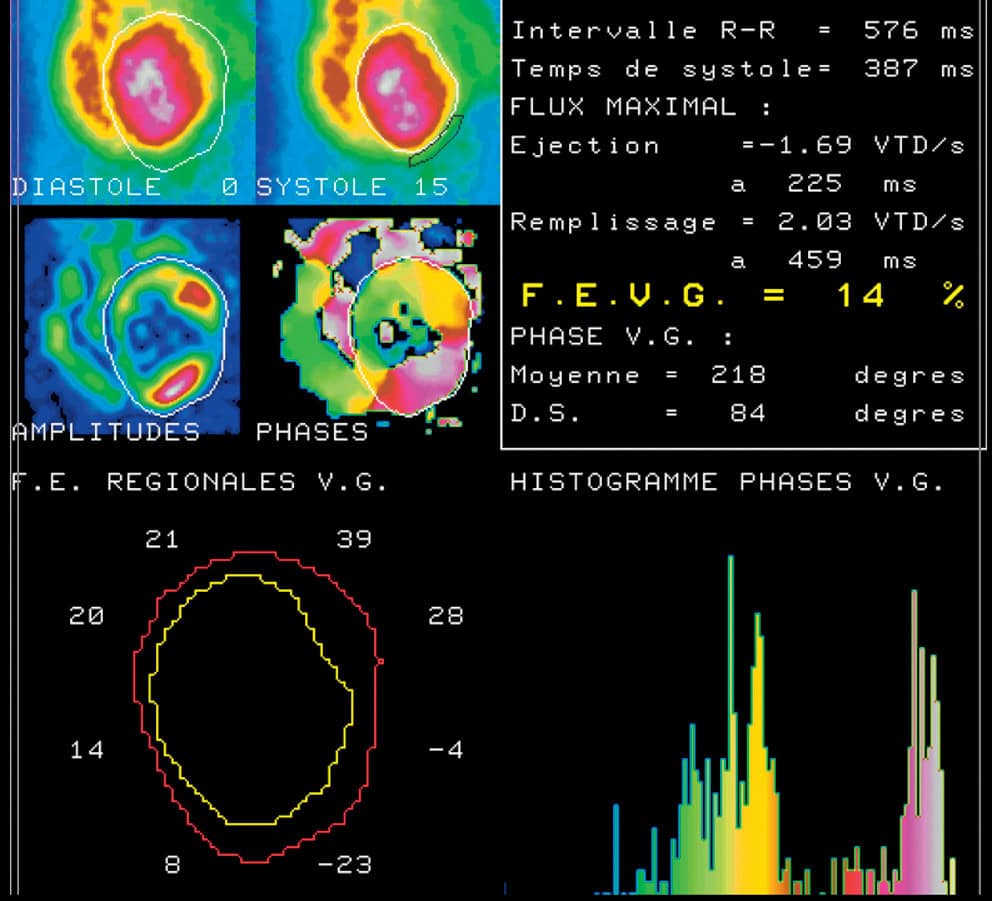
________________________________________________________________________________
Figure 3.26. IRM cardiaque après injection de gadolinium.
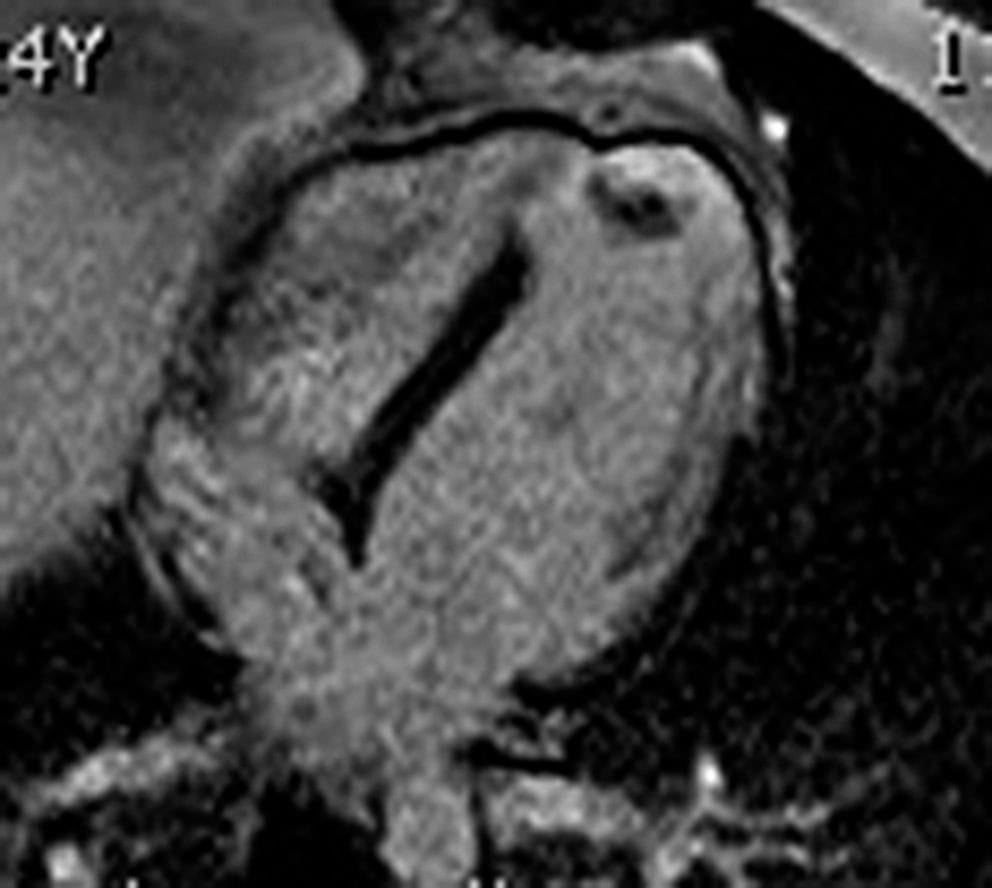
Séquence de rehaussement tardif (PSIR) réalisée dans le plan « quatre cavités » 15 minutes après injection de gadolinium. Infarctus transmural antéro-septo-apical. Notez le myocarde normal septal et la paroi latérale en hyposignal franc.
Source : Vignaux O. Imagerie cardiaque : scanner et IRM. 2e édition. Paris : Elsevier-Masson ; 2011.
________________________________________________________________________________
À noter que, tout comme l’échocardiographie, l’IRM cardiaque et la scintigraphie myocardique sont des examens pouvant être réalisés uniquement au repos. L’IRM cardiaque, gold standard de l’exploration anatomique cardiaque, permet de préciser chez le coronarien l’existence de troubles de la cinétique segmentaire ou globale ainsi que les fonctions ventriculaires gauche et droite. Elle permet également de détecter la fibrose myocardique. La scintigraphie myocardique au repos, l’échographie de stress sous faible dose de dobutamine et l’IRM permettent d’apprécier l’existence d’une viabilité myocardique résiduelle.
Scanner coronaire
La sensibilité et la spécificité du scanner coronaire pour la détection des lésions coronaires sont évaluées entre 95 % et 98 %. L’un des intérêts majeurs de cet examen est sa très forte valeur prédictive négative, qui peut atteindre jusqu’à 99 %.
Cet examen est, cependant, parfois limité par les calcifications coronaires, qu’il peut d’ailleurs quantifier. Il est par ailleurs de réalisation difficile chez les patients tachycardes ou dont le rythme cardiaque est irrégulier (fibrillation atriale notamment). Son apport est par ailleurs anatomique et non pas fonctionnel. En cas de sténose coronaire, il n’apporte à ce jour pas de renseignement fiable sur un éventuel retentissement de cette lésion sur la perfusion coronaire (même si de nouvelles techniques analysant la perfusion myocardique (analyse de la FFR) au scanner sont en cours de développement).
Coronarographie
La coronarographie reste l’examen de référence, en particulier en cas de syndrome coronaire aigu, elle permet de préciser de façon quantitative le degré des sténoses, le nombre de lésions ainsi que leur type en précisant longueur, excentricité, présence d’une occlusion, atteinte d’une branche de bifurcation ou au contraire lésions diffuses sur le réseau coronaire.
C’est l’opacification sélective successive des deux artères coronaires à l’aide de cathéters adaptés introduits successivement dans les deux ostia coronaires, gauche et droit, par voie artérielle radiale ou fémorale (rarement humérale).
On enregistre, à l’aide d’une caméra détectant les rayons X, l’opacification coronaire dans diverses incidences pour analyser les différents segments artériels afin de rechercher des lésions à type de sténoses et/ou la présence de thrombus intra-luminal.
La numérisation des images permet des études quantitatives (diamètre des artères, diamètre minimal et longueur des sténoses).
Dans le même temps d’exploration, il est possible de placer un cathéter dans le ventricule gauche pour réaliser un enregistrement des pressions dans les différentes cavités explorées (cathétérisme cardiaque avec étude hémodynamique). Il est également possible d’opacifier la cavité ventriculaire gauche avec du produit de contraste (ventriculographie gauche), ce qui permet d’analyser la cinétique segmentaire de sa paroi et de la corréler à l’état des artères coronaires et/ou de quantifier une fuite mitrale (la ventriculographie n’est quasiment plus utilisée actuellement car l’échocardiographie apporte des renseignements similaires en évitant d’injecter du produit de contraste). De la même façon, il est possible de réaliser des angiographies aortiques sus-sigmoïdiennes en injectant du produit de contraste dans l’aorte ascendante qui permettra de préciser l’anatomie de l’aorte ascendante et/ou de quantifier une régurgitation quantifiée en endocardiographie-Doppler aortique.
Une information précise du patient avec consentement signé doit être donnée avant l’examen (hors contexte d’urgence) et conservée dans le dossier du patient.
Les données de l’examen sont enregistrées, numérisées puis stockées sur support digital et mémoire informatique (réseaux d’images).
Les incidents et accidents, rares, mais dont certains peuvent mettre en jeu le pronostic vital sont :
- locaux, liés à la voie d’abord : hématome ou faux-anévrisme, thrombose artérielle avec ischémie aiguë d’un membre, dissection artérielle rétrograde, fistule artério-veineuse (surtout en cas d’abord par voie fémorale) ;
- cardiaques : dissection de l’aorte ou coronaire liée au cathéter, perforation coronaire voire rupture coronaire au cours de l’angioplastie qui peut être responsable d’une tamponnade ;
- liés au produit de contraste : réaction allergique (pouvant aller jusqu’au choc anaphylactique), néphrotoxicité des produits de contraste se traduisant par une insuffisance rénale aiguë pouvant aller jusqu’à la dialyse (risque plus prononcé chez les patients diabétiques, insuffisants rénaux chroniques ou présentant une instabilité hémodynamique notamment). Il peut être nécessaire de réaliser une préparation spécifique chez les patients insuffisants rénaux et de stopper transitoirement certains traitements (antidiabétiques oraux comme la metformine) au moment et dans les jours qui suivent l’examen.
- la maladie des micro-emboles de cholestérol (syndrome des orteils bleus) ;
- le sepsis.
Aspect normal
La distribution la plus habituelle du réseau artériel coronaire (cf. supra, Anatomie) est représentée schématiquement dans les figures suivantes (fig. 3.27 et 3.28).
________________________________________________________________________________
Figure 3.27. Coronaire gauche.
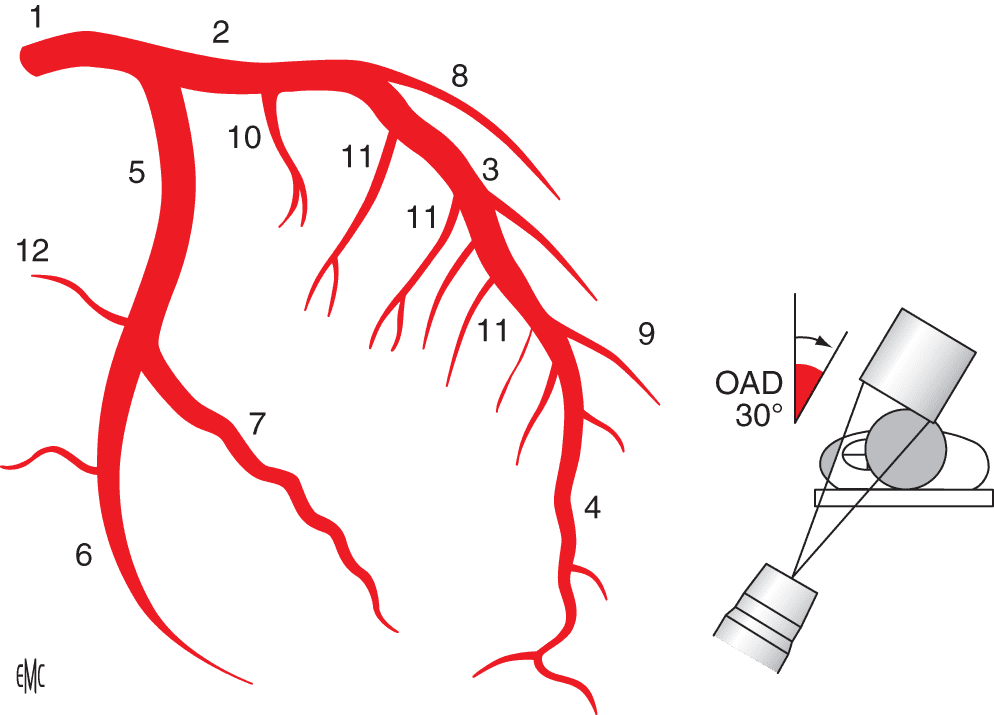
Coronarographie. Coronaire gauche : incidence oblique antérieure droite (OAD) 30°.
1. Tronc coronaire gauche. 2. Interventriculaire antérieure proximale. 3. Interventriculaire antérieure moyenne. 4. Interventriculaire distale. 5. Circonflexe proximale. 6. Circonflexe distale. 7. Marginale gauche. 8. Première diagonale. 9. Deuxième diagonale. 10. Première perforante septale. 11. Septales. 12. Branche auriculaire de la circonflexe.
Source : Bertrand M-E, 1978. In : Gibault-Genty G, Georges J-L. Cathétérisme cardiaque, angiocardiographie et coronarographie. Technique et résultats. Encycl Méd Chir (Elsevier, Paris), Radiologie et imagerie médicale. 32-005-C-30, 2009. Copyright © 2009 Elsevier Masson SAS. Tous droits réservés.
________________________________________________________________________________
Figure 3.28. Coronaire droite.
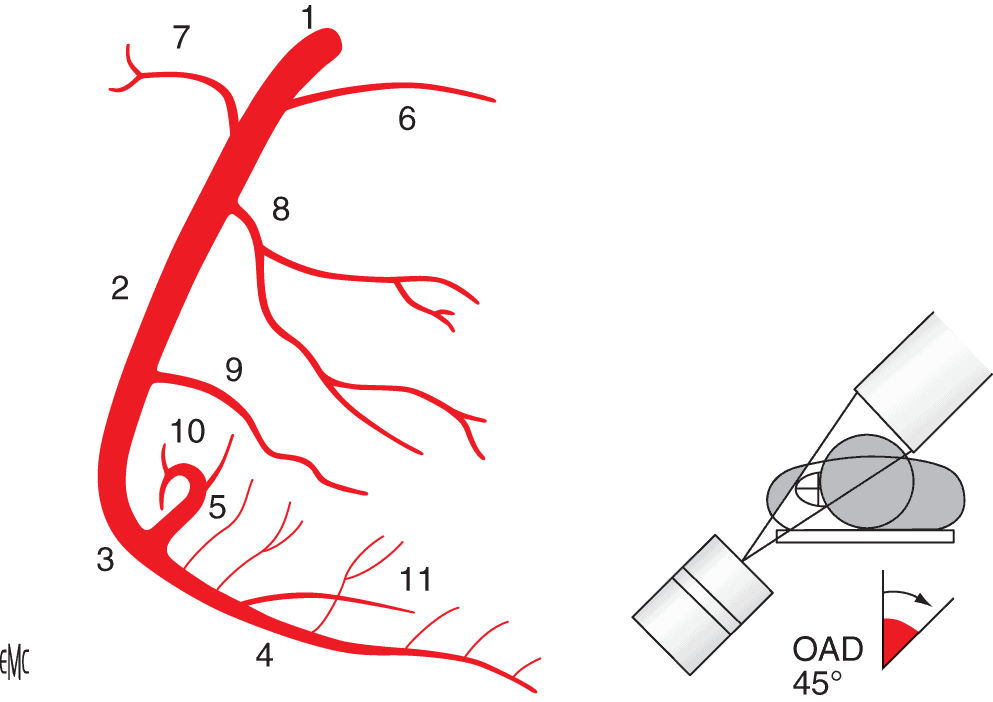
Coronarographie. Coronaire droite : incidence oblique antérieure droite (OAD) 45°.
1. Premier segment (horizontal) de la coronaire droite. 2. Deuxième segment (vertical) de la coronaire droite. 3. Troisième segment (horizontal) de la coronaire droite. 4. Interventriculaire postérieure. 5. Rétroventriculaire. 6. Artère du cône. 7. Artère du nœud sinusal. 8. Artère ventriculaire droite. 9. Artère marginale droite. 10. Artère du nœud auriculoventriculaire. 11. Septales inférieures.
Source : Bertrand M-E, 1978. In : Gibault-Genty G, Georges J-L. Cathétérisme cardiaque, angiocardiographie et coronarographie. Technique et résultats. Encycl Méd Chir (Elsevier, Paris), Radiologie et imagerie médicale. 32-005-C-30, 2009. Copyright © 2009 Elsevier Masson SAS. Tous droits réservés.
________________________________________________________________________________
Aspects pathologiques
Les artères coronaires peuvent présenter divers types de lésions.
Sténoses (rétrécissement)
Plus ou moins serrées (considérées comme significatives si supérieures à 50 %–70 % du diamètre), plus ou moins longues, tortueuses, calcifiées. Des classifications permettent de les décrire et d’en juger la sévérité.
Sur chaque artère, la localisation de la sténose aura un retentissement d’autant plus important qu’elle sera plus proximale, plus serrée et plus longue (fig. 3.29)
________________________________________________________________________________
Figure 3.29. Coronarographie. Sténose serrée calcifiée et excentrée du tronc commun de la coronaire gauche.
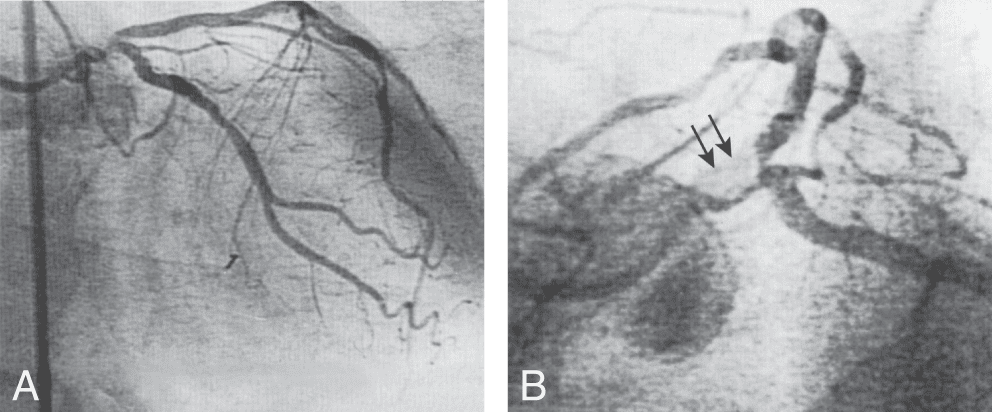
A. En incidence oblique antérieure droite (OAD) 30°. B. En incidence oblique antérieure gauche (OAG) 45° et craniocaudale 25°.
Source : Bertrand M-E, 1978. In : Gibault-Genty G, Georges J-L. Cathétérisme cardiaque, angiocardiographie et coronarographie. Technique et résultats. Encycl Méd Chir (Elsevier, Paris), Radiologie et imagerie médicale. 32-005-C-30, 2009. Copyright © 2009 Elsevier Masson SAS. Tous droits réservés.
________________________________________________________________________________
On parlera d’atteinte mono-, bi- ou tritronculaire selon le nombre de troncs principaux lésés (IVA-diagonales, coronaire droite, circonflexe-marginales).
Le degré de sévérité anatomique des sténoses peut être quantifié par analyse informatisée (quantification acoustique, QCA), le cathéter d’injection (de diamètre connu) servant à l’étalonnage.
Une sténose du tronc coronaire gauche de plus de 50 % est considérée comme serrée car la quantité de myocarde ventriculaire gauche qui en dépend est importante (fig. 3.29). L’indication d’une revascularisation est proposée dans les recommandations internationales.
Occlusions
Ces occlusions peuvent être aiguës, essentiellement thrombotiques, notamment lors de la survenue d’un infarctus du myocarde aigu ou, au contraire, chroniques par athérome organisé souvent calcifié. Une perfusion coronaire au-delà de la thrombose par une collatéralité est possible et en limite les conséquences néfastes.
Spasme
Contraction paroxystique inappropriée d’une zone artérielle coronaire, il peut être observé spontanément ou provoqué pharmacologiquement pendant l’examen coronarographique par injection intraveineuse de méthylergométrine, Méthergin® (par exemple), qui est un vasoconstricteur coronaire.
Compression extrinsèque
Il est possible d’observer sur certains segments coronaires un trajet intra-myocardique responsable d’une compression extrinsèque de l’artère rythmée par les contractions ventriculaires (pont musculaire, compression systolique). C’est généralement le segment moyen de l’artère interventriculaire antérieure qui est concerné. La compression peut aller jusqu’à être responsable d’un arrêt complet du flux sanguin dans l’artère et être à l’origine de symptômes ou d’événements cardiaques ± graves (syndrome coronaire aigu, troubles du rythme ventriculaire).
Explorations fonctionnelles et imagerie de la paroi des artères coronaires au cours de la coronarographie
Plusieurs techniques complémentaires d’analyse des lésions coronaires au cours de la coronarographie diagnostique ont été développées ces dernières années.
- La mesure de la FFR ou fraction de réserve coronaire consiste à mesurer l’impact hémodynamique (ou fonctionnel, générant une ischémie) d’une sténose coronaire visible en angiographie. Pour cela, l’opérateur utilise un guide de pression qui recueille la pression dans la coronaire en aval de la sténose (Pd). Il mesure en même temps la pression dans la coronaire en amont de la sténose (Pa). La superposition des courbes de pression permet de rechercher un gradient exprimé par le rapport Pd/Pa qui n’est généralement pas présent au repos sauf en cas de sténose très serrée. L’effort n’étant pas possible pendant une coronarographie, on va simuler ce dernier en injectant de l’adenosine en intraveineux ou en intracoronaire afin d’induire une vasodilatation des microvaisseaux cardiaques en aval de la sténose. Cette vasodilatation induit une hyperhémie et donc une accélération du flux dans la coronaire. Le caractère hémodynamiquement significatif de la sténose sera retenu si Pd/Pa < 80 %. La sténose coronaire sera alors éligible à une revascularisation (fig. 3.30).
________________________________________________________________________________
Figure 3.30. Mesure de la fraction de réserve coronaire (fractional flow reserve ou FFR) au guide de pression.
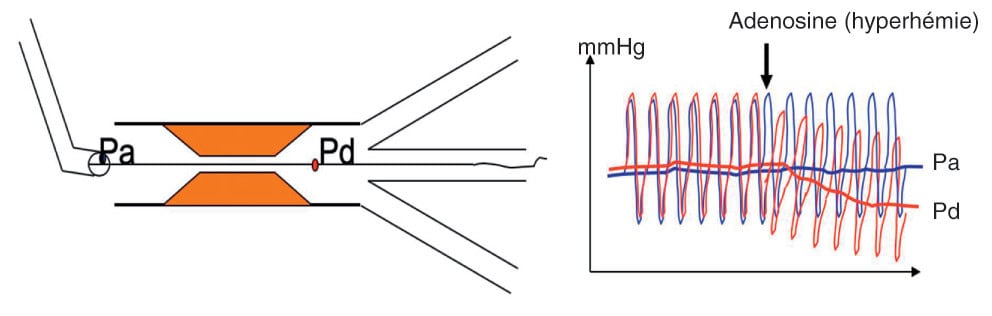
À gauche, schéma représentant une sonde de coronarographie de laquelle sort un guide de pression qui a été introduit dans la coronaire jusqu’en aval de la sténose (en orange). La pression d’amont Pa est recueillie par la sonde de coronarographie. La pression distale Pd est recueillie par le guide de pression. A droite représentation des courbes de pression Pa et Pd qui divergent en situation d’hyperhémie en raison du caractère hémodynamiquement significatif de la sténose coronaire.
________________________________________________________________________________
- L’imagerie endocoronaire s’est développée avec actuellement deux techniques utilisables en routine : l’échographie endocoronaire également appelée IVUS (intravascular ultrasound) au moyen d’une mini-sonde d’échographie placée dans la coronaire et la tomographie par cohérence optique ou OCT (optical coherence tomography) là encore au moyen d’une sonde d’imagerie intracoronaire basée sur les infras rouges. Ces deux techniques permettent d’apprécier avec des degrés différents de résolution spatiale l’extension des plaques d’athérosclérose dans la lumière artérielle et dans la paroi. Elles analysent aussi de façon plus précise les lésions de l’endothélium ainsi que le déploiement d’un stent après son insertion.
Biologie au cours des syndromes douloureux thoraciques
En cas d’angor, l’hémogramme sera attentivement examiné, une anémie pouvant aggraver voire provoquer la symptomatologie.
Même en cas d’angor d’effort sévère, les marqueurs de souffrance myocardique, notamment la troponine, (cf. infra) restent en général normaux (angor stable ou syndrome coronaire chronique).
Au cours de l’infarctus du myocarde, ces biomarqueurs sont libérés par les cardiomyocytes. Ils seront progressivement détectables dans le sang périphérique. À noter que ces marqueurs ne sont pas spécifiques de l’infarctus du myocarde aigu, puisqu’ils peuvent parfois être augmentés au cours d’autres affections cardiaques douloureuses avec nécrose moycytaire telles que la myocardite aiguë ou l’embolie pulmonaire grave avec retentissement cardiaque. Les marqueurs utilisés en biologie clinique pour confirmer le diagnostic de syndrome coronaire aigu sont des enzymes et des protéines présentes dans le plasma lorsqu’elles sont libérées par les cellules musculaires nécrosées. Ils confirment a posteriori le diagnostic. Les biomarqueurs usuels (tableau 3.5) sont les suivants :
- la troponine constitue un des éléments d’un complexe macromoléculaire en association à l’actine et la myosine, protéines contractiles constituant les myofibrilles présentes dans les cellules musculaires de tous les muscles striés. Elle est composée de trois sous-unités : C, I et T. Les isoformes spécifiques du tissu cardiaque (Tn Ic et Tn Tc) ont, lors d’une destruction du tissu cardiaque, une cinétique de libération lente dans le torrent circulatoire du fait de leur localisation intrafibrillaire et des processus enzymatiques mis en jeu pour désolidariser les différentes protéines contractiles. Le pic maximum de concentration dans le plasma n’est atteint qu’au bout d’environ 12 heures (en cas de SCA, les troponines commencent néanmoins à s’élever dès les premières heures) et persiste en plateau jusqu’à environ 24 heures, pour décroître ensuite lentement et revenir à la normale au bout de 3 à 6 jours. La cinétique des taux sériques (élévation puis normalisation) au cours des premiers jours est un élément diagnostic important. Il existe désormais des dosages de troponine ultrasensibles ou hypersensibles qui permettent un diagnostic plus précoce d’un épisode d’ischémie myocardique avec nécrose des cardiomyocytes ; leur dosage est recommandé devant toutes douleurs angineuses évoquant un SCA ;
- les isoenzymes MB (Myocardial Band) des créatines kinases (CK-MB) qui présentent une bonne spécificité et sensibilité mais ont été largement supplantés par les troponines.
Tableau 3.5. Informations utiles à la prescription et à l’utilisation des marqueurs de souffrance myocardique.
| Troponines ultra/hypersensibles | CK-MB | |
| Biologie | Protéine fibrillaire | Enzyme cytosolique |
| Début de détection | 2 à 4 heures | 3 à 7 heures |
| Pic | 12 à 24 heures | 10 à 24 heures |
| Retour à la normale | 5 à 10 jours | 3 à 5 jours |
| Avantages | C’est le marqueur le plus spécifique de nécrose | Bonne spécificité et sensibilité pour la nécrose |
| Inconvénients | Risque de faux positifs notamment chez l’insuffisant rénal | Détection plus tardive que la troponine |
| Seuil de positivité | > 0.014 μg/l pour la Tn Tc, variable en fonction du kit de dosage pour la Tn Ic | > 5 μg/l |
Le dosage sanguin des D-dimères fait partie de l’algorithme décisionnel en cas de suspicion de maladie veineuse thromboembolique avec une probabilité faible ou intermédiaire. Il s’agit d’un examen ayant une très faible spécificité, une élévation aspécifique du taux de D-Dimères pouvant être décrite dans de nombreuses situations cliniques. Il jouit cependant d’une excellente valeur prédictive négative ce qui permet le plus souvent d’écarter le diagnostic de maladie thromboembolique veineuse (thrombose veineuse profonde, embolie pulmonaire) si le taux reste normal au cours d’un syndrome douloureux thoracique.
Les examens biologiques standards sont systématiquement prescrits : hémogramme, plaquettes, ionogramme sanguin, urée et créatinine sanguine, bilan hépatique, bilan de coagulation en fonction de la clinique.
Pharmacologie et thérapeutiques de la maladie coronaire
Généralités
Les grands principes du traitement de la maladie coronaire stable sont les suivants :
- réduire l’ischémie myocardique, particulièrement lorsque les patients sont symptomatiques, grâce aux médicaments anti-angineux, et/ou à la revascularisation coronaire (pontages chirurgicaux et/ou angioplastie-stenting des coronaires) et à la réadaptation cardiaque ;
- prévenir et/ou ralentir la survenue des lésions athéromateuses des coronaires, en luttant contre les facteurs de risque : lutte contre le tabagisme et la sédentarité, traitements du diabète, de l’HTA et des dyslipidémies, notamment l’hyper LDL-cholestérolémie ;
- prévenir le risque de thrombose ou de récidive de thrombose coronaire, notamment grâce aux médicaments antiagrégants plaquettaires ;
De plus, la prise en charge des formes instables de la maladie coronaire nécessite de restaurer en urgence la perfusion coronaire en cas de thrombose aiguë (infarctus), grâce à la thrombolyse et/ou la reperfusion par angioplastie coronaire.
Enfin, dans le cas du développement d’une cardiopathie ischémique (c’est-à-dire un retentissement direct et séquellaire sur le myocarde de la maladie coronaire), il faudra prévenir et traiter les complications que sont les troubles du rythme cardiaque (cf. chapitre 6) et l’insuffisance cardiaque (cf. chapitre 5).
Anti-angineux
On regroupe sous ce terme les médicaments visant à restaurer ou à améliorer le déséquilibre entre apport et consommation en O2 du muscle cardiaque. Lorsque le patient présente une symptomatologie angineuse (angor d’effort), ces traitements ont un effet important sur la réduction des symptômes. Cependant, cette action est aussi utile lorsque le patient est asymptomatique et qu’il présente une ischémie myocardique sans angor (ischémie myocardique silencieuse) (tableau 3.6). Aucun de ces traitements n’a en revanche montré une amélioration du pronostic des patients en dehors de la situation du postinfarctus du myocarde et de l’insuffisance cardiaque compliquant la coronaropathie (pour les bêtabloquants notamment).
Tableau 3.6. Anti-angineux (disponibles en France et avec AMM dans l’indication).
| Familles | Principales molécules commercialisées | |
| Dérivés nitrés | Trinitrine, isosorbide dinitrate | |
| Médicaments apparentés aux dérivés nitrés | Molsidomine, nicorandil | |
| Bêtabloquants | Non sélectifs | Nadolol, pindolol, propranolol |
| Cardio-/β1-sélectifs | Acébutolol, aténolol, bétaxolol, bisoprolol, céliprolol, métoprolol | |
| Sélectifs avec effets vasculaires⁎ | Carvédilol, céliprolol, Nébivolol | |
| Inhibiteurs calciques | Dihydropyridines | Amlodipine, Félodipine, Nifédipine |
| Non dihydropyridiniques | Diltiazem, vérapamil | |
| Autres anti-angineux | Bradycardisants purs | Ivabradine |
| Modulateurs métaboliques | Trimétazidine | |
⁎ Carvedilol : α1-antagonistes, Celiprolol et Nébivolol : β2 agonistes.
Dérivés nitrés
Les dérivés nitrés sont des prodrogues sources de monoxyde d’azote (NO). Leur action est donc liée à leur capacité à former du radical libre NO. On les appelle ainsi des « donneurs de NO ». Le mécanisme actuellement reconnu comme prédominant et responsable de la libération du NO fait intervenir la glutathion-S-réductase (particulièrement présente dans les parois vasculaires, notamment veineuses).
Le NO, ainsi libéré, active la guanylate cyclase soluble, augmentant les concentrations intracellulaires de GMPc. Dans les cellules musculaires lisses, ceci induit la déphosphorylation des chaînes légères de la myosine et diminue la concentration intracellulaire en calcium, entraînant une relaxation des fibres musculaires lisses veineuses et artérielles à l’origine des effets favorables et secondaires de ces médicaments.
La vasodilatation veineuse diminue le retour veineux et donc la précharge cardiaque, ce qui réduit la consommation en O2 du myocarde.
La vasodilatation artérielle coronaire est rapide au niveau des gros troncs coronaires épicardiques et des artérioles intra-myocardiques. Il s’agit d’un traitement de choix pour lutter contre les symptômes angineux.
De plus, les nitrés s’opposent aux spasmes vasculaires et améliorent la perfusion sous-endocardique. Les dérivés nitrés sont à un moindre degré des vasodilatateurs artériels systémiques.
La vasodilatation systémique entraîne fréquemment l’apparition de céphalées et de flush de la face (qui s’améliorent en général avec la prolongation de l’utilisation) et parfois, à doses plus élevées, des chutes tensionnelles avec tachycardie réflexe non souhaitées.
Prescription (tableau 3.7)
Les dérivés nitrés sont soumis à un métabolisme hépatique important et à un effet de premier passage hépatique limitant fortement leur action lorsqu’ils sont administrés par voie orale. Pour éviter cet effet de premier passage, on recourt le plus souvent à des voies d’administration sublinguales (sprays), percutanée (patch) et intraveineuse (utilisation en urgence). Les formes orales utilisent des formes galéniques retard.
Tableau 3.7. Dérivés nitrés et apparentés : médicaments existants, formes galéniques et utilisation.
| D’action immédiate | D’action prolongée | |
| Dérivés nitrés | ||
| Trinitrine | Solution pour pulvérisation buccale de 0,15 et 0,30 mg/dose
Solution pour perfusion IV à 1 mg/ml |
Dispositif transdermique : 5, 10 et 15 mg/24 heures |
| Isosorbide dinitrate | Solution pour pulvérisation buccale de 1,25 mg/dose
Solution pour perfusion IV et intracoronaire de 10 mg/10 ml Gélules à libération immédiate de 20 mg |
|
| Apparentés | ||
| Molsidomine | Comprimés de 2 et 4 mg | |
| Nicorandil | Comprimés de 10 et 20 mg | |
De plus, l’utilisation continue de dérivés nitrés expose à un phénomène de tolérance et d’échappement thérapeutique. On utilise donc un intervalle libre quotidien plutôt dans la période où le patient ne présente pas de symptômes angineux (classiquement pendant le sommeil).
Indications
Lors de la crise d’angor, le médicament à utiliser d’urgence (que le malade doit avoir dans sa poche) est la trinitrine administrée par voie sublinguale (spray ou comprimé à croquer). Le patient doit être formé à son utilisation.
Au cours de la maladie angineuse, ils sont fréquemment utilisés sous forme « retard » en patchs cutanés (à la dose de 5 à 15 mg par jour) placé environ 12 heures sur 24 (surtout le jour) sur la peau en appoint des autres thérapeutiques.
La forme injectable n’est utilisée que dans les unités de soins intensifs, les réanimations et par les équipes du SAMU, notamment dans les syndromes coronaires aigus et au cours des cardiopathies évolutives avec signes d’insuffisance cardiaque gauche (voir chapitre 5).
Interactions importantes à connaitre
Les dérivés nitrés ne doivent jamais être utilisés en association avec des inhibiteurs PDE5 (traitements de la dysfonction érectile comprenant sildénafil (Viagra®), tadalafil (Cialis®), vardénafil (Levitra®)). Il existe en effet un risque nettement accru de potentialisation des effets vasodilatateurs et d’hypotension artérielle sévère.
Bêtabloquants
Ces médicaments sont des antagonistes des récepteurs β-adrénergiques soit de manière non sélective (antagonisme des récepteurs β1 et β2), soit cardiosélectifs car spécifiques des récepteurs β1 (seulement retrouvés au niveau du muscle cardiaque). Les bêtabloquants ont des propriétés qui leur donnent des indications dans différentes pathologies cardiaques : HTA, troubles du rythme, insuffisance cardiaque chronique à fraction d’éjection réduite, cardiomyopathie hypertrophique et chez les patients atteints de cardiopathies ischémiques. Seul ce dernier aspect est abordé dans ce paragraphe.
Ils entraînent sur le plan cardiaque une diminution de la contractilité cardiaque (effet inotrope négatif), un ralentissement de la fréquence cardiaque et de ses accélérations (effet chronotrope négatif), un allongement du temps de conduction atrioventriculaire (effet bathmotrope négatif). Ils agissent aussi au niveau rénal en diminuant la synthèse de rénine et d’angiotensine II circulante. Ces effets conduisent à diminuer la consommation myocardique en O2, notamment lors des efforts, et justifient l’utilisation des bêtabloquants en première intention comme traitement prophylactique de l’angor et des accidents évolutifs post-infarctus du myocarde.
Les bêtabloquants (cf. tableau 3.6) peuvent être ou non β1-adrénergiques sélectifs (effets essentiellement cardiaques et rénaux), avoir une activité sympathomimétique intrinsèque (discrète stimulation β-adrénergique mais en bloquant l’effet des catécholamines), avoir une activité agoniste α1-adrénergique ou β2-adrénergique (effets vasculaires vasodilatateurs associés). Ainsi, les bêtabloquants cardiosélectifs sont plus bradycardisants et baissent indirectement la pression artérielle (en diminuant le débit cardiaque), alors que les bêtabloquants avec effets vasculaires sont moins bradycardisants mais ont un effet vasodilatateur direct (utile chez un patient ayant une hypertension artérielle associée par exemple). Certaines molécules ont un effet anti-arythmique plus prononcé.
Indications
Dans la cardiopathie ischémique, notamment au cours de l’angor, ils sont prescrits (sauf contre-indications) en première intention (parmi les anti-angineux), progressivement en se guidant sur les chiffres de fréquence cardiaque, que l’on souhaite réduire à 60 battements par minute au repos environ en l’absence d’effets secondaires.
Certains bêtabloquants sont plus particulièrement indiqués en cas d’altération associée de la fonction systolique du ventricule gauche (FEVG < 40 %) car ils ont montré une diminution de la morbi mortalité chez ces patients (metoprolol, bisoprolol, carvedilol et nebivolol).
Il est possible de les associer aux dérivés nitrés et aux inhibiteurs calciques non bradycardisants (autrement dit de type dihydropyridines).
Contre-indications
Les principales contre-indications sont les bradycardies et blocs atrioventriculaires de haut grade non appareillés, l’hypotension artérielle sévère, l’insuffisance cardiaque décompensée, le choc cardiogénique, les bronchopathies chroniques ou les asthmes sévères (compte tenu de l’effet bronchoconstricteur de l’antagonisme des récepteurs bronchiques β2-adrénergiques). Les bêtabloquants peuvent aussi aggraver un syndrome de Raynaud et le psoriasis.
Inhibiteurs calciques
Les médicaments antagonistes des canaux calciques ont tous en commun de bloquer les canaux calciques lents voltage-dépendents des cellules musculaires. On peut cependant les regrouper en deux grandes classes selon leur structure chimique et leur point d’impact :
- les dihydopyridines inhibent préférentiellement les canaux calciques localisés au niveau des muscles lisses mais pas au niveau du muscle cardiaque. Leurs effets en cardiologie sont donc essentiellement vasculaires. Sur le plan coronaire, ils entraînent une dilatation artérielle coronaire et s’opposent au spasme coronaire. L’effet antihypertenseur est bien sûr un appoint puisqu’il réduit le travail cardiaque. Il existe de nombreuses molécules de la famille des dihydropyridines développés pour le traitement de l’HTA, mais seules 3 d’entre elles peuvent être utilisés pour le traitement symptomatique de l’angor. N’ayant pas d’effets cardiaques directs, les dihydropyridines peuvent être associés aux bêtabloquants pour renforcer l’effet anti-angineux ;
- le diltiazem et le vérapamil sont des antagonistes calciques n’appartenant pas à la famille des dihydropyridines et dont l’action est non sélective, au niveau cardiaque et vasculaire. Ils entraînent ainsi une vasodilatation artérielle moindre que les dihydropyridines, mais ils ont des effets cardiaques directs inotropes négatifs et bradycardisants, similaires aux bêtabloquants auxquels ils ne doivent donc pas être associés.
Prescription
Le choix de l’une ou l’autre classe d’inhibiteur calcique est réalisé en tenant compte de leurs effets cardiovasculaires globaux.
Indications
Le diltiazem et le vérapamil ont une indication de première intention au choix avec les bêtabloquants pour le traitement symptomatique des patients avec coronaropathie (mais les bêtabloquants seront privilégiés dans la situation du post-infarctus du myocarde et de l’insuffisance cardiaque). Le diltiazem et le vérapamil peuvent être choisis lorsque le rythme cardiaque est rapide, qu’il existe une contre-indication aux bêtabloquants, ou en présence de troubles du rythme supraventriculaires sur lesquels ils sont assez efficaces. Ces médicaments sont à éviter en cas de troubles de conduction de haut grade non appareillés ou d’insuffisance cardiaque par dysfonction systolique ventriculaire gauche avec baisse marquée de la FEVG.
On préféra les dihydropyridines chez les patients hypertendus, éventuellement en association à un bêtabloquant. Ils sont aussi un traitement de choix en cas d’angor spastique.
Effets indésirables
Tous les inhibiteurs calciques peuvent provoquer des œdèmes des membres inférieurs qui alarment le patient, mais sont en général faciles à traiter en réduisant la posologie et en ajoutant éventuellement un diurétique. Les dihydropyridines peuvent être responsables de bouffées vasomotrices en début de traitement. Le diltiazem et le vérapamil peuvent provoquer des troubles conductifs de haut degré et ne doivent pas être utilisés en cas d’insuffisance cardiaque à fraction d’éjection réduite (FEVG < 40 %).
Autres anti-ischémiques
Les médicaments suivants sont généralement utilisés en seconde intention pour le traitement des patients avec coronaropathie et symptomatique (angor résiduel).
Molsidomine
La molsidomine est un donneur de NO, apparenté aux dérivés nitrés. Elle entraîne une relaxation vasculaire, notamment des coronaires. Comme les nitrés, il ne doit pas être utilisé en même temps que les inhibiteurs PDE5 (cf. supra). Ils peuvent induire des céphalées.
Nicorandil
Ce médicament est un vasodilatateur artériel et veineux. Son mécanisme d’action est double. Il augmente le taux de GMPc intracellulaire du fait de la présence d’un radical nitré dans sa structure. Par ailleurs, c’est un activateur des canaux KATP, entraînant une hyperpolarisation des cellules musculaires lisses vasculaires, la fermeture des canaux calciques dépendants du voltage et une vasorelaxation. Comme les nitrés, il peut induire des céphalées.
D’autres classes d’anti-angineux existent mais n’ayant pas d’indications reconnues en France elles ne seront pas détaillées dans ce chapitre (ivabradine, trimetazidine et ranolazine)
Antiagrégants, anticoagulants, thrombolytiques
Antiagrégants plaquettaires
Les antiagrégants plaquettaires sont très utilisés en cardiologie. Ces médicaments ont tous à ce jour pour cible les plaquettes (antiplaquettaires), effecteurs essentiels de la phase primaire de la coagulation (tableau 3.8) (voir chapitre 1).
Tableau 3.8. Étapes de la thrombose et armes thérapeutiques.
| Étapes | Cible | Traitements possibles |
| Hémostase primaire | Plaquettes | Antiagrégants plaquettaires |
| Coagulation | Thrombine | Héparines
Antivitamine K Antithrombine directs⁎ |
| Fibrinolyse | Caillot constitué | Thrombolytiques |
⁎ Les anti-Xa sont une autre cible pour le traitement anticoagulant oral.
Cette classe thérapeutique a montré un bénéfice clinique sur la morbi-mortalité des patients coronariens.
Aspirine
L’aspirine est le plus ancien des antiagrégants plaquettaires.
Médicaments
Kardégic® (poudre), Aspegic® (poudre), Resitune® et Aspirine Protect® (comprimé).
Mode d’action
L’aspirine agit en inhibant de manière irréversible la cyclo-oxygénase (la COX-1 et à un moindre niveau la COX-2). Elle diminue ainsi la production de thromboxane A2 (TXA2), un médiateur plaquettaire qui a un effet pro-agrégant. Le TXA2 active les autres plaquettes circulantes. L’effet de l’aspirine sur la plaquette inhibée par l’aspirine est irréversible mais cette même plaquette (qui ne peut donc plus produire elle-même du TXA2), peut être activée par du TXA2 produit par une autre plaquette voisine non inhibée par l’aspirine. La disparition de l’effet nécessite donc d’attendre le remplacement de la majorité des plaquettes (généralement 7 jours).
Posologie
L’aspirine a de nombreux effets pharmacologiques qui dépendent des posologies utilisées. Les doses nécessaires pour obtenir l’effet antiagrégant sont faibles (dès 75 mg/j et < 500 mg/j) alors que les effets anti-inflammatoires ou antipyrétiques sont obtenus à des posologies supérieures. La bonne dose d’aspirine chez le patient coronarien stable est donc de 75-160 mg par jour. L’aspirine est rapidement active per os (10 minutes) mais peut aussi s’administrer par voie intraveineuse.
L’aspirine est de plus en plus souvent associée à d’autres traitements très fréquemment prescrits chez le patient coronarien (autre antiagrégant plaquettaire parfois anticoagulants notamment à la phase initiale du syndrome coronaire aigu).
Indications
En l’absence de contre-indications, tout coronarien doit recevoir de l’aspirine à dose antiagrégante plaquettaire et le traitement est prescrit à vie (amélioration du pronostic cardiovasculaire).
Les autres indications de l’aspirine dans la maladie athéroscléreuse sont la prévention secondaire de chez les patients porteurs d’une artériopathie des membres inférieurs (AOMI), et/ou ayant présenté un AVC ischémique ne relevant pas d’un traitement par les anticoagulants oraux (AVC compliquant une fibrillation atriale ou une embolie paradoxale).
Effets indésirables essentiels
Les effets indésirables essentiels sont représentés par l’augmentation du risque de saignements et la survenue d’ulcères gastriques secondaires à l’inhibition de la cyclo-oxygénase au niveau de la muqueuse gastrique. Il ne s’agit donc pas d’une toxicité de contact, mais pharmacodynamique et qui existe dès la plus faible dose. Il faut souvent associer une protection gastrique (inhibiteur de la pompe à proton) dans les situations à risque pour prévenir ce risque, et surveiller régulièrement la possibilité d’un saignement digestif occulte ou une symptomatologie ulcéreuse.
Des allergies vraies peuvent exister. Leur suspicion est beaucoup plus fréquente que les formes avérées. Le syndrome de Widal associe asthme, polypose nasale et allergie à l’aspirine.
L’aspirine doit être évitée chez les femmes enceintes de plus de 6 mois compte tenu du risque de fermeture prématurée du canal artériel chez le fœtus.
Thiénopyridines et ticagrelor
Médicaments
Clopidogrel (Plavix®), prasugrel (Efient®), ticagrelor (Brilique®), cangrelor (Kengrexal®).
Mode d’action
Il s’agit d’une classe d’antiagrégants plaquettaires qui agit en bloquant la voie de l’ADP par blocage de son récepteur plaquettaire dénommé P2Y12. L’ADP est relarguée par les premières plaquettes ayant adhéré à la lésion et agit comme un activateur des plaquettes environnantes. Il joue aussi un rôle direct dans l’externalisation du récepteur plaquettaire GPIIb/IIIa qui joue un rôle majeur dans l’agrégation des plaquettes entre elles et la constitution du thrombus plaquettaire.
Les effets des médicaments de cette classe sont additifs à ceux de l’aspirine et ils peuvent donc être associés à l’aspirine. Ils ont permis d’incontestables progrès dans les situations à haut risque de thrombose, en particulier coronaire, notamment lors de la phase initiale du syndrome coronaire aigu.
Le clopidogrel a été longtemps le chef de file de cette classe. Il s’agit d’une prodrogue. C’est son métabolite qui est le médicament actif. Ce métabolisme passe par la voie du cytochrome P450, en particulier par le CYP2C19. Chez 2 à 3 % des patients de type caucasiens, le CYP2C19 est déficient et le métabolisme du clopidogrel se fait mal, le médicament n’est ainsi pas ou trop peu actif. Le clopidogrel est utilisé en traitement chronique à la dose de 75 mg par jour mais l’inhibition rapide de l’agrégation plaquettaire peut nécessiter de fortes doses (jusqu’à 900 mg lors d’une dose de charge initiale). Son action est irréversible.
Le prasugrel est aussi un inhibiteur du récepteur P2Y12 de la même famille que le clopidogrel. Comme le clopidogrel, son action est irréversible.
Le ticagrelor fait partie d’une famille voisine (cyclo-pentyl-triazolo-pyrimidines) mais agit aussi comme un antagoniste sélectif du récepteur P2Y12 de l’ADP. Il ne nécessite cependant pas de métabolisation pour être actif. Son effet est réversible.
Prasugrel et ticagrelor ont un effet antiplaquettaire plus puissant et plus rapide que le clopidogrel. En raison d’une supériorité clinique démontrée dans les essais thérapeutiques, ils sont préférés dans le traitement des syndromes coronaires aigus.
Le cangrelor est un inhibiteur compétitif réversible de P2Y12, utilisable par voie intraveineuse uniquement, dont la demi-vie est très courte (3-5 minutes). Il est réservé à des situations particulières d’angioplastie coronaire à la phase aiguë d’un SCA lorsque qu’il n’a pas été possible d’administrer une dose de charge d’inhibiteur de P2Y12 per os (patient intubé ou ayant vomi)
Posologie (tableau 3.9)
Le clopidogrel est donné à une dose de charge de 300 à 900 mg puis, le plus souvent, à des posologies quotidiennes de 75 mg en une prise par jour (cp. à 300 et à 75 mg).
Tableau 3.9. Thiénopyridines et ticagrelor : posologies.
| Médicament | Dose de charge | Dose d’entretien | Nombre de prise(s) par jour |
| Clopidogrel | 300–900 mg | 75 mg | 1 |
| Prasugrel | 60 mg | 10 mg | 1 |
| Ticagrelor | 180 mg | 90 mg × 2 | 2 |
Le prasugrel est donné à une dose de charge à 60 mg par jour puis à 10 mg par jour en une prise par jour (cp. à 10 mg).
Le ticagrelor est prescrit à 180 mg en dose de charge puis 90 mg par jour deux fois par jour.
Indications
Les indications de chacun de ces antiagrégants plaquettaires sont inhérentes aux études cliniques qui ont été conduites et qui ont pu montrer un intérêt dans telle ou telle pathologie. Toutes ces molécules ne sont pas « interchangeables ». Ces indications sont évolutives avec l’arrivée de nouvelles études qui sont en cours :
- le ticagrelor est indiqué à la phase aiguë d’un SCA en association avec l’aspirine puis pendant une durée de 12 mois ou plus au décours ;
- le prasugrel est indiqué à la phase aiguë d’un SCA qui doit être traité par angioplastie en association avec l’aspirine, puis pendant une durée de 12 mois au décours ;
- le clopidogrel est indiqué à la phase aiguë d’un SCA et après angioplastie coronaire dans un contexte stable en association avec l’aspirine, pour une durée de 3 à 12 mois. Il peut aussi remplacer l’aspirine en monothérapie lorsque cette dernière est mal tolérée ou contre-indiquée.
Surveillance
Il n’existe pas de test biologique fiable utilisable en routine pour surveiller l’efficacité des thiénopyridines ou du ticagrelor.
Contre-indications absolues
Tous ces traitements augmentent le risque hémorragique et sont donc contre-indiqués en cas de saignement majeur en cours. Le prasugrel comporte un risque hémorragique cérébrale qui le contre-indique chez les sujets ayant des antécédents d’accident cérébral (hémorragique ou ischémique).
Contre-indications relatives
Les sujets de moins de 60 kg et ceux de plus de 75 ans étant les plus susceptibles de saigner, ils constituent une contre-indication relative au prasugrel.
L’effet adénosine-like du ticagrelor par lequel le médicament est actif peut être responsable de dyspnée gênante et de rares bradycardies.
Anti-GpIIb/IIIa
Médicaments
Abciximab (Reopro®), eptifibatide (Integrilin®), tirofiban (Agrastat®).
Mode d’action
La glycoprotéine IIb/IIIa est un récepteur de la plaquette qui permet son adhésion au fibrinogène (constituant une des phases essentielles de l’agrégation plaquettaire puis de l’élaboration du thrombus). Les anti-GpIIb/IIIa bloquent ce récepteur (fig. 3.31).
________________________________________________________________________________
Figure 3.31. Les récepteurs de la plaquette et les actions thérapeutiques possibles.
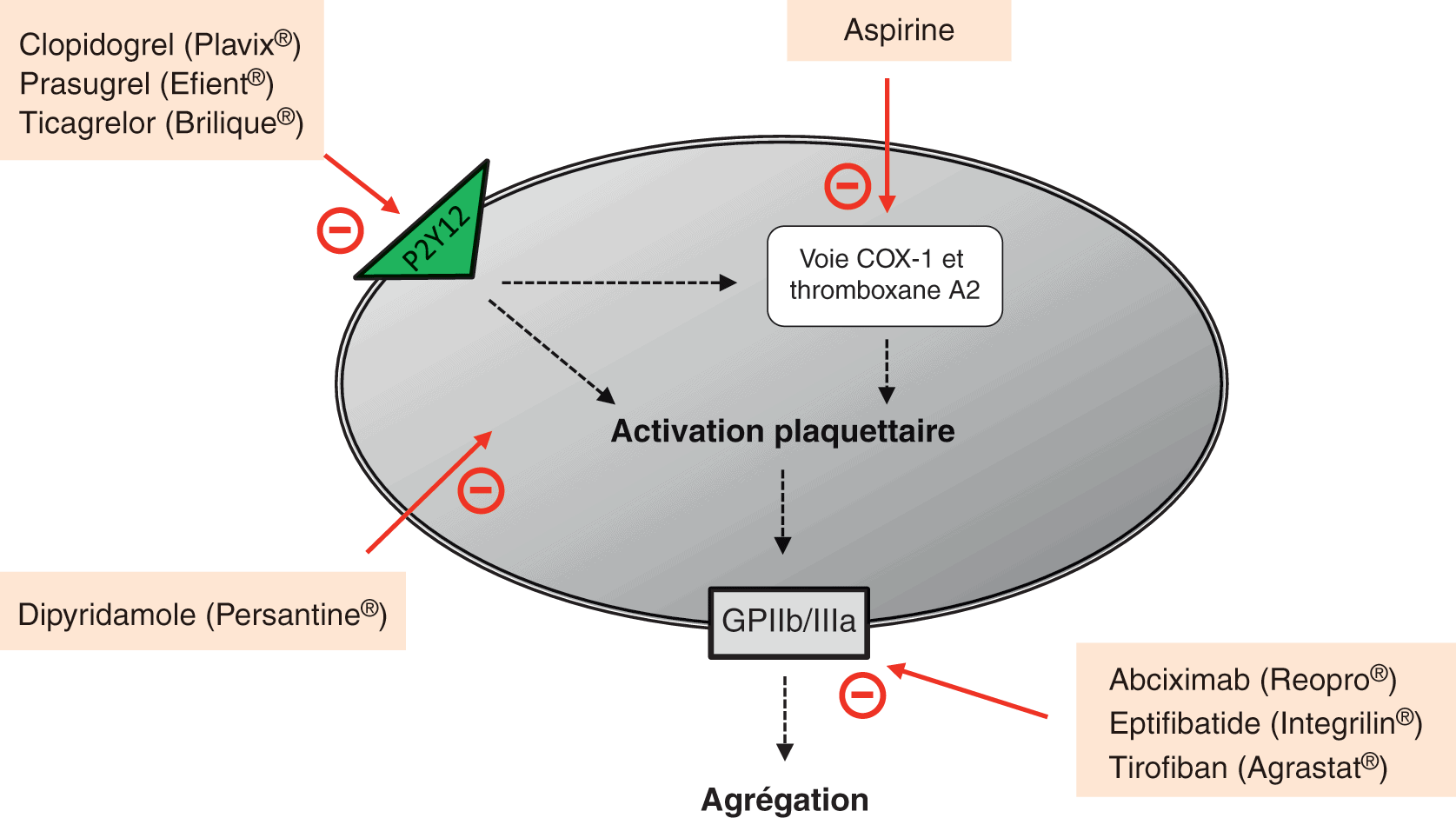
________________________________________________________________________________
Indications
Ces traitements efficaces ne sont utilisés que par voie veineuse sur de très courtes périodes. Ils sont réservés à des conditions très particulières, notamment en salle d’angioplastie lors des dilatations coronaires à haut risque de thrombose. Ils sont de moins en moins utilisés depuis l’avènement des nouveaux inhibiteurs du récepteur P2Y12 (prasugrel, ticagrelor, cangrelor).
Effets indésirables
Le risque hémorragique est important. L’abciximab est responsable de thrombopénies. Leur coût est élevé.
Dipyridamole
C’est un antiagrégant plaquettaire peu puissant, peu ou plus utilisé en cardiologie. Il inhibe la captation d’adénosine avec, paradoxalement, des effets « adénosine » qui seraient dus à une sensibilité accrue à l’adénosine endogène.
Dans sa forme injectable, il peut être utile pour sensibiliser la recherche d’ischémie myocardique au cours de certaines scintigraphies myocardiques.
Anticoagulants
Les anticoagulants ont, dans la coronaropathie et à ce jour, une indication uniquement lors de la phase initiale (72 premières heures) d’un syndrome coronaire aigu (SCA) en dehors des indications reconnues de ces traitements (fibrillation atriale, valve cardiaque prothétique mécanique, thrombose veineuse…).
Seuls l’héparine non fractionnée (HNF), les héparines de bas poids moléculaires (HBPM), le fondaparinux et la bivalirudine (cette dernière n’est plus disponible en France et ne sera donc pas abordée) ont une indication retenue.
Les antivitamines K et les anticoagulants oraux directs n’ont à ce jour aucune indication en coronaropathie en France que ce soit à la phase aiguë ou chronique. Il est toutefois possible de voir cela évoluer dans les prochaines années à la suite des résultats des études sur la dose très faible de rivaroxaban 2,5 mg deux fois par jour. Les autres anticoagulants oraux directs n’ont pas à ce jour d’étude dans ce contexte. En l’absence d’indication en France, à ce jour, ces traitements ne seront donc pas abordés dans ce paragraphe.
Héparines
Médicaments (tableau 3.10)
On distingue :
- l’héparine standard non fractionnée (HNF) : héparine intraveineuse et Calciparine® (voie sous-cutanée) ;
- les héparines de bas poids moléculaires (HBPM) : enoxaparine (Lovenox®), tinzaparine (Innohep®), nadroparine (Fraxiparine®), daltéparine (Fragmine®), qui correspondent à une fraction plus courte de la chaîne d’héparine, administrées soit en intraveineux soit en sous-cutanée ;
- des héparinoïdes comme le fondaparinux (Arixtra®), voie sous cutanée uniquement.
Tableau 3.10. Caractéristiques des héparines.
| Héparine | Action par anti-thrombine | Élimination par le rein | Demi-vie | Antidote |
| HNF | Oui | + | 1 h 30 | Oui (sulfate de protamine) |
| HBPM | Oui | +++ | 8 à 24 heures | Sulfate de protamine, mais peu efficace |
| Fondaparinux | Non | +++ | 17 à 21 heures | Non |
Mode d’action
L’HNF et les HBPM agissent en activant un anticoagulant physiologique présent dans le sang qui est l’anti-thrombine. Le fondaparinux est un anti-Xa synthétique qui mime la fraction anti-thrombine des héparines.
Après injection intraveineuse, l’effet anticoagulant de l’HNF est immédiat. La demi-vie de l’HNF est courte de l’ordre d’une heure à une heure et demie. Le maintien de l’activité anticoagulante désirée est donc obtenu en perfusant l’HNF en continu (seringue auto-pousseuse) après parfois l’utilisation d’un bolus pour obtenir un effet plus rapide.
Les HBPM qui ont une demi-vie plus longue se font en injections sous-cutanées une ou deux fois par jour en fonction de leur demi-vie. Attention, la phase initiale du syndrome coronaire aigu est la seule indication ou un bolus intraveineux d’enoxaparine peut être utilisé suivi d’un traitement sous-cutané pendant deux à trois jours.
Le fondaparinux qui a une demi-vie longue s’administre en sous-cutanée une seule fois par jour.
L’HNF est éliminée en grande partie par une fixation sur les protéines, les cellules endothéliales et les macrophages et, pour une petite partie, par le rein, tandis que les HBPM et le fondaparinux sont essentiellement éliminés par le rein, ce qui peut poser des risques de surdosage et d’accumulation chez les patients avec insuffisance rénale sévère (DFG < 30 ml/min).
Pour l’héparine standard, il existe un antidote qui est le sulfate de protamine qui doit être administré par voie intraveineuse. Il neutralise instantanément l’action de l’héparine non fractionnée. Ce même antidote est utilisable mais moins efficace pour les HBPM.
Posologies
Les posologies curatives de l’héparine standard pour obtenir un effet anticoagulant rapide sont de l’ordre de 80 à 100 UI/kg (environ 50 UI/kg en bolus pour obtenir une hypocoagulation immédiate), puis de 18 UI/kg par heure (à la seringue auto-pulsée).
Les posologies curatives des HBPM sont fonction du poids du sujet (100 U anti-Xa/kg ; par exemple, 0,8 ml deux fois par jour pour l’enoxaparine pour un poids de corps de 80 kg), ceci implique d’obtenir le poids du malade avec la plus grande précision. Lorsqu’un bolus IV d’enoxaparine est utilisé à la phase initiale du SCA, la dose utilisée est de 0,5 ml/kg.
Indications
Les héparines sont des anticoagulants d’action rapide utilisés dans toutes situations où une anticoagulation urgente est nécessaire :
- traitements des thromboses veineuses profondes et de l’embolie pulmonaire ;
- troubles du rythme atrial (fibrillation atriale, flutter atrial) nécessitant un traitement anticoagulant, le plus souvent en attente de l’efficacité des anticoagulants oraux. Cependant, leurs indications se réduisent avec la diffusion des anticoagulants directs ;
- syndrome coronaire aigu, le plus souvent sur une période de quelques jours.
Les héparines sont également utilisées en prévention de la thrombose veineuse en contexte chirurgical ou médical à risque (les doses préventives sont alors utilisées non détaillées ici).
Surveillance
L’effet thérapeutique de l’HNF se mesure par le temps de céphaline activée (TCA) qui doit être deux à trois fois prolongé par rapport à celui du témoin et/ou par l’activité anti-Xa (entre 0,5 et 0,8/ml).
Sauf exception, l’activité thérapeutique des HBPM n’a pas besoin d’être mesurée dès lors qu’elle est prescrite de façon correcte en fonction du poids et en l’absence d’insuffisance rénale.
Il faut également surveiller la numération plaquettaire en raison du risque de thrombopénie induite à l’héparine.
Contre-indications
Les HBPM ainsi que le fondaparinux sont contre-indiqués lorsque la clairance de la créatinine est inférieure à 30 ml/min.
Effets indésirables de l’héparinothérapie
Le principal effet indésirable, corollaire de l’effet anticoagulant recherché, est le risque hémorragique.
Les thrombopénies sont une complication classique mais rare de l’héparinothérapie. Il en existe deux types, le premier par mécanisme toxique direct (dit type I) est rapide, peu profond, et bénin. Le second correspond à un phénomène immunoallergique (dit type II) et est particulièrement grave. Typiquement, les thrombopénies de type II surviennent vers le septième-dixième jour (lors de la première exposition au traitement). Elles correspondent paradoxalement à une situation hautement thrombogène avec des thromboses essentiellement veineuses (80 % des cas) mais aussi artérielles (20 % des cas), car le mécanisme fait intervenir des auto-anticorps tournés contre un complexe immunogène plaquette-héparine et induit un amas des plaquettes entre elles. Cette crainte des thrombopénies à l’héparine impose une surveillance régulière des plaquettes. Elle doit surtout être à l’origine chaque fois que possible de l’introduction rapide d’autres traitements anticoagulants lorsqu’un relais est nécessaire (AVK ou anticoagulants oraux directs).
Le risque de thrombopénie semble plus limité avec le fondaparinux.
Une ostéoporose, une alopécie, une élévation des transaminases ainsi qu’un priapisme sont des complications possibles des héparines.
Thrombolytiques
Les traitements thrombolytiques sont des antithrombotiques puissants qui n’appartiennent ni à la classe des antiagrégants plaquettaires ni à la classe des anticoagulants. Leur indication est limitée à la phase initiale du syndrome coronaire aigu avec sus-décalage du segment ST, de l’accident vasculaire cérébral ischémique, ou de l’embolie pulmonaire grave. Ils ne sont utilisables que par voie veineuse.
Médicaments
Altéplase (Actilyse®), tenectéplase (Métalyse®), urokinase (Actosolv®).
Mode d’action
Les thrombolytiques sont des médicaments administrés par voie intraveineuse qui ont pour objectif de lyser les caillots déjà constitués. Ce sont des activateurs de la fibrinolyse physiologique, en particulier du plasminogène.
Indications
- Infarctus du myocarde (avec sus-décalage du segment ST uniquement (STEMI) datant de moins de 6 à 12 heures lorsqu’il n’y a pas de possibilité d’angioplastie primaire dans un délai suffisamment cours (produit utilisé essentiellement en France par les Samu en pré-hospitalier).
- Accident ischémique cérébral (AIC) vu dans les quatre premières heures, après exclusion d’une cause hémorragique.
- Embolie pulmonaire à haut risque compliquée de choc.
Effets indésirables et contre-indications
Leur efficacité s’accompagne d’un risque hémorragique important qui doit faire peser leur indication. Le risque d’hémorragie intracérébrale est de l’ordre de 0,7 à 1 %.
La liste des contre-indications comporte toutes les situations à risque hémorragique : certains accidents ischémiques cérébraux, hémorragie récente, chirurgie récente, ulcère digestif évolutif, diathèse hémorragique, etc.
Stratégies thérapeutiques proposées chez les patients porteurs de maladie coronaire
Maladie coronaire stable
La maladie coronaire stable se définit par la présence d’une maladie coronaire authentifiée en l’absence ou à distance (1 an) d’un syndrome coronaire aigu, d’une angioplastie coronaire ou d’une revascularisation par pontage coronaire. Les patients porteurs d’une maladie coronaire stable ont un excellent pronostic s’ils reçoivent un traitement adapté associé à une surveillance régulière par un cardiologue.
Le traitement repose sur :
- une prise en charge des facteurs de risque cardiovasculaire (cf. supra)
- la prescription de médicaments visant à prévenir les symptômes et les accidents cardiovasculaires aigus
- la formation du patient à la conduite à tenir en cas de crise angineuse (récidive ou apparition de douleur thoracique)
- la revascularisation myocardique dans certains cas
L’ordonnance de l’angineux stable doit comporter au minimum (BASIC) :
- un bêtabloquant si antécédent d’infarctus du myocarde et/ou en cas de dysfonction ventriculaire gauche (FEVG < 40 %) ;
- un anti-agrégant plaquettaire : aspirine en première intention, clopidogrel si intolérance à l’aspirine ;
- des hypolipémiants en prévention secondaire : statine à forte dose +/− ezetimibe +/− anti PCSK9 (objectif de baisse de 50 % du LDL-c avec concentration cible < 0,55 g/L) ;
- un inhibiteur de l’enzyme de conversion de l’angiotensine si la fraction d’éjection ventriculaire gauche est altérée (FEVG < 40 %) et/ou en cas de diabète et/ou en cas HTA ;
- un dérivé nitré d’action rapide sublinguale en cas de crise angineuse.
Quand proposer une revascularisation coronaire au patient coronarien stable ?
Il est recommandé de proposer une revascularisation dans trois situations :
- en cas de non-contrôle des symptômes angineux d’effort par le traitement médicamenteux anti-angineux bien conduit (patient symptomatique sous traitement) ;
- en cas de lésions coronaires sévères : sténoses multitronculaires (incluant les sténoses du tronc commun gauche ou de IVA proximale) ;
- en cas d’altération de la fonction ventriculaire gauche susceptible de s’améliorer après revascularisation. Des études récentes (ISCHEMIA) ont remis en cause le dogme de la revascularisation coronaire systématique en cas d’ischémie myocardique documentée (pas de réduction des événements cardiovasculaires)
Quel type de revascularisation proposer ?
Selon la sévérité des lésions (nombre, localisations) et le niveau de risque du patient (présence d’un diabète) on proposera une revascularisation par angioplastie per cutanée (avec mise en place de stents) ou par chirurgie (pontages).
________________________________________________________________________________
Attention : En cas de revascularisation par angioplastie dans ce contexte stable et en dehors du SCA, une double anti-agrégation plaquettaire associant aspirine et clopidogrel est nécessaire pendant un à six mois. Ensuite une mono anti-agrégation plaquettaire par aspirine est recommandée actuellement. Parfois, la durée de la double anti-agrégation plaquettaires est prolongée au-delà de 6 mois.
________________________________________________________________________________
Syndromes coronaires aigus (SCA)
Dans le cadre des syndromes coronaires aigus, l’urgence est de mettre en route les moyens thérapeutiques qui réduisent le risque de décès et la taille de l’infarctus du myocarde (et donc ses conséquences). La stratégie thérapeutique combine l’administration de médicaments antithrombotiques et une revascularisation coronaire de la lésion coupable du SCA. Le risque de décès notamment par troubles du rythme ventriculaire nécessite une surveillance scopée du patient à la phase initiale et la présence d’un défibrillateur cardiaque externe à proximité dès le diagnostic suspecté.
On distingue la prise en charge des infarctus du myocarde (IDM) avec sus décalage du segment ST de celle des autres syndromes coronaires aigus.
Prise en charge du SCA avec sus décalage du segment ST
Aussitôt le diagnostic posé (cf. « Sémiologie ») une prise en charge médicalisée pré hospitalière est indiquée avec recours à une équipe mobile médicale (Smur) qui dirigera le patient vers une unité de soins intensifs cardiaque (USIC) équipé d’une salle de coronarographie. L’objectif est de rouvrir l’artère coronaire occluse le plus rapidement possible (reperfusion myocardique en extrême urgence). La stratégie de revascularisation prioritaire est l’angioplastie coronaire percutanée primaire en salle de coronarographie. Pendant l’acheminement du patient vers la salle de coronarographie un traitement antithrombotique est débuté associant :
- aspirine 250 mg IV ou per os ;
- ticagrelor 180 mg per os, ou prasugrel 60 mg per os (ou clopidogrel 600 mg per os) ;
- héparine non fractionnée 80-100 UI/kg en bolus IV (ou enoxaparine 0,5 ml/kg IV) ;
- traitement de la douleur par titration de morphine IV si nécessaire.
Dans certains cas, une revascularisation pharmacologique peut être tentée par thrombolyse intraveineuse (cf. paragraphe pharmacologie), débutée pendant le transport vers l’USIC (IDM pris en charge précocement dans les deux heures suivant le début de la douleur chez des sujets jeunes à faible risque hémorragique et pour lesquels le délai d’acheminement vers la salle de coronarographie sera supérieur à deux heures et donc trop long). En cas de thrombolyse, le traitement antithrombotique associe aspirine 250 mg, clopidogrel 300 mg et héparine 60 UI/kg avec relais au pousse-seringue électrique. Une coronarographie sera systématiquement réalisée dans les heures qui suivent l’admission en USIC.
Le patient sera surveillé trois à cinq jours en USIC selon la gravité de son IDM initial et de son évolution. Le traitement du post IDM sera introduit dans les 24 heures qui suivent son admission associant :
- une bithérapie antiagrégante plaquettaire : aspirine 75 mg/j + ticagrelor 90 mg x 2/j ou prasugrel 10 mg/j (ou clopidogrel 75 mg/j) poursuivie idéalement 12 mois en l’absence de saignement ou de hauts risque hémorragique (et au-delà dans certaines situations à risque accru de thrombose) ;
- un traitement hypolipémiant intensif en prévention secondaire associant statine à forte dose + /− ézétimibe +/− anti PCSK9 avec un objectif de diminution de 50 % du LDL-c et une concentration cible < 0,55 g/L ;
- un inhibiteur de l’enzyme de conversion de l’angiotensine ;
- un bêtabloquant ;
- un dérivé nitré d’action rapide sublinguale en cas de crise angineuse.
D’autres classes pharmacologiques et interventions thérapeutiques peuvent être indiquées si la fraction d’éjection ventriculaire gauche est altérée en post-IDM (FEVG ≤ 40 % mais elles seront détaillées dans une autre partie du programme d’enseignement de cardiologie (voir chapitre 5)
Une réadaptation cardiovasculaire favorisant l’observance thérapeutique, le contrôle des facteurs de risque, le respect d’un régime alimentaire adapté et la pratique d’une activité physique régulière est proposée dans tous les cas ainsi qu’un suivi cardiologique à vie, avec mise en place d’une éducation thérapeutique (le patient devenant acteur et actif dans le traitement de la maladie coronaire et des facteurs de risque).
Prise en charge du SCA sans sus décalage du segment ST
Dans certains cas, le tableau clinique est sévère d’emblée avec un ou plusieurs des signes suivants : douleur thoracique persistante, insuffisance cardiaque (œdème pulmonaire), défaillance hémodynamique (choc), troubles du rythme ventriculaire graves, modifications dynamiques du segment ST (sus décalage transitoire). Ces patients sont considérés à très haut risque et doivent être transportés en urgence par une équipe médicalisée vers une salle de coronarographie. La prise en charge dans cette situation sera très proche de celle décrite ci-dessus pour le SCA avec sus-décalage du segment ST.
Dans les autres cas, la coronarographie pourra être un peu retardée de 12 à 24 heures selon les signes de gravité. Pendant ce temps un traitement antithrombotique est débuté avec surveillance en USIC. Ce traitement associe :
- aspirine 250 mg IV ou per os ;
- fondaparinux sous cutané ou enoxaparine sous cutanée ou héparine non fractionnée.
La coronarographie sera réalisée précocement dans les 12 à 24 heures chez les patients à haut risque (élévation de la troponinémie, modifications de la repolarisation sur l’ECG, diabète, etc.).
La coronarographie ne sera pas réalisée systématiquement en cas de douleur thoracique ne récidivant pas avec absence d’anomalie à l’ECG et absence d’élévation de la troponinémie. Dans ce cas, un test de dépistage non invasif de la maladie coronaire (test d’ischémie avec ou sans imagerie couplée sera réalisé avant de proposer une coronarographie. Ce test devra néanmoins être réalisé avant de laisser sortir le patient de l’hôpital (à la différence de l’angor stable ou ce type d’examen est fait en externe sur rendez-vous).
Au décours de la phase aiguë le traitement au long cours est le même que pour les patients ayant présenté un IDM avec sus-décalage du segment ST (cf. supra).
________________________________________________________________________________
Points importants
- Le système vasculaire propre au coeur comporte les artères coronaires gauche et droite qui se connectent au niveau de l’aorte ascendante quelques centimètres au-dessus de la valve aortique, des veines dont le drainage principal se fait par un collecteur appelé sinus coronaire qui se termine dans l’atrium droit, et des lymphatiques.
- L’artère coronaire gauche débute par le tronc coronaire et se divise en deux branches principales : l’interventriculaire antérieure et la circonflexe. La coronaire droite, en général moins développée que la gauche, se divise en interventriculaire postérieure et rétroventriculaire gauche.
- La distribution artérielle coronaire est de type terminal (chaque artère vascularisant un territoire), mais des anastomoses entre artères par des collatérales sont possibles.
- Sur le plan embryologique, la vasculogenèse des artères coronaires débute à partir de sinusoïdes embryonnaires situées dans les sillons interventriculaires et coronaires, se poursuit autour de l’ébauche des troncs artériels, pour finalement remonter vers l’aorte et établir des connexions avec les sinus aortiques. En général, seules deux connexions persistent pour former les deux ostia artériels coronaires (droit et gauche).
- Les artères coronaires sont des artères musculaires composées de trois couches : l’intima (épithélium pavimenteux reposant sur une lame basale et un tissu conjonctif), la média (constituée de lames élastiques et de cellules musculaires lisses) et l’adventice (essentiellement constituée de tissu conjonctif). L’endothélium, couche la plus interne, joue un triple rôle : transport de molécules (cholestérol, glucose, oxygène, médiateurs neuro-hormonaux, etc.), maintien du sang à l’état liquide (inhibition de l’activation-agrégation plaquettaire et de la coagulation) et régulation de la vasomotricité coronaire (via la sécrétion de monoxyde d’azote vasodilatateur et de l’endothéline vasocontrictrice).
- La consommation d’oxygène du myocarde est dépendante de la fréquence cardiaque, de la pression artérielle systolique et de la contractilité du myocarde.
- Le débit coronaire, rythmé par la contraction du myocarde, est diastolique à 80 % à gauche, et à égalité entre la diastole et la systole pour le ventricule droit.
- Le débit coronaire normal est de 0,8 à 1 l/min/gramme de myocarde pour le ventricule gauche et de 0,6 à 0,7 ml/min/gramme de myocarde pour le ventricule droit.
- Le débit coronaire représente 5 % du débit cardiaque chez un sujet normal.
- L’adaptation du débit coronaire à la demande en oxygène du myocarde se fait dans la microcirculation coronaire (petites artères et artérioles) et dépend de trois facteurs : métabolisme du myocarde, endothélium coronaire et système nerveux autonome.
- L’endothélium coronaire produit le monoxyde d’azote (NO), substance relaxante des cellules musculaires lisses de la paroi vasculaire et donc le responsable de la vasodilatation des vaisseaux. Le système nerveux autonome contrôle la vasomotricité coronaire.
- Les récepteurs bêta 1 et bêta 2 adrénergiques prédominent dans les petites artères coronaires ; les récepteurs bêta adrénergiques sont prédominants dans les artérioles coronaires.
- La réserve de débit coronaire correspond à la capacité maximale de vasodilatation de la circulation coronaire pour une pression de perfusion coronaire donnée. La réserve de débit coronaire normal est comprise entre 3,5 et 4,5.
- Le métabolisme cardiaque est principalement aérobie. Le fonctionnement normal du cœur nécessite une production permanente d’ATP et donc des apports permanents et adéquats en O2 au myocarde. Le rôle de la circulation coronaire est d’assurer une bonne adéquation entre les besoins et les apports en O2 au myocarde. Les besoins en O2 vont augmenter avec la fréquence cardiaque, la contractilité du muscle cardiaque et la contrainte pariétale. Les apports en O2 vont varier en fonction de la teneur du sang en O2 et du débit coronaire. Dans des conditions physiologiques, la régulation du débit sanguin coronaire suit les fluctuations des besoins en O2 du muscle cardiaque. Cette adaptation se fait principalement par la régulation du débit sanguin myocardique grâce aux facteurs influençant la vasomotricité des artérioles coronaires (vasodilatation et vasoconstriction).
- L’ischémie myocardique est liée à une inadéquation entre besoins et apports en O2 au myocarde. Celle-ci est soit liée à un problème global (hypoxie importante, par exemple) soit à une anomalie locale (sténose serrée d’une artère coronaire). Les anomalies de perfusion aboutissent à des anomalies du métabolisme myocardique puis à des anomalies de fonction contractile du myocarde. Ces dysfonctions sont initialement réversibles. Néanmoins, dans les cas extrêmes tels que l’occlusion coronaire aiguë, les cellules myocardiques nécrosent et le phénomène devient irréversible.
- La cascade à l’origine d’une ischémie myocardique fait d’intervenir successivement : la réduction de la perfusion myocardique, puis l’altération du métabolisme myocardique, précédant une altération de la fonction mécanique, relaxation et contraction du myocarde ischémique, précédant les troubles de l’électrogénèse, et l’apparition de la douleur angineuse.
- La pathologie des artères coronaires est essentiellement consécutive au développement de l’athérome coronaire lié à la présence de facteurs de risque dont les effets délétères se multiplient entre eux. Ces facteurs sont essentiellement l’âge, le sexe masculin, le diabète, l’hypertension artérielle, l’hypercholestérolémie avec élévation du LDL-cholestérol, le tabagisme.
- La formation d’une brèche endothéliale donne accès à de nombreux éléments sanguins, notamment des globules rouges.
- L’accumulation précoce du cholestérol dans la paroi constitue la strie lipidique dans laquelle le cholestérol s’oxyde et peut être capté par les cellules musculaires lisses et les monocytes/macrophages, qui se transforment en cellules spumeuses, composantes essentielles de la formation du noyau lipidique dans le fibro-athérome.
- Les plaques coronaires sujettes à l’érosion sont responsables de 20 à 30 % des événements coronaires aigus.
- Ces plaques contiennent plus de cellules musculaires lisses ainsi qu’une matrice extracellulaire riche en protéoglycanes et en acide hyaluronique, comparativement aux plaques vulnérables.
- Les plaques coronaires sujettes à l’érosion sont faiblement inflammatoires, moins chargées en lipides et dépourvues de zones nécrotiques dans plus de la moitié des cas.
- Les deux modalités d’évolution de la plaque, rupture ou érosion, conduisent à des modalités d’expression clinique variée.
- Dans les deux cas, l’altération de la plaque induit la formation d’un thrombus intracoronaire qui peut connaître quatre modalités évolutives : lyse in situ ; transformation fibrocalcaire contribuant à réduire le calibre de l’artère ; réduction brutale du calibre de l’artère sans occlusion complète ; embolisation en distalité et occlusion totale et brutale de l’artère coronaire
- La sémiologie, étude des signes cliniques des affections, regroupe des signes fonctionnels (ceux dont se plaint le patient) et les signes physiques (découverts par l’examen du patient). Au cours des affections d’origine coronaire, les signes fonctionnels sont dominés par les douleurs coronariennes (angor et douleur de l’infarctus) et par des signes de complications évolutives (notamment la dyspnée d’effort qui traduit l’insuffisance cardiaque gauche).
- L’angor ou angine de poitrine, douleur thoracique angineuse est la traduction clinique de l’ischémie myocardique, quelle qu’en soit la cause.
- La douleur angineuse est évocatrice par son caractère constrictif, sa localisation médiothoracique rétrosternale, irradiant vers le cou, la mâchoire, la face interne du bras gauche.
- La douleur de l’angor typique survient à l’effort dont elle impose l’arrêt et disparaît après l’arrêt de l’effort et/ou l’administration de trinitrine par voie sublinguale. La douleur révélant un infarctus myocardique est une douleur angineuse mais survenant habituellement au repos, prolongée (supérieure à 20 minutes) et non soulagée par la trinitrine.
- L’intensité de la douleur angineuse n’est pas proportionnelle à la gravité de la pathologie coronaire sous-jacente.
- Le terme actuellement usité par les recommandations européennes en lieu et place de l’angor stable est le syndrome coronaire chronique.
- Le seuil ischémique, déséquilibre entre les besoins et les apports en oxygène au myocarde, est défini par le niveau d’effort pour lequel l’angor survient.
- Le syndrome coronaire aigu (SCA), angor instable ou infarctus du myocarde, est la traduction clinique d’une ischémie myocardique aiguë, déclenchée par la diminution brutale des apports myocardiques en oxygène et à la formation aiguë d’un thrombus intracoronaire, totalement occlusif (infarctus du myocarde) ou non (syndrome coronaire aigu sans sus décalage du segment ST).
- L’angor crescendo, l’angor de novo et l’angor de repos ou spontané sont considérés comme des syndromes coronaires aigus.
- L’électrocardiogramme d’un syndrome coronaire aigu doit distinguer la présence ou non d’un sus-décalage du segment ST (SCA STEMI versus non STEMI) correspondant à un territoire coronaire.
- Les diagnostics différentiels de la douleur angineuse sont la douleur thoracique de péricardite aiguë, l’embolie pulmonaire et surtout la dissection aortique aiguë, urgence médico chirurgicale.
- L’ECG per-critique lors d’une ischémie myocardique documente des anomalies de la repolarisation ventriculaire dépendant du type de syndrome coronaire aigu.
- L’exploration de la fonction ventriculaire gauche, notamment la mesure de la fraction d’éjection du ventricule gauche (FEVG), élément pronostique majeur, est en général réalisée par l’écho-Doppler cardiaque. Il est possible de faire appel aux techniques isotopiques ou à l’IRM pour préciser cette étude.
- L’épreuve d’effort est indiquée à la recherche d’arguments pour une ischémie myocardique et est contre-indiquée en cas de syndrome coronaire aigu.
- Elle est indiquée en cas de douleur thoracique atypique à la recherche de la documentation d’une ischémie myocardique et en cas de maladie coronaire chronique, pour rechercher une ischémie myocardique résiduelle après revascularisation et à la recherche d’optimisation du traitement médicamenteux.
- Le test à la recherche de la documentation d’une ischémie couplé à une imagerie comporte l’échographie de stress, la scintigraphie myocardique de stress et l’IRM de stress.
- Le principe général d’un test d’ischémie est de coupler les données cliniques (apparition d’un angor, intolérance hémodynamique), électrocardiographiques à l’effort (délai d’apparition de l’ischémie, hyperexcitabilité ventriculaire, bloc de branche gauche), avec des données morphologiques permettant de caractériser la topographie et l’étendue de l’ischémie myocardique.
- Le scanner coronaire a une bonne sensibilité et spécificité pour détecter des lésions coronaires, et est indiqué en dehors d’un syndrome coronaire aigu.
- La coronarographie est l’examen d’exploration des coronaires de référence, indiquée de façon systématique dans un contexte de syndrome coronaire aigu.
- La précocité de cet examen est justifiée en cas d’un syndrome coronaire aigu avec sus décalage du segment ST (STEMI), de façon à proposer une revascularisation qui réduit la morbimortalité.
- La coronarographie peut documenter une sténose, considérée comme significative pour une réduction de diamètre supérieur à 70 % (supérieur à 50 % pour le tronc commun de la coronaire gauche) ; elle peut mettre en évidence une occlusion coronaire.
- Dans certaines situations, les artères coronaires sont angiographiquement normales et un spasme coronaire peut être documenté, soit lors du cathétérisme sélectif de l’artère, soit après injection par voie intraveineuse d’un médicament vasoconstricteur comme la méthylergométrine.
- La fraction de réserve coronaire (FFR) consiste à mesurer l’impact hémodynamique ou fonctionnel d’une sténose coronaire visible en angiographie. Elle est considérée comme altérée lorsqu’elle est inférieure à 80 %.
- Parmi les biomarqueurs caractérisant la nécrose myocytaire, les troponines Ic et Tc sont utilisées actuellement de façon exclusive dans la documentation de l’ischémie myocardique, supplantant le dosage des isoenzymes MB de la créatine kinase (CPK-MB).
- Les principes du traitement de la maladie coronaire sont la réduction de l’ischémie myocardique à l’aide des antiangineux, la revascularisation coronaire, la prévention et/ou le ralentissement de l’évolution des lésions athéromateuses par le contrôle des facteurs de risque et enfin la prévention de la thrombose ou des récidives de thrombose coronaire à l’aide des antiagrégants plaquettaires et/ou des anticoagulants, en fonction du contexte.
- Les dérivés nitrés sont des prodrogues sources de monoxyde d’azote (NO) et leur action est liée à la capacité de former des radicaux libres NO.
- Les dérivés nitrés ne doivent pas être utilisés en association avec des inhibiteurs de la phosphodiestérase, sildénafil, tadalafil et vardénafil, du fait d’un risque d’hypotension artérielle sévère.
- Les bêtabloquants sont un médicament de référence de la maladie coronaire. Il convient de privilégier un bêtabloquant cardiosélectif en respectant les contre-indications.
- Les inhibiteurs calciques, antagonistes des canaux calciques lents voltage-dépendant des cellules musculaires lisses comprennent deux classes : les dihydropyridines et les non-dihydropyridines ayant un effet bradycardisant tel le diltiazem et le vérapamil.
- Les antiagrégants plaquettaires per os comprennent l’acide acétylsalicylique ou aspirine et les inhibiteurs de P2Y12.
- L’aspirine agit en inhibant de façon irréversible la cyclo-oxygénase ou COX1, et à un degré moindre la COX2 et diminue la production de thromboxane A2.
- Les bloqueurs du récepteur plaquettaire P2Y12 comprennent les molécules suivantes : clopidogrel, prasugrel, ticagrélor et cangrélor.
- Les anti-GPIIbIIIa ne sont utilisés que par voie injectable sur des périodes courtes, pour encadrer un geste de revascularisation percutané.
- Parmi les anticoagulants, les héparines (non fractionnée ou héparine de bas poids moléculaire) sont les molécules de référence dans le syndrome coronaire aigu.
- La place des thrombolytiques à la phase aiguë d’un infarctus du myocarde avec sus décalage du segment ST (STEMI) a été réduite par la place accordée à l’angioplastie primaire, plus efficace et à moindre risque hémorragique.
- La stratégie thérapeutique du traitement d’un syndrome coronaire chronique comprend l’association d’un antiagrégant plaquettaire, d’une statine, d’un inhibiteur de l’enzyme de conversion, d’un bêtabloquant et d’un dérivé nitré d’action rapide réservé à la crise angineuse.
- La revascularisation coronaire par angioplastie avec stenting ou pontage aortocoronaire est recommandée en cas de non-contrôle des symptômes angineux par un traitement médicamenteux optimal, en cas de lésions coronaires sévères, intéressant le tronc commun de la coronaire gauche et/ou la présence de lésions coronaires multiples peu accessibles à un geste percutané, et en cas d’altération de la fonction ventriculaire gauche.
- La discussion au cas par cas lors d’une confrontation médico-chirurgicale est recommandée pour choisir la méthode de revascularisation optimale.
- En cas de syndrome coronaire aigu avec sus décalage du segment ST (STEMI), l’urgence est de rétablir la perfusion coronaire après une coronarographie qui doit être effectuée dans les meilleurs délais.
- En l’absence de sus décalage du segment ST lors d’un syndrome coronaire aigu (non-STEMI), la coronarographie peut être différée de 12 à 24 heures, en fonction des signes de gravité, et après instauration du traitement pharmacologique.
- En post SCA le traitement préventif optimal comporte un béta bloqueur, une bi anti agrégation plaquettaire associant l’aspirine et un inhibiteurs de P2Y12 de durée variable, un traitement faisant baisser le cholestérol (statines, ézétimibe, anti PCSK9) avec un objectif de diminution de 50 % du LDL cholestérol devant atteindre une concentration < 0,55 g/L, un inhibiteur de l’enzyme de conversion de l’angiotensine (on un sartan en alternative), un dérivé nitrés d’action rapide en cas de crise angineuse et un contrôle optimal des facteurs de risque qui passe notamment par un programme de réadaptation cardiaque. Un suivi cardiologique au long cours est indispensable.
________________________________________________________________________________
Compléments en ligne
Des compléments numériques sont associés à cet ouvrage. Ils proposent des vidéos. Pour voir ces compléments, connectez-vous sur http://www.em-consulte.com/e-complement/475848 et suivez les instructions.
________________________________________________________________________________
Vidéo 3.1
Ciné-IRM cardiaque, orientation grand axe vertical.Akinésie post-infarctus myocardique dans le territoire apical.
________________________________________________________________________________
Vidéo 3.1 : Ciné-IRM cardiaque, orientation grand axe vertical. Akinésie post-infarctus myocardique dans le territoire apical.
Exercices en ligne
Les exercices relatifs à ce chapitre sont disponibles en ligne à l’adresse suivante : http://www.em-consulte.com/e-complement/475848
Partagez cette publication
Written by : SFC
Plus de publications de la SFC

CARDIOLOGIE PÉDIATRIQUE Tetralogy of Fallot: electrophysiology-guided surgical ablation during pulmonary valve replacement | Lire [...]

CARDIOLOGIE PÉDIATRIQUE 📌 À LA UNE : Tetralogy of Fallot: electrophysiology-guided surgical ablation during [...]


