Suivez-nous sur les réseaux sociaux !
Sommaire du chapitre :
Dernières publications
Publications
Chapitre 4 – Valvulopathies
Auteurs : A. Cohen, C. Kerneis, L.-D. Azoulay, B. Iung
Le cœur comprend quatre valves (voir chapitre 1 Anatomie du système cardiovasculaire).
À gauche, on distingue deux valves :
- la valve mitrale, atrioventriculaire, est formée de deux valvules ; elle permet la séparation de l’atrium gauche du ventricule gauche ;
- la valve aortique sépare le ventricule gauche de l’aorte ; elle est composée de trois valvules.
Le cœur droit comprend :
- la valve tricuspide, composée de trois valvules, est une valve atrioventriculaire séparant le ventricule droit de l’atrium droit ;
- la valve pulmonaire, elle aussi composée de trois valvules, permet de séparer le ventricule droit du tronc de l’artère pulmonaire.
Histologiquement, les valves sont formées d’endocarde, la tunique la plus interne des trois tuniques de la paroi cardiaque. Les valves cardiaques proviennent embryologiquement des bourgeons endocardiques. Leur développement débute entre la cinquième et la huitième semaine de vie.
Les valvulopathies sont classées selon deux critères :
- la localisation de la valve concernée : mitrale, aortique, tricuspide, ou pulmonaire ;
- le mécanisme de la pathologie : insuffisance (anomalie lors de la fermeture de la valve) ou rétrécissement (anomalie lors de l’ouverture de la valve).
De plus, il est important de différencier les valvulopathies aiguës des valvulopathies chroniques, dont les causes et les mécanismes hémodynamiques diffèrent.
Ce chapitre est consacré plus particulièrement aux trois principales valvulopathies :
- rétrécissement aortique et insuffisance aortique (l’association de ces deux valvulopathies étant appelée maladie aortique) ;
- insuffisance mitrale et rétrécissement mitral (l’association de ces deux valvulopathies étant appelée maladie mitrale) ;
- la sténose mitrale, les valvulopathies droites (régurgitation tricuspide) et les prothèses valvulaires ne seront que brièvement abordées.
Anatomie
Les valves cardiaques peuvent être schématiquement visualisées comme des clapets s’ouvrant et se fermant à chaque cycle cardiaque, et séparant les principales cavités cardiaques entre elles.
Le cœur est composé de quatre valves (fig. 4.1).
- deux valves séparent les atriums des ventricules :
- la valve mitrale sépare l’atrium gauche (AG) du ventricule gauche (VG),
- la valve tricuspide sépare l’atrium droit (AD) du ventricule droit (VD) ;
- deux valves séparent les ventricules des troncs artériels :
- la valve aortique sépare le ventricule gauche de l’aorte thoracique ascendante,
- la valve pulmonaire sépare le ventricule droit du tronc de l’artère pulmonaire.
________________________________________________________________________________
Figure 4.1. Vue d’ensemble des valves et des appareils sous-valvulaires.
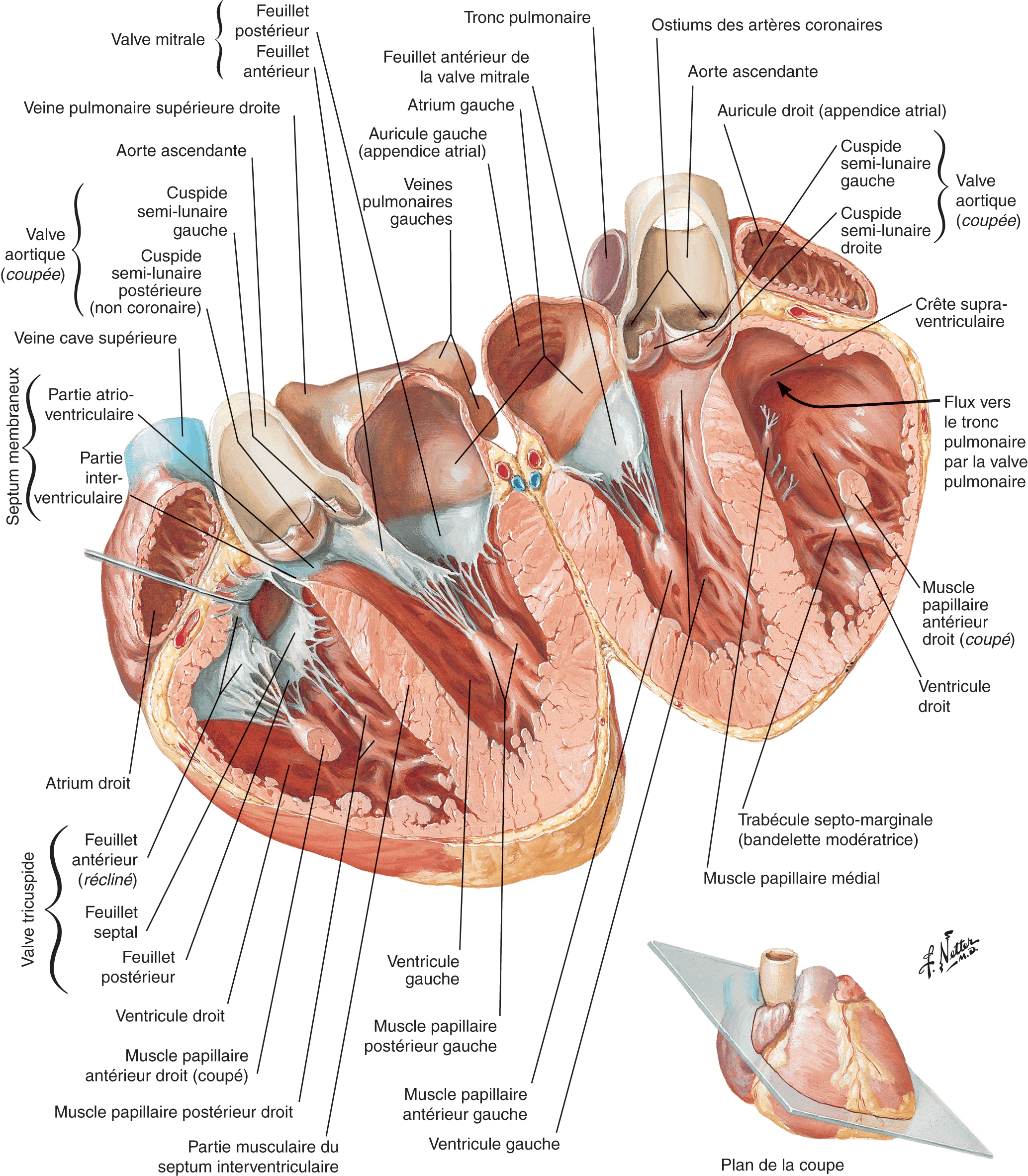
Chaque valve est elle-même composée de plusieurs feuillets (ou cuspides, ou valvules) : deux ou trois selon le type de valve. Ces feuillets se rejoignent en des points appelés commissures valvulaires.
Source : Netter FH. Atlas d’anatomie humaine. 5e édition. Paris : Elsevier-Masson ; 2011.
________________________________________________________________________________
Valve aortique (et aorte thoracique)
Localisation
La valve aortique sépare le ventricule gauche de l’aorte.
Description
La valve aortique est tricuspide, c’est-à-dire composée normalement de trois feuillets, ou cuspides (cusps en anglais), dont la taille et la morphologie sont normalement identiques : deux cuspides antérieures (antéro-droite et antéro-gauche) et une cuspide postérieure. Les cuspides de la valve aortique (et celles de la valve pulmonaire) diffèrent des cuspides des deux valves atrioventriculaires : de par leur forme de cupule, elles sont nommées valvules sigmoïdes ou encore cuspides semi-lunaires (fig. 4.2). Les valvules sigmoïdes sont naturellement ouvertes et accolées à la paroi aortique lors de l’éjection du sang du ventricule gauche vers l’aorte. Elles ne représentent donc pas d’obstacle à l’éjection lors de la systole en condition physiologique. C’est le retour sanguin en diastole qui ferme mécaniquement les valvules sigmoïdes aortiques.
________________________________________________________________________________
Rappel sur l’anatomie de l’aorte (voir chapitre 1, Anatomie)
La connaissance de l’anatomie de l’aorte ascendante est indispensable pour comprendre les valvulopathies aortiques dont une grande partie n’est pas liée à une anomalie des sigmoïdes directement, mais à une anomalie anatomique de l’aorte ascendante.
On distingue l’aorte thoracique de l’aorte abdominale. L’aorte thoracique est segmentée en trois parties : l’aorte ascendante, l’aorte horizontale et l’aorte thoracique descendante.
L’aorte ascendante est elle-même divisée en trois portions :
- la première portion correspond aux sinus de Valsalva (trois petites dilatations sur la portion initiale de l’aorte). C’est à ce niveau que se trouvent également les ostiums des deux artères coronaires : artère coronaire droite (sinus de Valsalva droit) et tronc commun de l’artère coronaire gauche (sinus de Valsalva gauche), qui se ramifie rapidement en artère circonflexe et artère interventriculaire antérieure. Lors de la diastole, le reflux de sang dans l’aorte entraîne la fermeture de la valve aortique et c’est à ce moment que se remplissent les artères coronaires et que s’effectue la vascularisation du myocarde (voir chapitre 3, Physiologie de la circulation coronaire). On notera que l’ostium de l’artère coronaire droite se trouve en regard de la cuspide semi-lunaire antéro-droite, tandis que l’ostium de la coronaire gauche se situe en regard de la cuspide semi-lunaire antéro-gauche (fig. 4.2) ;
- la deuxième portion est dénommée jonction sinotubulaire ;
- la troisième portion est l’aorte thoracique ascendante (dite tubulaire) à proprement parler.
________________________________________________________________________________
________________________________________________________________________________
Figure 4.2. Valves du cœur gauche.
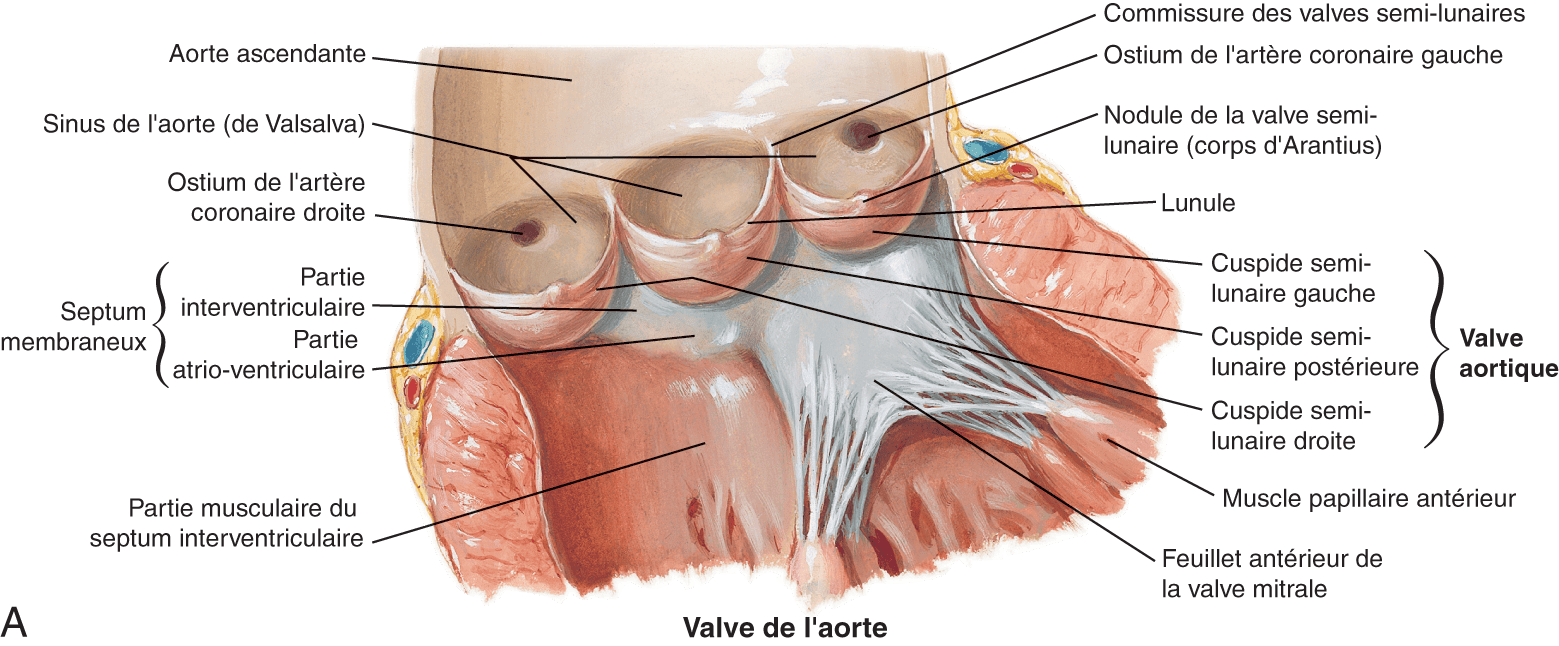
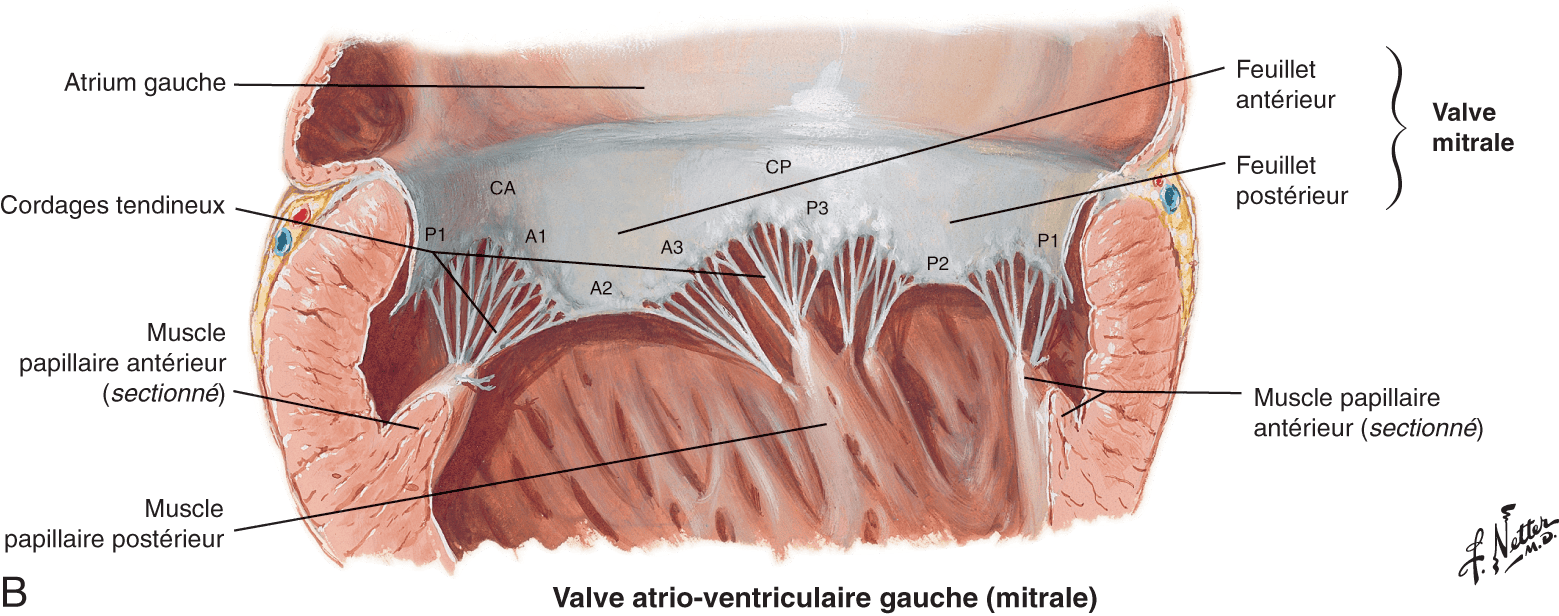
A. Les cuspides semi-lunaires (ou sigmoïdes) de la valve aortique, avec les deux ostium coronaires. La cuspide semi-lunaire postérieure, qui ne comporte pas d’ostium coronaire, est également dénommée « cuspide non coronaire ». B. Valve mitrale après ouverture de la paroi postérolatérale du ventricule gauche. Visualisation des deux piliers et des cordages rattachant les piliers aux deux feuillets valvulaires mitraux : le feuillet antérieur (A : A1 à A3), ou « grande valve mitrale », et le feuillet postérieur (P : P1 à P3), ou « petite valve mitrale ». CA, commissure antérieure ; CP, commissure postérieure.
Source : Netter FH. Atlas d’anatomie humaine. 5e édition. Paris : Elsevier-Masson ; 2011.
________________________________________________________________________________
Ces trois segments sont tous recouverts par le péricarde ce qui n’est plus le cas à partir de l’aorte thoracique horizontale.
Valve mitrale (ou appareil sous-valvulaire)
Localisation
La valve mitrale est la valve atrioventriculaire gauche, séparant l’atrium gauche du ventricule gauche (fig. 4.3).
________________________________________________________________________________
Figure 4.3. Vue interne du ventricule gauche.
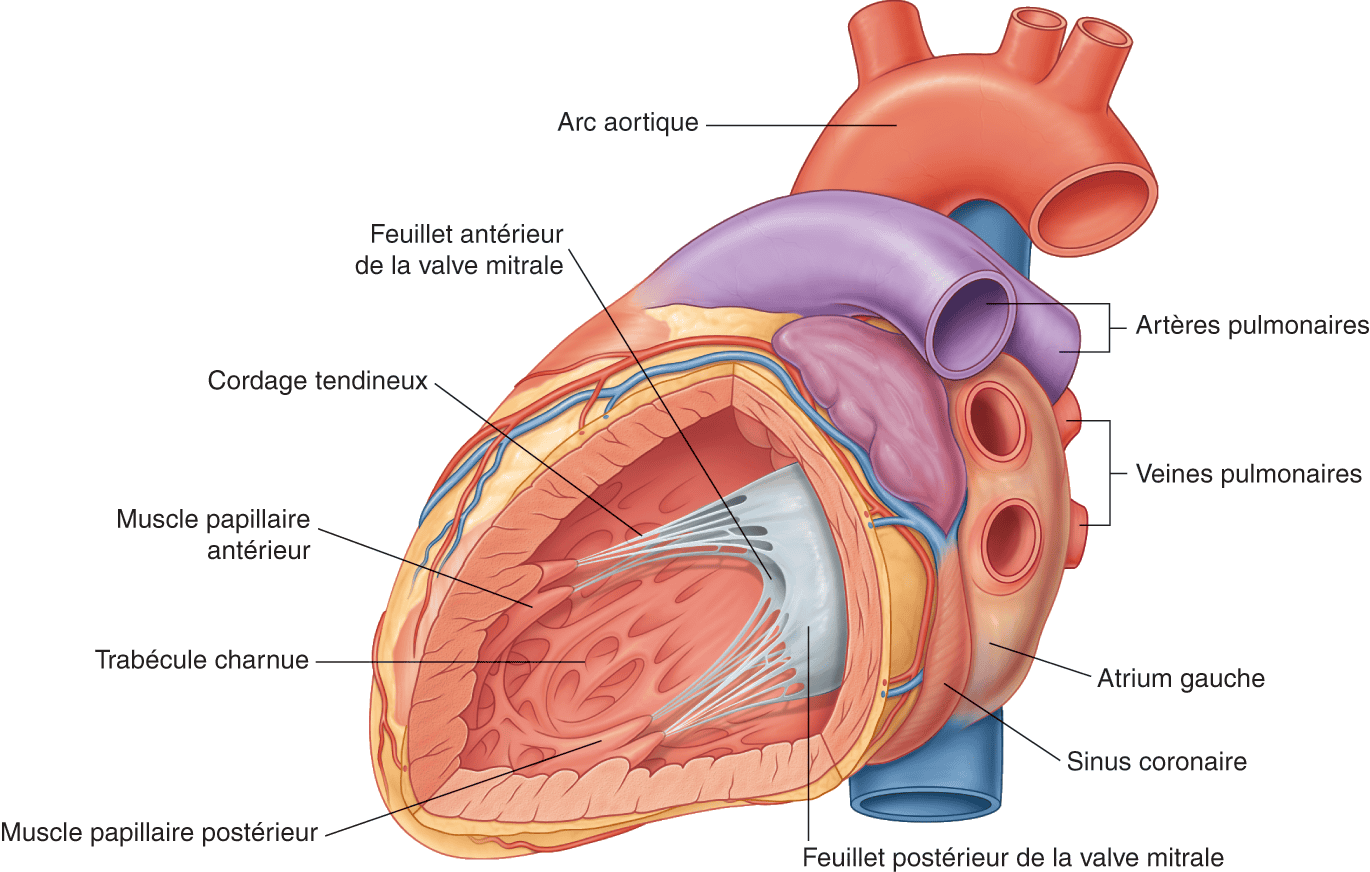
Source : Drake RL, Vogl AW, Mitchell AWM. Gray’s Anatomie pour les étudiants. 2e édition. Paris : Elsevier ; 2010.
________________________________________________________________________________
Description
La valve mitrale est bicuspide. Les deux feuillets qui la composent sont de taille inégale : on décrit une petite valve mitrale, ou valve postérieure, et une grande valve mitrale, ou valve antérieure. La surface de coaptation est le terme consacré à la ligne de contact entre les deux feuillets mitraux.
Chacun des deux feuillets est lui-même segmenté en trois sous-parties (fig. 4.2B), du fait de la présence de deux indentations par feuillet :
- le feuillet postérieur est ainsi divisé en trois parties : paracommissurale antérieure (P1), médiale (P2), paracommissurale postérieure (P3) ;
- il en va de même pour le feuillet antérieur regroupant à l’identique une partie paracommissurale antérieure (A1), médiale (A2) et paracommissurale postérieure (A3).
Ces deux feuillets se rejoignent en deux points :
- la commissure antérieure (CA), ou antérolatérale, jonction de A1 et P1 ;
- la commissure postérieure (CP), ou postéromédiale : jonction de A3 et P3.
Ces feuillets sont rattachés à l’anneau mitral, structure avant tout fibreuse, la valve mitrale antérieure s’insérant en regard du septum interventriculaire et la valve postérieure en regard de la partie externe de l’anneau.
Par ailleurs, l’appareil valvulaire mitral est relié à un squelette fibreux (cf. infra, Histologie) occupant l’espace interventriculaire gauche. Les feuillets mitraux sont rattachés sur leur face ventriculaire à des cordages fibreux, eux-mêmes reliés à des piliers (ou muscles papillaires), qui sont des extensions myocardiques. On décrit deux piliers : un pilier postéromédial (en regard de la commissure postérieure) et un pilier antérolatéral (en regard de la commissure antérieure). Le pilier postéromédial s’insère sur la paroi inférieure du myocarde, qui est vascularisée par une branche de la coronaire droite. La vascularisation du pilier antérieur dépend de l’artère coronaire gauche (voir chapitre 1, Vascularisation du cœur).
Ce système sous-valvulaire (piliers et cordages) empêche la protrusion des feuillets mitraux à l’intérieur de l’atrium gauche lors de la systole, c’est-à-dire lors de la fermeture de la valve mitrale et assure donc la coaptation valvulaire.
Valve pulmonaire
Localisation
La valve pulmonaire sépare le ventricule droit du tronc de l’artère pulmonaire (fig. 4.4).
________________________________________________________________________________
Figure 4.4. Vue médiale du ventricule droit : valve tricuspide et valve pulmonaire.
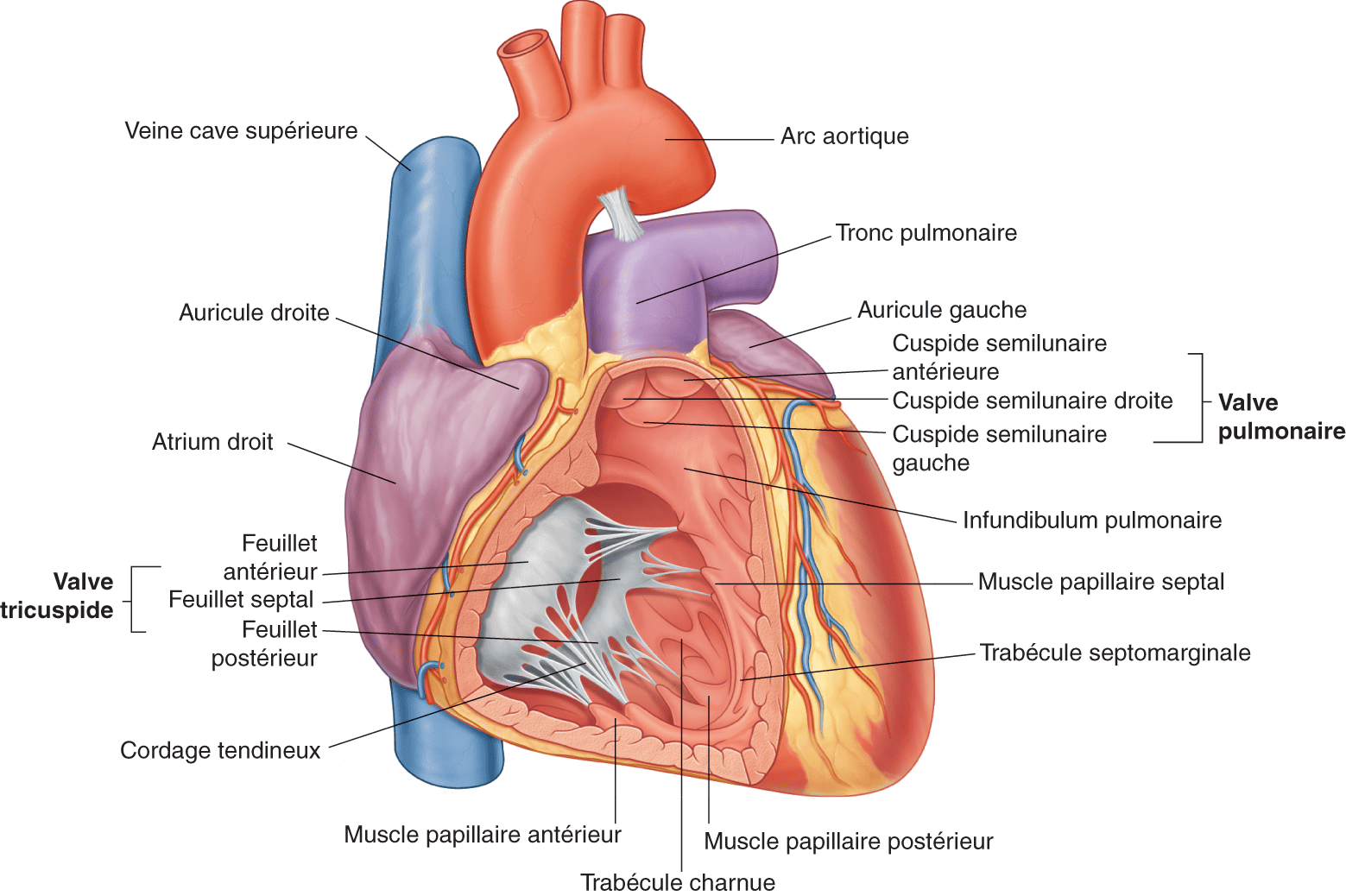
Source : Drake RL, Vogl AW, Mitchell AWM. Gray’s Anatomie pour les étudiants. 2e édition. Paris : Elsevier ; 2010.
________________________________________________________________________________
Description
Cette valve est composée de trois feuillets sigmoïdes : deux feuillets postérieurs et un feuillet antérieur.
Valve tricuspide
Localisation
La valve tricuspide est la valve atrioventriculaire droite, séparant l’atrium droit du ventricule droit (fig. 4.4).
Description
Cette valve est composée, comme son nom l’indique, de trois feuillets : un feuillet antérieur, un feuillet postérieur et un feuillet septal. Il existe un appareil sous-valvulaire fibreux comme pour la valve mitrale, mais il est composé ici de trois piliers (ou muscles papillaires antérieur, postérieur et septal).
Histologie
Principales cellules impliquées
Cellule endothéliale
Origine embryologique
La cellule endothéliale dérive du mésoblaste.
Localisation
Cette cellule, composant l’intima des vaisseaux sanguins et l’équivalent de l’intima au niveau cardiaque, l’endocarde, forme donc une interface entre le sang circulant et les tissus sous-jacents.
Composition
Cette cellule est habituellement polygonale. Son noyau unique est protrusif dans la lumière des vaisseaux s’il s’agit des cellules endothéliales vasculaires ou vers l’intérieur des cavités cardiaques dans le cas des cellules endothéliales de l’endocarde. Son cytoplasme est de faible épaisseur et comprend un réticulum sarcoplasmique granuleux, un appareil de Golgi, des mitochondries et des ribosomes.
Cardiomyocyte
Localisation
Cette cellule compose le myocarde, équivalent de la média au niveau cardiaque. Les cardiomyocytes représentent les trois quarts de la masse ventriculaire.
Composition
Il s’agit de cellules semblables aux cellules musculaires striées. Elles possèdent un noyau unique et un cytoplasme composé de mitochondries et d’un réticulum sarcoplasmique. Mais à la différence des cellules musculaires striées habituelles, le noyau des cardiomyocytes est central, il existe plus de mitochondries et le réticulum sarcoplasmique est moins développé.
La particularité de ces cellules musculaires réside dans la présence de sarcomères, résultant eux-mêmes de l’association de myofibrilles. Un sarcomère est une unité contractile : chaque sarcomère est composé d’une part de myofilaments épais de myosine et d’autre part de myofilaments plus fins d’actine. Le raccourcissement et l’allongement successifs des sarcomères au cours du cycle cardiaque, à l’origine de la contraction du muscle cardiaque, résultent de l’activation/désactivation de ponts d’actine-myosine en fonction du taux de calcium présent dans ces cellules. En plus de leur rôle contractile, ces cellules sont impliquées dans la fonction électrophysiologique cardiaque (voir chapitre 1, Physiologie, Cœur).
Tuniques myocardiques
Les parois du cœur sont constituées de trois tuniques.
Tunique interne : l’endocarde
L’endocarde est constitué d’une fine couche unique de cellules endothéliales reposant sur un tissu sous-endothélial, l’épaisseur totale étant d’environ 1 mm. C’est cette tunique interne (équivalent de l’intima vasculaire) qui constitue les valves cardiaques. L’endocarde et le myocarde sont reliés par une couche sous-endocardique de tissu conjonctif (qui comporte notamment les cellules de Purkinje du système cardionecteur ; voir chapitre 6, Histologie).
Tunique moyenne : le myocarde
C’est la couche la plus épaisse. C’est elle qui assure la contraction du muscle cardiaque. Elle est formée par les cellules musculaires striées myocardiques : les cardiomyocytes. Selon leur composition spécifique, on distingue les cellules musculaires dont la fonction est d’assurer une contraction/relaxation cardiaque, et les cellules musculaires dont la fonction est d’assurer une activité rythmique du cœur, ces cellules contiennent moins de myofibrilles et font partie du système cardionecteur. Ces fibres musculaires sont insérées sur le squelette fibreux (voir chapitre 1, Histologie, Tuniques cardiaques).
Tunique externe : l’épicarde, qui fait partie du péricarde
Le péricarde est l’enveloppe séreuse entourant le muscle cardiaque. Il est composé de deux feuillets accolés entre lesquels l’espace est virtuel. Il existe donc un feuillet externe, ou pariétal, et un feuillet interne, également appelé feuillet viscéral, accolé au myocarde : ce dernier feuillet est l’épicarde. L’épicarde est constitué d’un épithélium pavimenteux (la forme des cellules est rectangulaire, en pavé) simple (donc composé d’une seule couche de cellules), également dénommé mésothélium (moins de 1 mm d’épaisseur). L’épicarde et le myocarde sont reliés par une couche sous-épicardique composée d’un tissu conjonctif lâche.
Squelette fibreux
Au centre du cœur se trouve le squelette fibreux. Il est composé de fibres de collagène denses et comprend plusieurs éléments anatomiques :
- les anneaux fibreux sur lesquels s’insèrent les feuillets valvulaires ;
- les cordages, structures fibreuses reliant la face ventriculaire des valves atrioventriculaires aux piliers ;
- Les trigones fibreux : on décrit un trigone fibreux mitro-aortique (entre la valve antérieure mitrale et l’orifice aortique) et un trigone fibreux mitro-tricuspide (entre la valve mitrale et la valve tricuspide).
Les muscles papillaires n’appartiennent pas strictement au squelette fibreux, puisque ce sont des excroissances myocardiques intraventriculaires, appelés aussi muscles papillaires. Ils sont, cependant, en contact avec les cordages : via les cordages, deux muscles papillaires sont reliés à la valve mitrale et trois piliers sont reliés à la valve tricuspide. Pendant la systole, après la fermeture passive des valves atrioventriculaires, la contraction myocardique ventriculaire assure une traction sur les cordages par contraction des muscles papillaires, ce qui empêche l’éversion des feuillets valvulaires et la régurgitation du sang vers l’atrium, et assure l’étanchéité valvulaire.
Appareil valvulaire
Les valves cardiaques sont constituées d’un axe fibreux (fibres de collagène, fibres élastiques et quelques cellules musculaires lisses) autour duquel se dépose un revêtement de cellules endothéliales. Sur les valves atrioventriculaires, le versant atrial est le siège de la vascularisation artériolaire, tandis que le versant ventriculaire est relié au squelette fibreux.
Embryologie (voir chapitre 1)
Le cœur est le premier organe à fonctionner au cours de l’embryogenèse. Il se développe à partir de la troisième semaine de gestation. La première structure cardiaque est définie par deux tubes cardiaques latéraux, parallèles entre eux, composés d’une couche externe unique de cellules myocardiques et une couche interne unique de cellules endocardiques. Le tube cardiaque primitif est achevé au 22e jour de vie en moyenne. Il est alors fonctionnel : les premiers battements cardiaques apparaissent et le flux traversant le tube cardiaque se sépare en un flux droit et un flux gauche.
Un mouvement de rotation (droite), dénommé le looping, transforme ensuite ce tube cardiaque en une boucle (fig. 4.5). On y distingue les premières cavités cardiaques : le conus, le troncus, l’atrium primitif, le ventricule droit et le ventricule gauche primitifs.
________________________________________________________________________________
Figure 4.5. Looping cardiaque : mouvement de rotation (droite) qui transforme le tube cardiaque en une boucle.
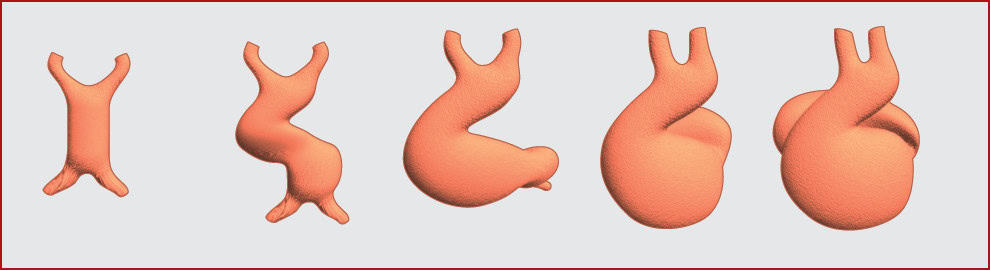
Source : Schleich J-M. Embryogenèse cardiaque. Arch Cardiovasc Dis, 2013 ; 106 : 612–23.
________________________________________________________________________________
Les valves atrioventriculaires se forment à partir de ces bourgeons endocardiques et des cellules du myocarde ventriculaire. Elles se formeront entre la cinquième semaine et la huitième semaine du développement embryonnaire. Les valves semi-lunaires aortique et pulmonaire dérivent de la région conotroncale (fig. 4.6) : à ce niveau se trouvent des bourgeons endocardiques, également dénommés crêtes conotroncales.
________________________________________________________________________________
- Précharge : Contraintes s’exerçant sur les parois du ventricule gauche à la fin de la diastole, avant la phase de contraction isovolumique. D’après la loi de Frank-Starling, la précharge conditionne la force de contraction myocardique, donc le volume d’éjection systolique.
- Post-charge : Somme de toutes les résistances à l’éjection ventriculaire (surface aortique plus ou moins rétrécie, résistances artérielles périphériques plus ou moins élevées), dont dépendent le volume et la pression télésystoliques.
- Loi de Laplace : T=P×D2e, avec T, tension pariétale ; P, pression intraventriculaire ; D, diamètre du ventricule gauche ; e, épaisseur pariétale (myocarde) du ventricule gauche.
- Loi de Frank-Starling : La force de contraction myocardique augmente avec le degré d’élongation des fibres myocardiques. Ainsi, plus le volume télédiastolique augmente, plus les fibres sont étirées et plus la contraction suivante sera puissante.
________________________________________________________________________________
Figure 4.6. Les trois étapes du développement cardiaque : looping, convergence, wedging. Le cercle rouge indique la position initiale puis finale de la valve aortique.
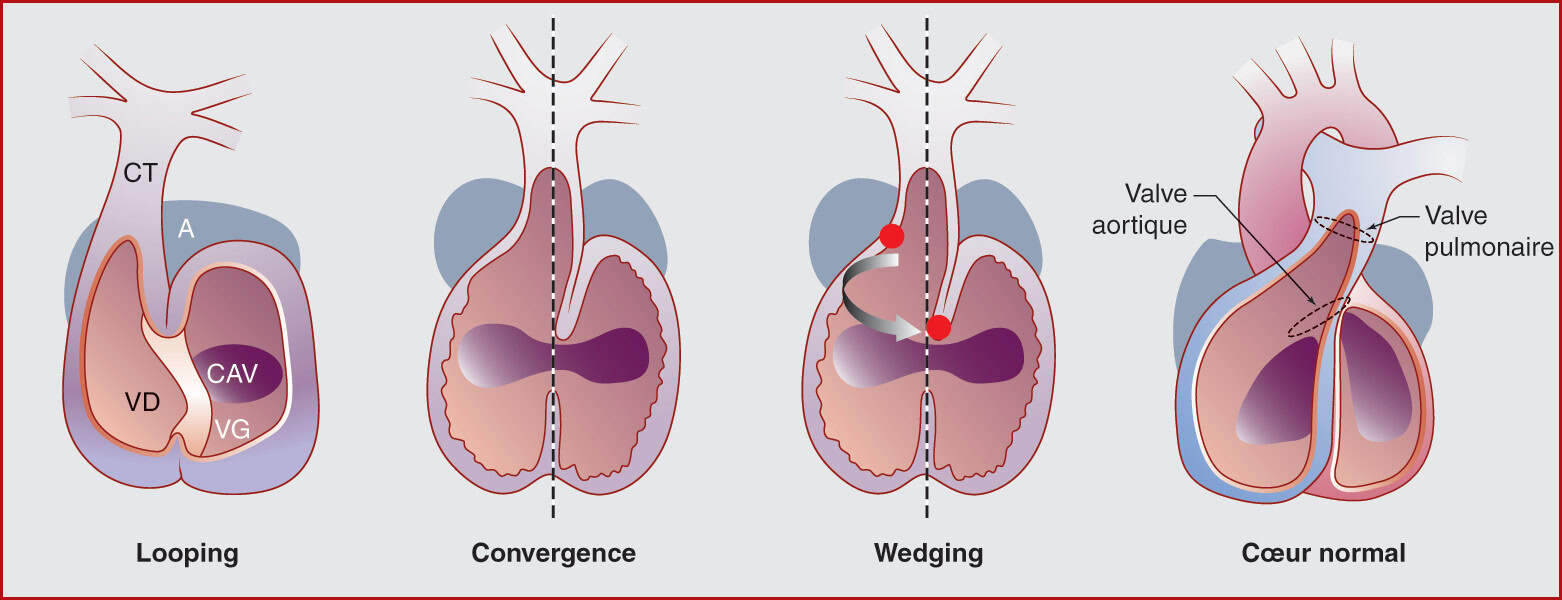
A, atrium ; CAV, canal atrioventriculaire ; VG, ventricule gauche ; CT, chambre de chasse (conotroncus) ; VD, ventricule droit.
Source : Schleich J-M. Embryogenèse cardiaque. Arch Cardiovasc Dis, 2013 ; 106 : 612–23.
________________________________________________________________________________
Physiopathologie
Voir fig. 4.7.
________________________________________________________________________________
Figure 4.7. Physiopathologie de l’HTAP dans les valvulopathies gauches.
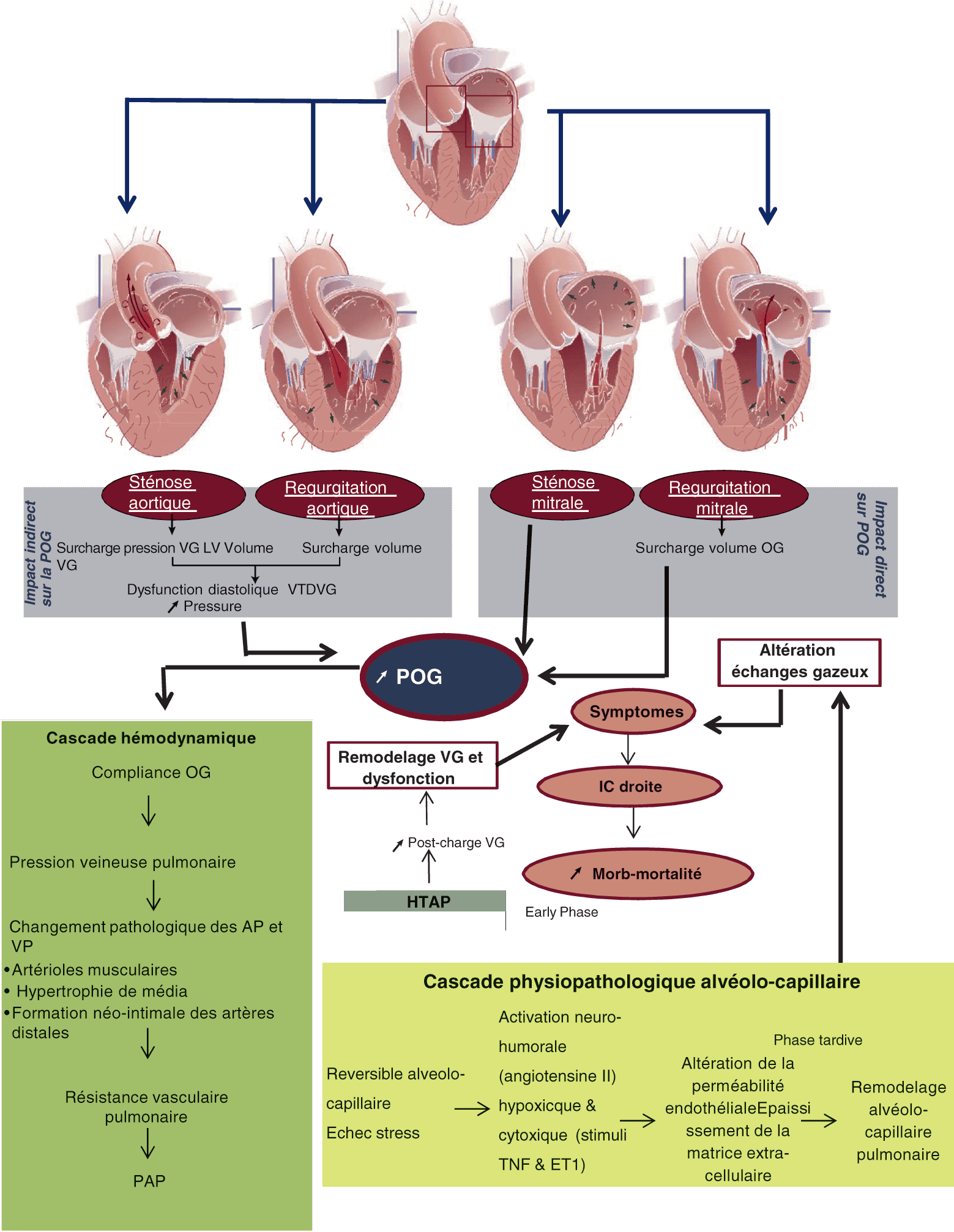
Source : d’après Magne J, JACC Cardiovasc Imaging. 2015;8:83–99.
________________________________________________________________________________
Sémiologie
La sémiologie des valvulopathies repose sur un élément clé de l’examen physique cardiovasculaire : l’auscultation cardiaque.
Il ne faut, cependant, pas négliger le reste de l’examen clinique qui, pour rappel, comprend l’interrogatoire du patient à la recherche des signes fonctionnels (plaintes du patient : dyspnée, douleur…) et l’examen physique qui comprend : l’inspection, la palpation, la percussion (bien que de peu d’implication ici) et, enfin, l’auscultation.
Les premières questions auxquelles il convient d » répondre au terme de l’examen clinique sont les suivantes :
- le type de valve atteinte : cela dépend du foyer cardiaque auquel est entendu le souffle, ainsi que de ses irradiations ;
- le mécanisme du souffle : rétrécissement ou insuffisance (régurgitation, fuite) ; les souffles de rétrécissement sont perçus lors de l’ouverture de la valve, tandis que les souffles d’insuffisance sont perçus lors de la fermeture de la valve ; cela dépend donc du temps auquel est perçu le souffle (systole ou diastole) et des caractéristiques du souffle (dur ou doux) ;
- la sévérité de la valvulopathie (par exemple, dans le rétrécissement aortique, signes fonctionnels ou abolition du B2 sont deux critères de rétrécissement serré).
Installation
Une auscultation cardiaque normale se réalise à l’aide d’un stéthoscope. Il comprend habituellement deux parties : le pavillon et la cloche. La membrane, ou pavillon, permet d’entendre les sons de haute fréquence (souffles) ; elle doit être appliquée assez fermement contre la poitrine. La cloche (plus petite que le pavillon) permet quant à elle de distinguer les sons de basse fréquence (bruits du cœur) ; elle doit être posée plus légèrement sur le patient.
L’examen se fait chez un patient habituellement en décubitus dorsal, torse nu, au repos. L’examinateur est habituellement positionné à la droite du patient.
Foyers d’auscultation cardiaque
Il en existe quatre (fig. 4.8) :
- foyer aortique : deuxième espace intercostal parasternal droit (les souffles aortiques peuvent également être bien audibles en regard du troisième espace intercostal gauche, correspondant à la localisation anatomique exacte de l’anneau aortique) ;
- foyer pulmonaire : deuxième espace intercostal gauche ;
- foyer tricuspide : au niveau de la xiphoïde ;
- foyer mitral : cinquième espace intercostal, au niveau de ligne médioclaviculaire, correspondant à l’apex du cœur.
________________________________________________________________________________
Figure 4.8. Les quatre foyers de l’auscultation cardiaque.
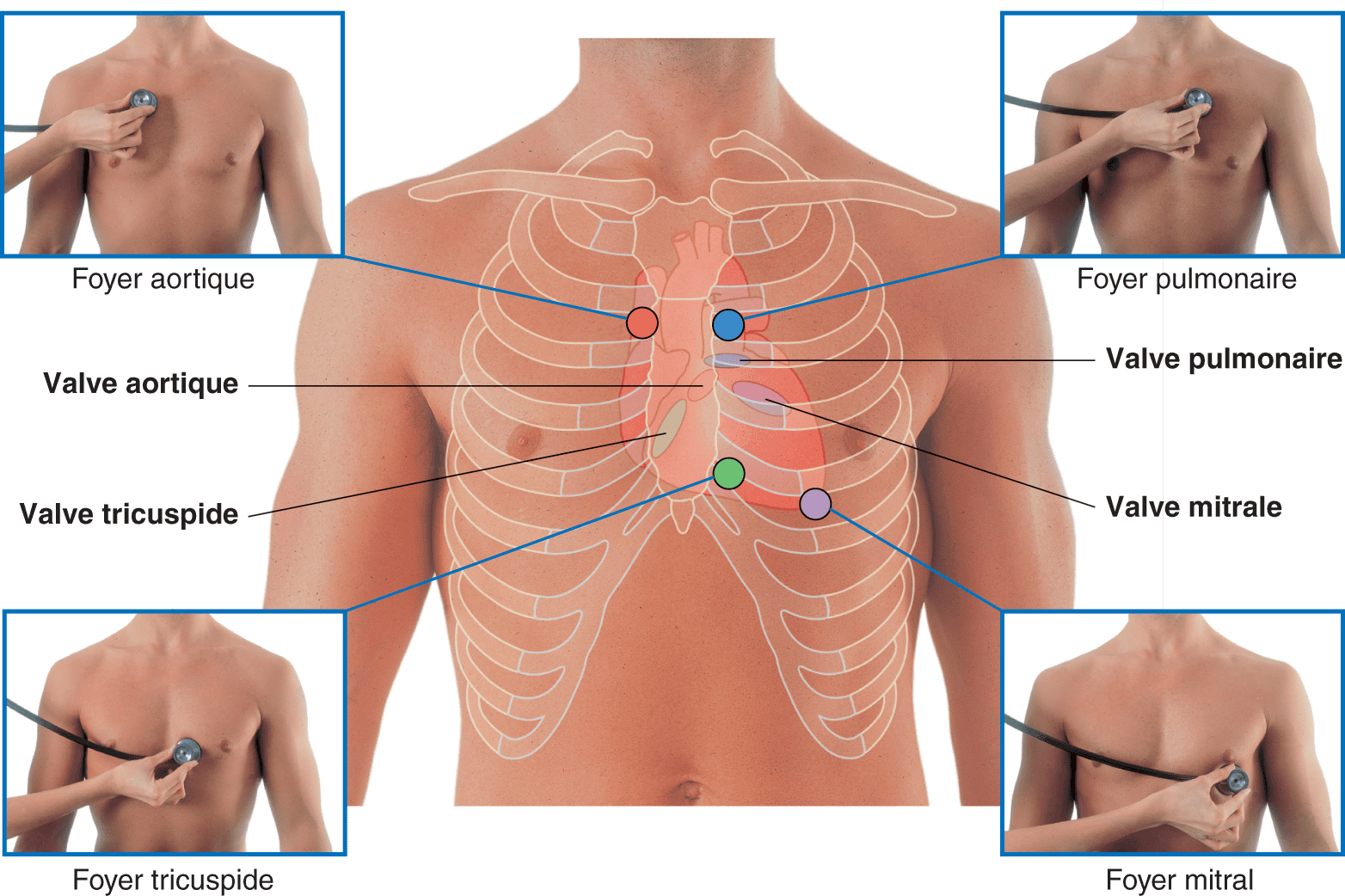
Source : Drake RL, Vogl AW, Mitchell AWM. Gray’s Anatomie pour les étudiants. 2e édition. Paris : Elsevier ; 2010.
________________________________________________________________________________
B1 (premier bruit du cœur)
Le bruit B1 marque le début de la systole. Il représente les bruits liés à la contraction myocardique associée à la fermeture des valves atrioventriculaires (mitrale et tricuspide). Il est maximal à l’apex du cœur (fig. 4.9).
________________________________________________________________________________
Figure 4.9. Hémodynamique intracardiaque et relation entre cycle cardiaque, bruits du cœur et souffles.
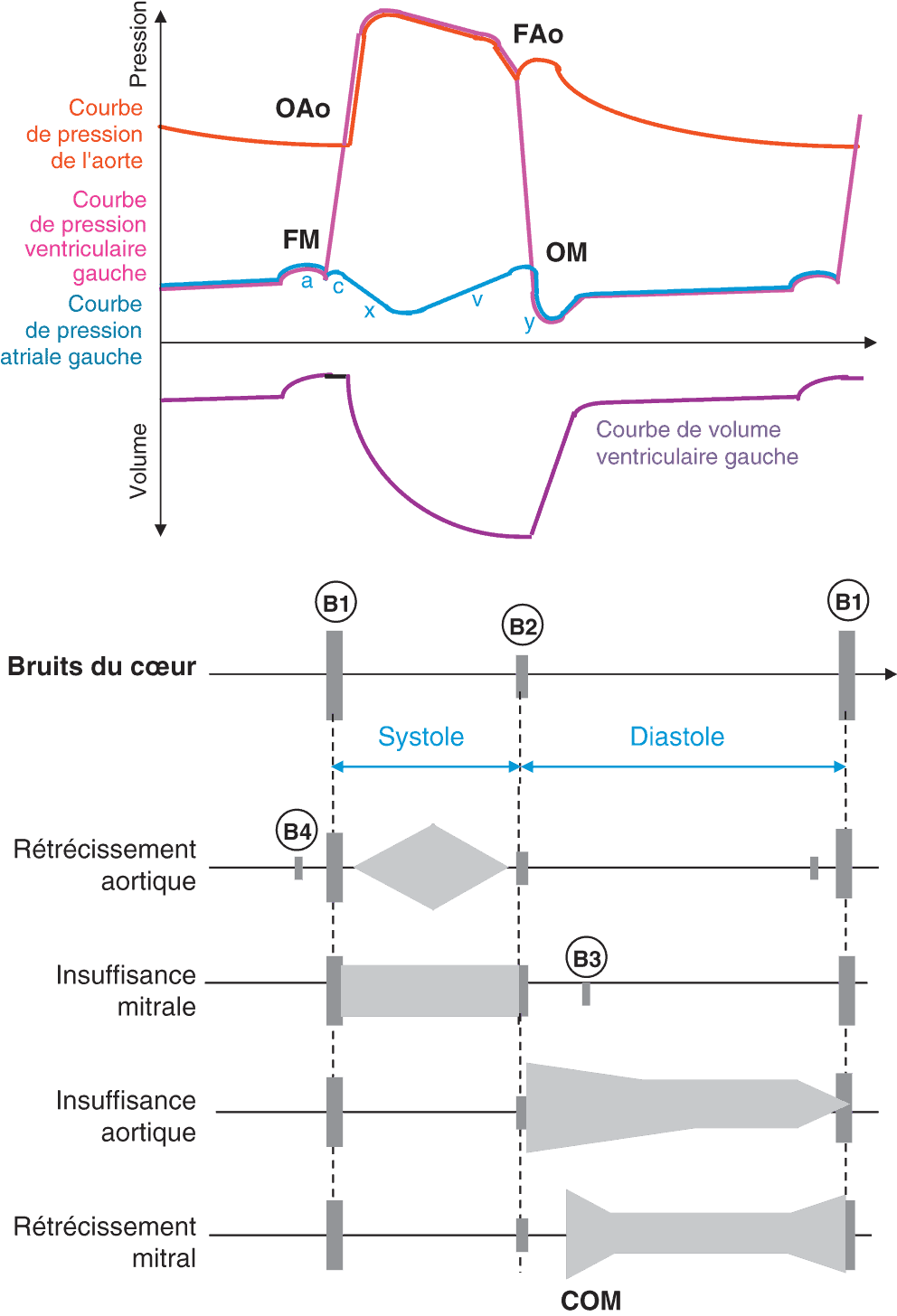
OAo, ouverture aortique ; FAo, fermeture aortique ; OM, ouverture mitrale ; FM, fermeture mitrale ; a, contraction atriale ; c, déflexion positive atriale (pas toujours observée, due à la pression ventriculaire sur la valve mitrale au début de la systole) ; x, réduction de la pression atriale post-a et remplissage ; v, augmentation de pression atriale suite au remplissage à valve mitrale fermée ; y, baisse de la pression atriale consécutive à la vidange atriale (ouverture de la valve mitrale) ; COM, claquement d’ouverture mitrale. B1 : premier bruit du cœur. B2 : deuxième bruit du cœur. B3 : galop protodiastolique. B4 : galop télédiastolique
________________________________________________________________________________
Son intensité est moindre chez les patients obèses, emphysémateux et en cas d’épanchement péricardique. Le B1 est accentué lorsque la valve mitrale est peu mobile. Les composantes audibles de B1 étant dues à la fermeture de la valve mitrale et de la valve tricuspide, un dédoublement peut être noté en cas de bloc de branche droit ou gauche ainsi qu’en cas de tachycardie ventriculaire.
Le dédoublement du B1 ne doit pas être confondu avec un bruit de galop présystolique, ou B4, mieux perçu à la pointe avec la cloche du stéthoscope, alors que le dédoublement du B1 est entendu dans la région parasternale gauche avec le diaphragme du stéthoscope.
B2 (deuxième bruit du cœur)
Le bruit B2 marque le début de la diastole et correspond donc à la fermeture des valves pulmonaire et aortique. La tonalité de B2 est discrètement plus aiguë que B1 et d’intensité plus forte. Un éclat du B2 peut-être un signe d’hypertension pulmonaire (l’hyperpression dans l’artère pulmonaire va, après la systole, propulser les cups de la valve pulmonaire les unes contre les autres de manière vigoureuse)
B3 (troisième bruit du cœur)
Le bruit B3, diastolique, survient après le deuxième bruit, il n’est entendu que de façon inconstante à la pointe en cas de B3 ventriculaire gauche. La présence d’un B3 est normale chez l’enfant ou l’adulte jeune.
Lorsqu’il existe une dysfonction ventriculaire systolique, la perception d’un B3 est appelée bruit de galop ventriculaire, ou galop protodiastolique. Le B3 correspond à l’irruption, en protodiastole, de sang dans un ventricule gauche qui n’a pas éjecté l’ensemble de sa pré-charge, du fait d’une dysfonction systolique (anomalie de la fonction pompe). La pression y est alors élevée en protodiastole, et le remplissage passif de l’oreillette gauche vers le ventricule gauche, produit alors un bruit : le B3. L’association B1-B2-B3 évoque à l’auscultation un bruit de galop.
Les autres causes de perception d’un B3 sont l’insuffisance mitrale volumineuse, le shunt gauche/droit et en cas d’hyperdébit (anémie sévère, hyperthyroïdie, fistule artérioveineuse, béribéri et maladie de Paget).
Un B3 correspond à une dysfonction ventriculaire systolique (anomalie de la phase d’éjection ventriculaire).
B4 (quatrième bruit du cœur)
Le bruit B4 correspond à la contraction atriale après le début de l’onde P et donc un peu avant B1. Le B4 peut être perçu de façon physiologique chez les sujets âgés, correspondant alors à l’augmentation de la contribution atriale au remplissage ventriculaire. En pathologie, un B4 audible traduit une perte de la distensibilité ventriculaire en rapport avec une hypertrophie pariétale ou une insuffisance cardiaque à FEVG préservée. Le défaut de relaxation ventriculaire gauche entraîne une augmentation des pressions lors du remplissage passif proto-mésodiastolique, ainsi, en télédiastole, le sang éjecté par la contraction atriale provoque le B4.
Un B4 correspond à une dysfonction ventriculaire diastolique (trouble de relaxation ou de compliance ventriculaire gauche)
Reconnaître B1 et B2 permet de distinguer la systole de la diastole. Une autre méthode est également utilisée pour distinguer ces deux temps : la prise du pouls de façon simultanée à l’auscultation cardiaque ; en effet, la pulsation de l’artère radiale est contemporaine de la systole.
L’intervalle entre B1 et B2 (systole) est plus court que l’intervalle entre B2 et B1 (diastole). Ces intervalles sont normalement réguliers entre chaque cycle cardiaque.
Auscultation d’un souffle cardiaque (fig. 4.8)
Pour analyser un souffle cardiaque, il faut pouvoir préciser plusieurs points.
À quel foyer le souffle est-il perçu ?
Pour répondre à cette question, il faut avoir ausculté les quatre foyers cardiaques : aortique, pulmonaire, tricuspide, mitral. Il ne faut, cependant, pas se limiter aux quatre foyers cardiaques : il est important d’ausculter également les régions parasternales, les axes carotidiens (irradiation fréquente des souffles aortiques) et le creux axillaire (irradiation des souffles mitraux).
À quel temps le souffle apparaît-il ?
Préciser si le souffle est entendu pendant la systole ou la diastole et à quel temps, en essayant d’être le plus précis possible :
- systolique : entre B1 et B2 (perception concomitante du pouls radial) ;
- diastolique : entre B2 et B1 (pas de pouls radial perçu, plus long qu’entre B1 et B2) ;
- proto- : au début ;
- méso- : au milieu ;
- télé- : à la fin ;
- holo- : du début à la fin.
Quelle est l’intensité du souffle ?
À l’auscultation, on peut le quantifier de 1 à 6 (6 étant la plus forte intensité du souffle perçu cliniquement) :
- 1/6 : très faible intensité et souffle difficilement perçu ;
- 2/6 : faible intensité, mais souffle tout de même perçu cliniquement ;
- 3/6 : intensité moyenne à forte, sans frémissement ;
- 4/6 : intensité forte, associée à un frémissement ;
- 5/6 : intensité très forte avec frémissement ;
- 6/6 : intensité maximale : le souffle est perceptible même lorsqu’on décolle son stéthoscope de la paroi thoracique.
Quelles sont les caractéristiques du souffle ?
- Timbre : grave ou aigu.
- Tonalité :
- dur et râpeux (fréquemment rencontré dans les souffles de rétrécissement) ;
- doux, humé et aspiratif (comme c’est plus souvent le cas dans le souffle de régurgitation aortique).
- Variabilité : selon la position du patient (debout, couchée, décubitus latéral, penchée en avant), selon la phase du cycle respiratoire.
________________________________________________________________________________
Caractéristiques d’un souffle « normal »
(sans atteinte valvulaire organique, caractérisée par l’absence d’anomalie morphologique et fonctionnelle)
- Absence de symptôme cardiovasculaire (dyspnée en particulier) ou symptôme aspécifique.
- Intensité de souffle inférieure à 3/6, jamais frémissant.
- Bruits du cœur normaux, en particulier B2, malgré un dédoublement variable physiologique.
- Souffle habituellement court mésosystolique, variant avec la position.
- Absence de déviation du choc de pointe (projection de l’apex cardiaque dans l’aire précordiale) attestant de l’absence de dilatation des massifs cardiaques.
- Examen artériel et pressions artérielles normaux.
________________________________________________________________________________
Examens complémentaires
Interprétation de l’électrocardiogramme
Voir chapitre 6, Électrocardiogramme normal et anormal.
Interprétation d’une radiographie thoracique
« Contenant »
- Arcs costaux.
- Vertèbres.
« Contenu »
- Parenchyme pulmonaire.
- Plèvre et culs-de-sac pleuraux.
- Silhouette médiastinale.
- Silhouette cardiaque.
________________________________________________________________________________
Arcs de la silhouette médiastinale (fig. 4.10)
- Arc supérieur droit : veine cave supérieure ;
- Arc inférieur droit : atrium droit ;
- Arc supérieur gauche : bouton aortique, c’est-à-dire la partie horizontale de la crosse aortique ;
- Arc moyen gauche : tronc de l’artère pulmonaire (pour les deux tiers supérieurs de l’arc) et auricule gauche (tiers inférieur de l’arc) ;
- Arc inférieur gauche : ventricule gauche.
________________________________________________________________________________
Figure 4.10. Correspondance anatomique des différents arcs de la silhouette médiastinale radiologique.
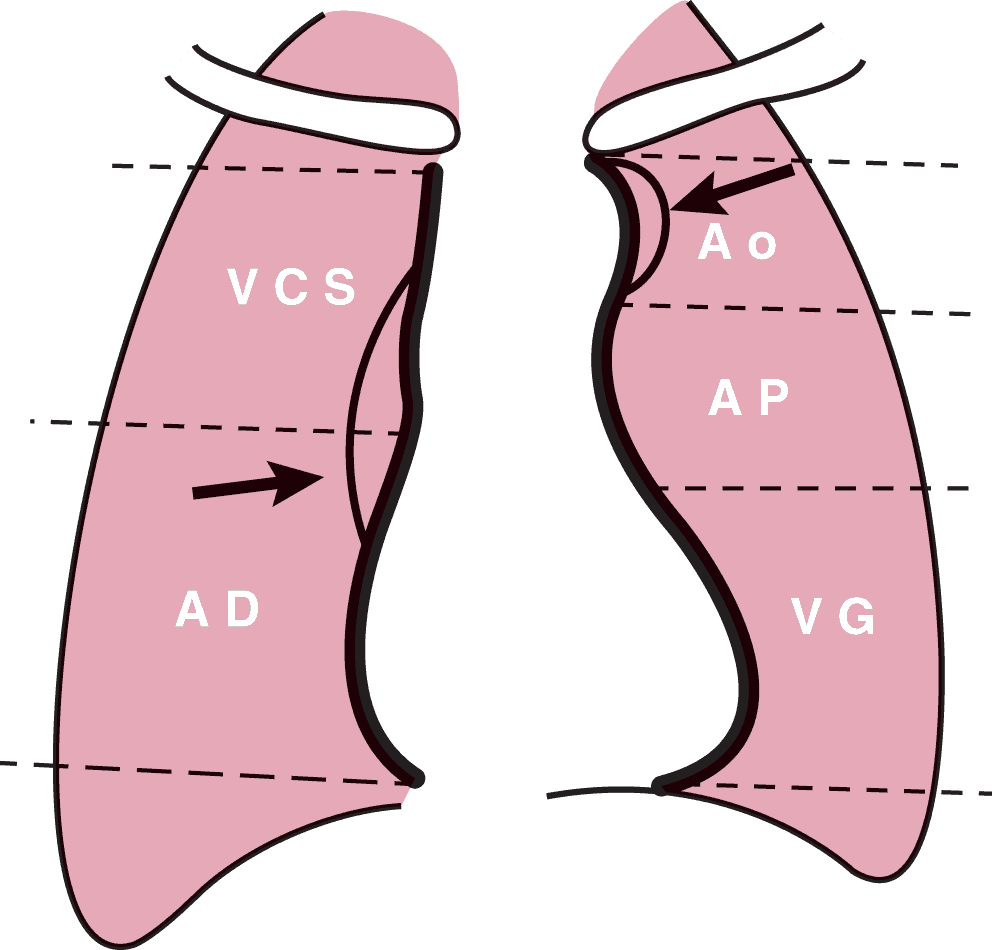
Source : d’après : Sémiologie cardiovasculaire, Collège national des enseignants de cardiologie et maladies vasculaires.
________________________________________________________________________________
Rapport cardiothoracique (fig. 4.11) (RCT)
Rapport de la largeur de la silhouette cardiaque sur la largeur thoracique.
Il est normalement inférieur à 0,5. Lorsque le cœur prend plus de la moitié de la largeur thoracique, on parle de cardiomégalie. Pour bien mesurer cet indice, vu l’asymétrie de la silhouette cardiaque, il convient d’additionner la plus grande largeur de la silhouette cardiaque à la droite de la ligne des épineuses rachidiennes (flèche 1) à la plus grande largeur de la silhouette à gauche de cette même ligne médiane (flèche 2). La somme de ces deux mesures permet d’évaluer avec précision la largeur cardiaque (mesure C) qu’il faut rapporter à la largeur de la cage thoracique (mesure T) afin de trouver le RCT.
RCT=Largeur de la silhouette cardiaqueLargeur thoracique=C/T>0,5
→ Cardiomégalie.
________________________________________________________________________________
Figure 4.11. Mesure du rapport cardiothoracique radiologique (RCT).
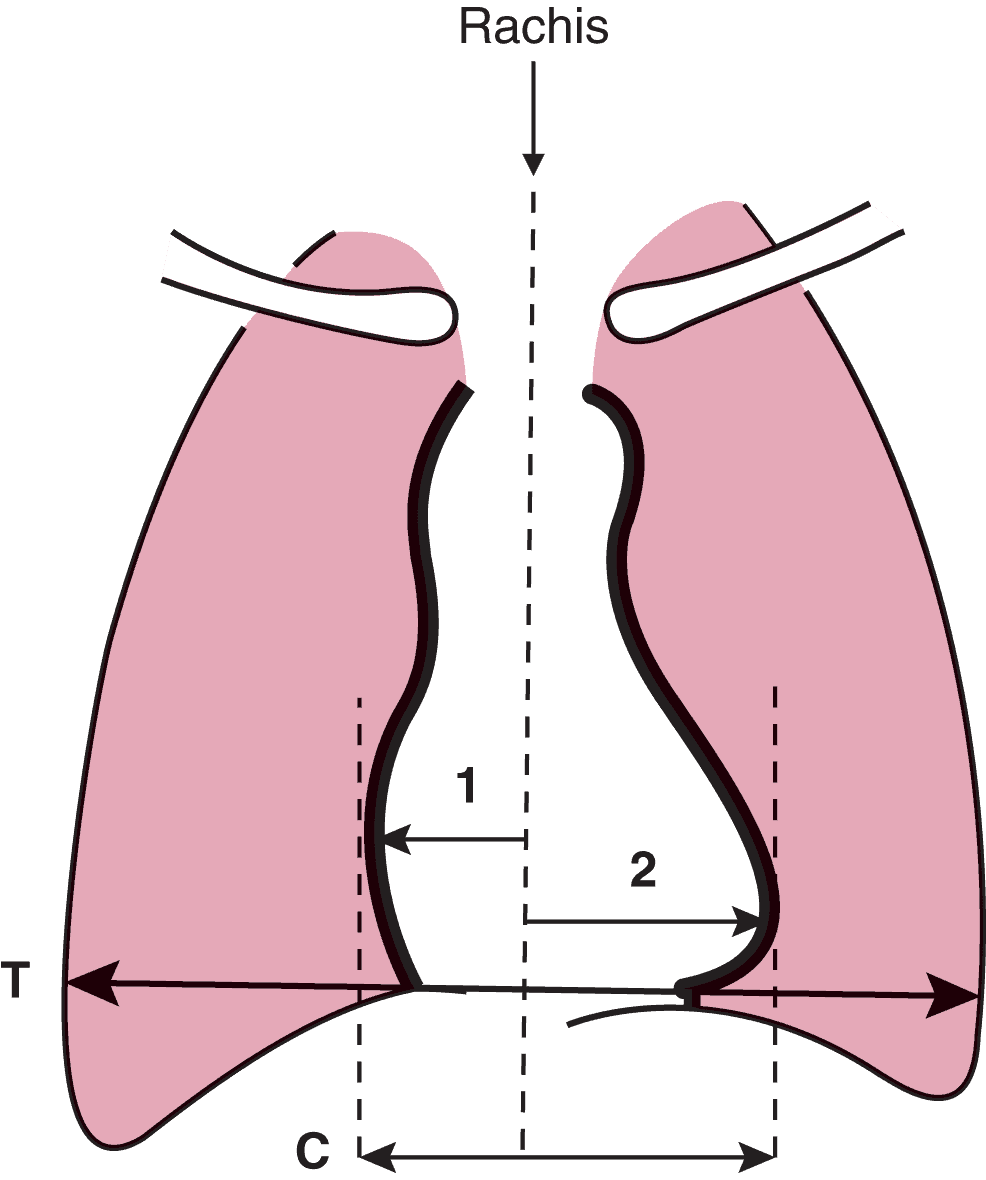
Source : d’après : Sémiologie cardiovasculaire, Collège national des enseignants de cardiologie et maladies vasculaires.
________________________________________________________________________________
Interprétation d’une échocardiographie
Définition et principe
L’échocardiographie est une technique d’imagerie non invasive utilisant les ultrasons. Les ultrasons, émis par la sonde, sont réfléchis de manière plus ou moins intense par les interfaces qu’ils rencontrent. Lorsque l’échographe envoie et reçoit des ultrasons le long d’une ligne ultrasonore (faisceau), une série de points lumineux à des distances variables et d’intensités différentes s’affiche sur l’écran, le long de cette ligne. L’échographie bidimensionnelle est formée de nombreuses lignes consécutives qui forment une image. Pour l’échographie Doppler, lorsqu’une structure se déplace au cours du temps (exemple : un globule rouge), les ultrasons qu’elle renvoie ont une fréquence différente des ultrasons émis par la sonde (effet Doppler). La machine en déduit par des calculs complexes des vélocités de flux sanguins lorsqu’il s’agit de globules rouges ou du myocarde lorsqu’il s’agit des myocytes (Doppler tissulaire). Ces vélocités peuvent être représentées par un « spectre » de vélocités au cours du temps, permettant de calculer des gradients de pression, maximum et moyen, entre deux cavités. Le speckle tracking imaging (ou strain) est une technique plus récente permettant la mesure des trois composantes de la déformation du myocarde : longitudinale, radiale, circonférentielle.
Déroulement d’un examen
L’examen est effectué sur un patient en décubitus latéral gauche, le bras gauche relevé derrière la tête. Plusieurs incidences sont utilisées, afin d’analyser les différentes structures myocardiques : les fenêtres parasternale (permettant d’obtenir les coupes parasternales grand axe et petit axe), apicale (permettant d’obtenir les coupes apicales quatre cavités, deux cavités, trois cavités et cinq cavités), sous-costale et suprasternale.
Principales indications
L’échocardiographie transthoracique (ETT) permet l’analyse des dimensions (dilatation, hypertrophie), de la fonction systolique (FEVG, strain) et diastolique du ventricule gauche, l’analyse de la cinétique segmentaire ventriculaire (recherche d’une hypokinésie, d’une akinésie, d’une dyskinésie dans l’exploration d’une cardiopathie ischémique), l’évaluation des pressions de remplissage du ventricule gauche, l’analyse des dimensions et de la fonction systolique du ventricule droit, la mesure des pressions pulmonaires, l’évaluation des quatre valves (morphologie, fuites, sténoses), l’analyse des oreillettes, du péricarde (épaisseur, épanchement, constriction), de la veine cave inférieure (dimensions), de l’aorte ascendante et de la crosse (dimensions, athérome, dissection).
L’ETT est l’examen clé pour le diagnostic d’une valvulopathie, pour la quantifier, pour décrire l’anatomie valvulaire, évaluer son mécanisme, pour évaluer sa sévérité, son retentissement et son pronostic.
Elle est indiquée chez tout patient porteur d’un souffle cardiaque.
L’échocardiographie transœsophagienne (ETO) est indispensable en cas de suspicion d’endocardite, analyse d’une valvulopathie, recherche de source cardiaque d’embolie, exploration des oreillettes et des auricules (analyse morphologique et fonctionnelle, recherche de contraste spontané préthrombotique, thrombus), exploration de l’aorte thoracique descendante et de la crosse aortique (maladie annulo-ectasiante, dissection aortique, athérome aortique), exploration du septum inter atrial (foramen ovale perméable, anévrysme du septum, communication inter atriale).
Une échocardiographie de stress peut être réalisée à l’effort (sur bicyclette ergonomique ou sur tapis roulant ; voir chapitre 3, Tests d’ischémie couplés à une imagerie) en cas de discordance entre le caractère hémodynamique d’une valvulopathie sténosante ou régurgitante et l’absence de retentissement fonctionnel à l’interrogatoire (patients asymptomatiques) ainsi que dans certaines situations complexes où la part de la dysfonction myocardique et du caractère serré d’une sténose aortique en bas débit se discute (échographie sous perfusion de faibles doses de dobutamine, à dose chronotrope).
________________________________________________________________________________
Évaluation échocardiographique d’un patient ayant une valvulopathie
Imagerie bidimensionnelle, tridimensionnelle et en mode M
Informations anatomiques (géométrie des cavités, anatomie valvulaire et des vaisseaux de la base, péricarde)
- Anatomie valvulaire : surface valvulaire.
- Évaluation qualitative ventriculaire gauche : cinétique segmentaire globale et régionale, fonction systolique globale.
- Évaluation quantitative ventriculaire gauche : dimensions, volume, fonction systolique globale (FEVG), masse ventriculaire gauche, strain (déformation) longitudinal global.
- Évaluation atriale gauche : volume indexé, surface, diamètre.
- Anatomie, structure et fonction ventriculaire droite.
- Complications (thrombose, masse, etc.).
Doppler (modalités : Doppler couleur, pulsé, continu)
Informations hémodynamiques et fonctionnelles
- Hémodynamique non invasive : fonction ventriculaire gauche diastolique (pressions de remplissage ventriculaire gauche), fonction ventriculaire droite, débit cardiaque (débit sous-aortique en règle générale), hémodynamique pulmonaire (pressions pulmonaires, résistances vasculaires pulmonaires), recherche et quantification d’un shunt intracardiaque.
- Mécanisme(s) et quantification d’une sténose valvulaire : vélocité maximale (Doppler continu), gradient maximal et moyen (Doppler continu), surface valvulaire (échocardiographie et Doppler).
- Mécanisme(s) et quantification d’une régurgitation valvulaire : surface de l’orifice régurgitant, diamètre du jet régurgitant à l’origine (vena contracta), volume régurgitant, fraction de régurgitation.
________________________________________________________________________________
Imagerie en coupes (IRM, scanner)
L’échocardiographie transthoracique et l’échocardiographie transœsophagienne sont le plus souvent suffisantes à caractériser le mécanisme et la sévérité de la valvulopathie sténosante ou fuyante.
Dans certaines situations, en particulier la bicuspidie aortique, le scanner cardiaque peut caractériser la sévérité d’une sténose aortique (planimétrie) et mesurer le diamètre de l’anneau aortique. Le scanner coronaire peut compléter l’examen cardiaque, à la recherche de calcifications et de lésions qui seront quantifiées.
L’IRM peut être proposée dans la quantification des valvulopathies régurgitantes. Ses indications sont élargies aux situations complexes dans lesquelles la quantification est difficile en échocardiographie ou lorsque l’apport de l’ETO est insuffisamment contributif.
Exploration hémodynamique et angiographique
Elle comporte trois étapes :
- évaluation des pressions de remplissage et du débit cardiaque ;
- angiographie ventriculaire gauche et angiographie sus-sigmoïdienne ;
- coronarographie.
Technique
Le cathétérisme droit évalue le retentissement d’amont :
- mesure de la pression capillaire pulmonaire (PCAP) ;
- mesure du débit cardiaque (Qc) et de l’index cardiaque (Qc rapporté à la surface corporelle).
Le cathétérisme gauche effectué par voie artérielle rétrograde :
- met en évidence et évalue le gradient systolique entre le ventricule gauche et l’aorte (gradient pic à pic) lorsque l’orifice valvulaire a pu être franchi ;
- mesure la pression télédiastolique du ventricule gauche (PTDVG) ;
- permet d’évaluer la surface aortique fonctionnelle dans la sténose aortique par l’application de la formule de Gorlin.
Angiographies
Avant toute injection d’iode, une contre-indication est systématiquement recherchée (anaphylaxie).
Sont analysés les calcifications et leur mouvement en radiocinéma.
Une ventriculographie gauche en incidence oblique antérieure droite 30° permet :
- la mesure des volumes diastolique, VTD, et systolique, VTS ;
- le calcul de la fraction d’éjection : FEVG = (VTD – VTS)/VTD ;
- la visualisation et la semi-quantification d’une éventuelle fuite mitrale.
Une aortographie sus-sigmoïdienne est systématique en cas de valvulopathie aortique :
- elle évalue la taille de l’aorte initiale (recherche et quantification d’une dilatation) ;
- elle quantifie (semi-quantification) une fuite aortique associée.
Coronarographie
Elle peut justifier à elle seule le cathétérisme gauche. Elle dépiste des lésions coronaires significatives (> 50 % de réduction de diamètre sur un tronc coronaire épicardique).
Indications
Cathétérisme cardiaque gauche
Il n’est discuté que lors d’une évaluation préopératoire (TAVI) chez un patient symptomatique, lorsque l’échocardiographie Doppler met en évidence une sténose aortique hémodynamiquement significative (< 1 cm2).
Le cathétérisme cardiaque complet (idéalement par voie radiale, minimisant le risque de complications artérielles) s’impose dans les cas suivants :
- discordance marquée entre la symptomatologie clinique et les données de l’échocardiographie-Doppler ;
- impossibilité de mesure des paramètres quantifiant la sténose en présence d’une symptomatologie évocatrice ;
- valvulopathie associée : insuffisance mitrale volumineuse, évaluation d’une maladie aortique sévère.
Coronarographie
Elle reste indiquée en préopératoire dans les cas suivants :
- patients âgés de plus de 40 ans et femmes ménopausées ;
- dysfonction systolique ventriculaire gauche (FEVG < 50 %) ;
- patients présentant un angor (examen coronarographique systématique) ou des arguments paracliniques pour une ischémie myocardique ;
- patients présentant des facteurs de risque d’athérosclérose (deux ou plus).
Bases physiopathologiques des traitements et pharmacologie
Traitement médical
Le traitement des valvulopathies est chirurgical. Le traitement médical, régime peu sodé, vasodilatateur et/ou déplétion est indiqué lors des poussées congestives. Le traitement des complications (FA, par exemple) est envisagé dans les chapitres du traitement spécifique.
Traitement chirurgical : généralités
Il se discute lors d’une confrontation médico-chirurgicale (« Heart Team ») et au décours d’un bilan d’opérabilité (voir encadré)
Remplacement valvulaire prothétique chirurgical : généralités
Avant tout remplacement valvulaire, il faut décider plusieurs modalités importantes liées à l’intervention :
- s’il s’agit bien d’un remplacement valvulaire ou d’une simple plastie valvulaire ;
- la valve concernée ;
- le type de valve prothétique utilisé : valve mécanique ou bioprothèse ;
- la voie d’abord : sternotomie ou voie percutanée.
Un bilan lésionnel est indispensable (voir section « Synthèse », en fin de chapitre).
Il est à noter qu’en cas de découverte de lésions coronaires ou vasculaires significatives sur le bilan préopératoire, la séquence de la prise en charge chirurgicale débute généralement par le traitement de ces lésions préalablement (ou de façon concomitante) au remplacement valvulaire prothétique.
Les traitements valvulaires percutanés (TAVI pour le RAC, CMP dans la sténose mitrale, MitraClip dans certaines IM primitives et secondaires, et plus récemment traitement percutané des IT) ont une place croissante dans l’arsenal de la correction d’un vice valvulaire.
La chirurgie conservatrice est privilégiée chaque fois que possible (confrontation écho-chirurgicale) en particulier en cas de régurgitation mitrale et/ou tricuspide fonctionnelle et plus rarement aortique (maladie annulo-ectasiante)
On oppose deux grands types de prothèses, les prothèses mécaniques et les bioprothèses.
Le tableau 4.1 ci-dessous résume les principales caractéristiques des prothèses valvulaires cardiaques.
Modalités thérapeutiques selon le type de valvulopathie et leur étiologie (voir sections spécifiques)
Tableau 4.1. Caractéristiques des différents types de prothèses valvulaires.
| Prothèse mécanique | Bioprothèse (hétérogreffes porcines) | |
| Indications | Patient jeune < 65 ans
Patient déjà sous anticoagulant pour une autre indication (fibrillation atriale, par exemple) Haut risque de dégénérescence d’une bioprothèse (hyperparathyroïdie, par exemple) Désir du patient en faveur d’une prothèse mécanique Éducation possible aux anticoagulants Absence de contre-indications aux anticoagulants |
Patient âgé > 70 ans (comorbidités lourdes)
Présence de contre-indication au traitement anticoagulant Désir de grossesse Désir du patient en faveur d’une bioprothèse |
| Avantages | Durée très prolongée (> 15 ans) (théoriquement, en l’absence de complications) | Bonnes performances hémodynamiques (faible gradient)
Ne nécessite pas la prise d’anticoagulant à vie |
| Inconvénients,
complications |
Endocardite sur prothèse
Désinsertion de prothèse Anticoagulants à vie → complications hémorragiques Risque thrombogène (minimum avec les prothèses St-Jude double ailettes ; thromboses de prothèse et/ou embolies systémiques) Hémolyse Bruits de prothèse perçus parfois gênants dans la vie quotidienne du patient |
Endocardite sur prothèse
Désinsertion de prothèse Durée de la prothèse 8 à 10 ans, parfois au-delà : dégénérescence de prothèse Moins de complications thromboemboliques qu’avec les prothèses mécaniques |
| En pratique | Traitement anticoagulant à vie pour un INR cible = 2,5 (peut varier entre 2 et 3)
Contre-indication aux anticoagulants oraux directs (anti-IIa, anti-Xa) Éducation aux anticoagulants Prévention de l’endocardite infectieuse Port d’une carte |
Traitement anticoagulant pendant 1 à 3 mois postopératoire pour un INR = 2–3 (cible = 2,5) (comme pour une plastie mitrale)
Prévention de l’endocardite infectieuse Port d’une carte |
Synthèse
Voir tableau 4.2.
Tableau 4.2. Principales anomalies rencontrées à l’ETT selon la pathologie valvulaire.
| VG | PRVG | Valves | VD | Aorte | Oreillettes | Péricarde | |
| RA | Normal, hypertrophié ou dilaté, parfois hypokinétique | Normales ou augmentées en cas d’insuffisance cardiaque | – Recherche le mécanisme (bicuspidie, calcifications)
– Quantifie le rétrécissement |
||||
| IM | Normal ou dilaté, parfois hyperkinétique, ou hypokinétique parfois trouble de la cinétique segmentaire (IM par restriction) | Normales ou augmentées en cas d’insuffisance cardiaque | Précision du mécanisme de l’IM (prolapsus, restriction ou destruction valvulaire) Quantification | Rechercher une HTAP | Normale | Oreillette gauche dilatée | Normale |
| IA | Normal ou dilaté, parfois hyperkinétique, parfois hypokinétique | Normales ou augmentées en cas d’insuffisance cardiaque | Précise le mécanisme de l’IA (dilatation annulaire, bicuspidie, hiatus, destruction valvulaire) et la quantifie | Normal | Rechercher un flap intimal, une dilatation de l’aorte | Normale | Normal |
| RA | Normal, hypertrophié ou dilaté, parfois hypokinétique | Normales ou augmentées en cas d’insuffisance cardiaque | – Recherche le mécanisme (bicuspidie, calcifications)
– Quantifie le rétrécissement |
Normal | Normale | Normale | Normal |
| Endocardite
infectieuse |
Normal | Normales ou augmentées en cas d’insuffisance cardiaque | Bilan des valves atteintes, lésions valvulaires (végétation, abcès, perforation) | Rechercher une atteinte tricuspidienne ou pulmonaire
-Sondes de PM |
Normale | Normale | Normal |
| Prothèse
valvulaire |
Normal ou dilaté, parfois hyperkinétique, parfois hypokinétique | Normales ou augmentées en cas d’insuffisance cardiaque | Recherche une dysfonction sténosante (mouvements valvulaires, gradient moyen, surface fonctionnelle), ou fuyante (mécanisme et quantification) | Normal, recherche une HTAP | Normale | Normale ou dilatée | Normal |
| IT | Normal | Normales | Précision du mécanisme de l’IT (fonctionnelle le plus souvent, prolapsus, RAA, carcinoïde) Quantification | Recherche d’une dysfonction systolique VD, d’une dilatation de l’anneau tricuspide.
Préciser le niveau des pressions pulmonaires |
Normale | Oreillette droite dilatée | Normal ou épanchement liquidien en phase de congestion |
| RM | Normal | Non évaluables | -Recherche le mécanisme (rhumatismal)
-Quantifie le rétrécissement, recherche une fuite associée, évalue la possibilité d’une commissurotomie percutanée |
Recherche une HTAP | Normale | Dilatée | Normal |
Rétrécissement (ou sténose) aortique (RA)
La sténose aortique (RA) est à l’origine de l’obstruction progressive de l’éjection VG, aboutissant à une hypertrophie VG et à l’apparition de symptômes d’insuffisance cardiaque, syncope et angor. La sténose valvulaire est la plus fréquente, bien qu’il soit possible qu’une sténose sous aortique ou supra valvulaire puisse être à l’origine d’une gêne à l’éjection VG.
Physiopathologie du rétrécissement aortique (fig. 4.12)
Le rétrécissement (ou sténose) aortique est à l’origine d’un obstacle à l’éjection du sang du ventricule gauche vers l’aorte. Plus le rétrécissement aortique est serré, c’est-à-dire plus la surface d’ouverture de la valve aortique est réduite, plus l’éjection du sang du ventricule gauche dans l’aorte à travers cet orifice est difficile et prolongée, ce qui crée un gradient croissant de pression systolique entre le ventricule gauche et l’aorte. La limitation de l’ouverture valvulaire aortique est donc responsable de l’augmentation de la post-charge. Ce n’est qu’à un stade très avancé que la fonction systolique est altérée, en rapport avec une dilatation tardive du ventricule gauche.
________________________________________________________________________________
Figure 4.12. Schéma de la physiopathologie de la sténose aortique.
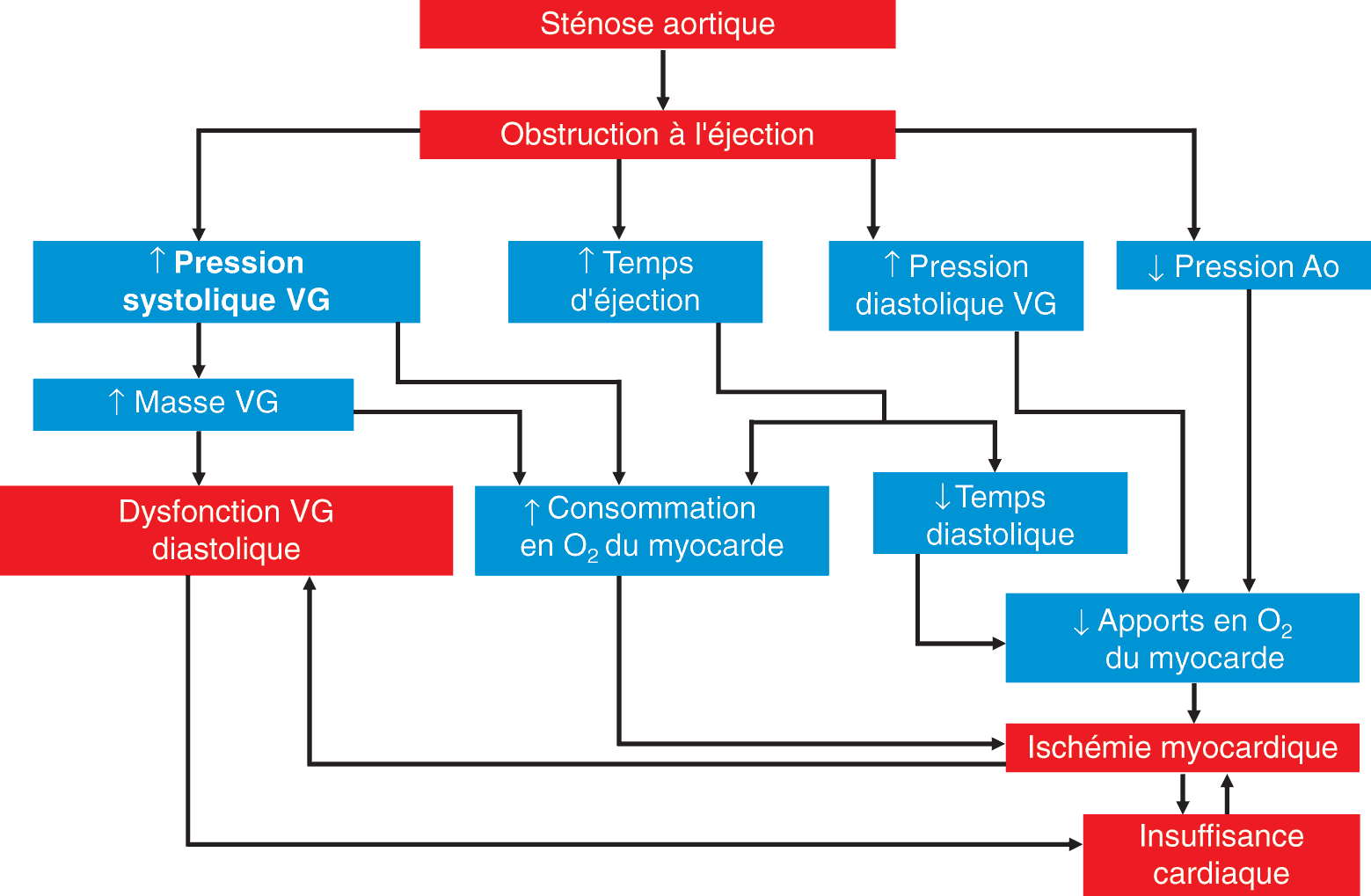
________________________________________________________________________________
Surcharge de pression
Afin de maintenir le débit cardiaque face à une augmentation de la post-charge, le VG doit générer une pression systolique plus élevée, qui augmente la tension pariétale VG. En réponse à cette surcharge de pression et cette augmentation du stress pariétale, le VG développe une hypertrophie concentrique compensatrice. L’augmentation de l’épaisseur pariétale permet initialement une normalisation du stress pariétal, conformément à la loi de Laplace : tension pariétale = (pression × rayon cavitaire)/2 fois l’épaisseur pariétale). Dans certaines situations, le VG ne peut compenser de façon adaptée la surcharge de pression et la dilatation VG ainsi que la dysfonction systolique VG apparaissent alors tardivement.
Dysfonction diastolique
La fonction diastolique VG est déterminée par les propriétés de relaxation du VG et de compliance (une modification de volume est liée à une modification de pression, dV/dP). Une augmentation de la post-charge et l’hypertrophie VG conduit à une réduction de la compliance VG. Les modifications de strain (déformation myocardique dans les trois directions de l’espace) et des caractéristiques de torsion du VG sont décrites dans la sténose aortique. Le remplissage protodiastolique passif est réduit, et le maintien d’une précharge VG adéquate est alors plus dépendant de la contraction atriale, phénomène actif, dont la perte (FA) précipite l’évolution vers l’insuffisance cardiaque.
Discordance apports/besoins en oxygène myocardique
La consommation en oxygène myocardique est déterminée par la FC, la contractilité et la contrainte pariétale myocardique qui est imposée au VG par une augmentation progressive de la surcharge de pression VG. À mesure que la sténose aortique évolue, la contrainte pariétale et la consommation en oxygène du myocarde augmentent parallèlement. La sténose aortique est associée avec une réduction des apports en oxygène aux cellules myocardiques. L’hypertrophie VG progressive et la dysfonction diastolique conduisent à une élévation de la pression télédiastolique du VG, qui conduit à une réduction de la pression de perfusion dans le lit coronaire, à l’origine d’une compression endothéliale des artères intra-myocardiques de petit calibre, altérant alors la réserve coronaire (vasodilatation coronaire avec adaptation à la perfusion coronaire). La discordance entre les apports et la consommation en oxygène myocardique peut précipiter des phénomènes ischémiques à l’effort, en l’absence de lésion coronaire significative des troncs épicardiques.
Causes du rétrécissement aortique
Maladie de Mönckeberg
Il s’agit de la première cause de sténose aortique après 70 ans. La maladie de Mönckeberg est également appelée rétrécissement aortique dégénératif (en opposition à la bicuspidie, qui est un rétrécissement aortique congénital). La valve aortique s’épaissit et se rigidifie (calcifications touchant à la fois les feuillets valvulaires et l’anneau aortique). Les calcifications valvulaires s’étendent progressivement et peuvent se recouvrir de dépôts fibrineux, ou thrombotiques. Elles peuvent aussi s’étendre au septum interventriculaire, avec un risque accru de troubles de la conduction, intra- ou auriculo-ventriculaire. Anciennement, l’apparition de calcifications valvulaires, sur la valve aortique notamment, s’expliquait principalement par des phénomènes dégénératifs passifs. Cependant, les théories actuelles font appel à des phénomènes actifs inflammatoires chroniques, rappelant ceux de l’athérosclérose. Ainsi, les patients présentant déjà de l’athérosclérose, des facteurs de risque d’athérosclérose (HTA, tabac, diabète, syndrome métabolique) ou une insuffisance rénale chronique développent préférentiellement ces lésions. En effet, l’analyse anatomopathologique des valves calcifiées met en évidence des lésions semblables à celles décrites dans l’athérosclérose : dysfonction de la couche endothéliale de la face aortique des sigmoïdes, migration sous-endothéliale de lymphocytes T et de macrophages qui s’activent en macrophages spumeux par accumulation de LDL-cholestérol oxydé, et début d’une formation calcaire par les myofibroblastes valvulaires qui se différencient en ostéoblastes (fig. 4.13). On remarque qu’habituellement cette calcification épargne les commissures valvulaires. Ces mécanismes expliquent l’épaississement et la rigidité de la couche. La calcification peut s’étendre progressivement jusqu’à toucher le septum interventriculaire, l’anneau mitral ou même la valve mitrale (sténose mitrale dégénérative). Il faut également ajouter la notion que ces calcifications valvulaires surviennent fréquemment sur une valve déjà pathologique pour une autre raison (par exemple, calcification sur valve rhumatismale ou sur bicuspidie).
________________________________________________________________________________
Figure 4.13. Physiopathologie de la formation des calcifications valvulaires aortiques.
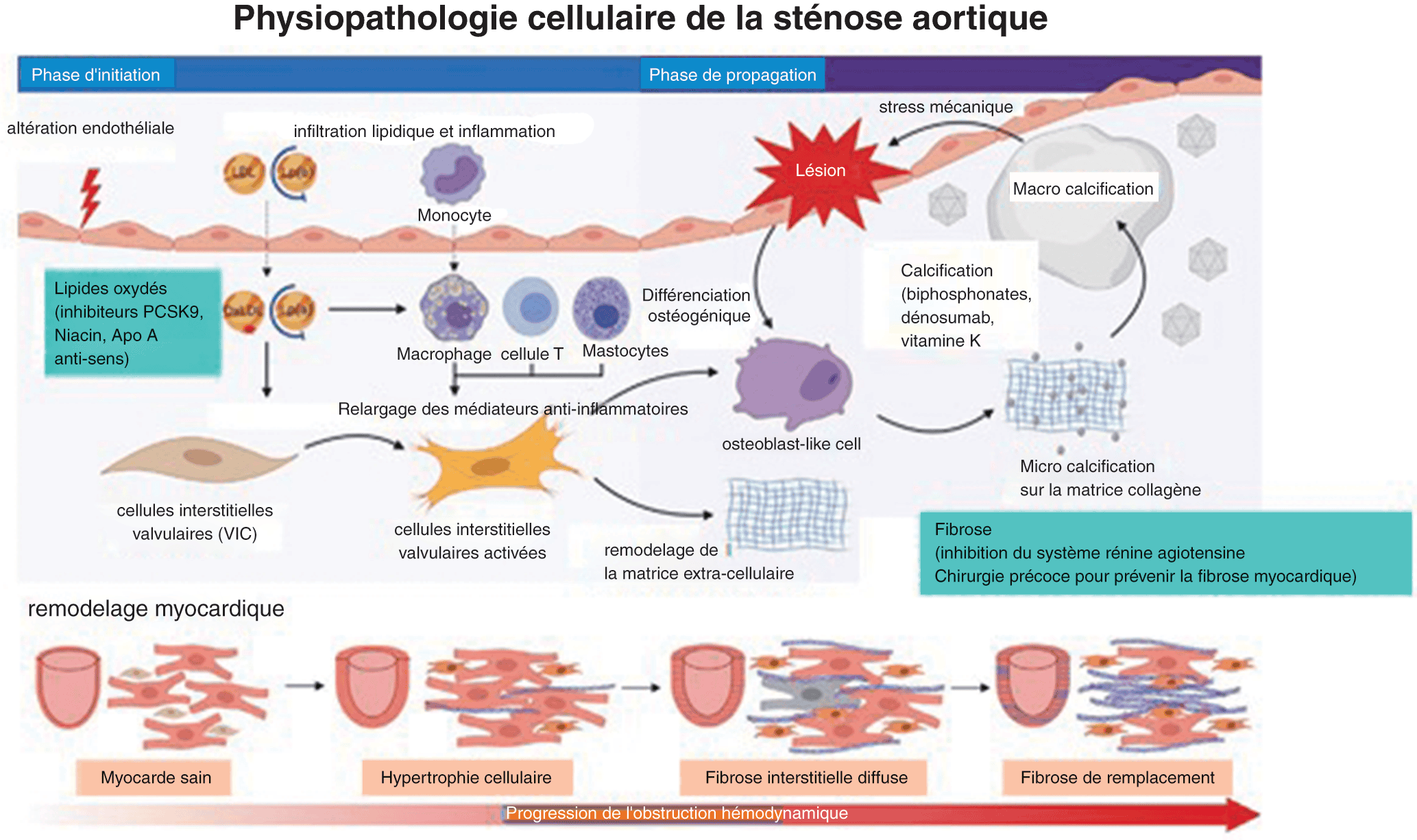
Phase d’initiation : L’évènement initiateur de la sténose aortique est une atteinte de l’endothélium valvulaire due à un stress mécanique ou à d’autres facteurs de risque. Les LDL et la Lpa s’accumulent et infiltrent la couche sous endothéliale ce qui aboutit à une modification de l’oxydation, à l’origine d’une réponse inflammatoire chronique qui implique le recrutement de macrophages, de cellules T et de mastocytes, conduisant à une activation des cellules interstitielles valvulaires (VIC).
Phase de propagation : Les cellules interstitielles valvulaires (VIC) produisent une altération du collagène à l’origine d’une fibrose et à une progression de l’épaississement et la rigidification des feuillets valvulaires. Inhibition de système rénine angiotensine pourrait d’ailleurs avoir des effets anti-fibrotiques. Il est possible que la chirurgie précoce puisse prévenir la fibrose médio pariétale. Les cellules ostéoblastes-like produisent des vésicules extra-cellulaires calcifiantes. La calcification valvulaire aboutit à une discordance (mismatch) avec altération de la compliance, aboutissant à une augmentation du stress mécanique, de l’altération valvulaire, avec phénomènes apoptotiques et activation des ostéoblastes, qui déclenchent une accélération du phénomène de calcification, aboutissant à un cercle vicieux.
Source : d’après Rajamannan, Calcific aortic valve disease: not simply a degenerative process: A review and agenda for research from the National Heart and Lung and Blood Institute Aortic Stenosis Working Group. Executive summary: Calcific aortic valve disease-2011 update. NM. Circulation 2011, 124 : 1783-1791.
________________________________________________________________________________
Bicuspidie aortique
Définition
Il s’agit d’une anomalie congénitale touchant la valve aortique, dans laquelle la valve aortique ne possède plus que deux valvules sigmoïdes au lieu de trois : on distingue un feuillet antérieur et un feuillet postérieur. Sa présence est observée chez 10 % des relations de premier lien familial, justifiant donc la recherche par échocardiographie d’une atteinte valvulaire dans ces situations.
La cusp ou sigmoïde présente habituellement un raphé médian fibreux, sorte d’indentation du feuillet valvulaire, qui sera secondairement le siège de calcifications s’étendant ensuite progressivement sur le reste de la surface des cusps ou feuillets sigmoïdiens. L’anomalie la plus fréquente de la bicuspidie est la fusion des cusps coronaires droite et gauche, (80 % des cas) ; la fusion des cusps droite et non coronaire est observée dans 19 % des cas, et la fusion cusp gauche et cusp non coronaire est plus exceptionnelle.
L’association à une dilatation de l’aorte thoracique est notée dans 50 % des cas, tandis que la coarctation, la dissection aortique et les anomalies coronaires sont observées dans une minorité de cas, mais doivent être recherchées. Elle touche typiquement l’anneau aortique, les sinus, ainsi que le segment proximal de l’aorte ascendante. En cas d’indication chirurgicale, 30 % des patients porteurs d’une bicuspidie aortique nécessitent un geste sur l’aorte thoracique.
Épidémiologie
Première cause de rétrécissement aortique avant 70 ans (50 % des rétrécissements aortiques chez les patients âgés de moins de 70 ans), la bicuspidie aortique ne représente plus que 30 % des causes de rétrécissement aortique au-delà de 75 ans.
Chez les enfants, la bicuspidie aortique est la première cause de sténose aortique et est rapportée dans 80 à 95 % des cas de rétrécissements aortiques.
La bicuspidie aortique est la pathologie congénitale cardiaque la plus commune, affectant 0,5 à 2 % de la population ; cette pathologie est trois fois plus fréquente chez les hommes.
La bicuspidie aortique peut être responsable de dysfonction valvulaire (rétrécissement aortique plus souvent qu’insuffisance aortique), d’une dilatation de l’aorte thoracique et être compliquée d’une endocardite infectieuse.
Histoire naturelle
L’évolution de la bicuspidie aortique est la calcification valvulaire, entraînant un rétrécissement aortique. La bicuspidie aortique, par un défaut de fermeture centrale, peut être responsable d’insuffisance valvulaire. En effet, 15 à 20 % des bicuspidies aortiques ont une fermeture incomplète. Parfois, ces dernières sont la cause d’une maladie aortique, association équilibrée d’un rétrécissement et d’une régurgitation aortiques.
Particularités cliniques
Les bicuspidies peuvent être isolées ou bien associées à d’autres pathologies cardiovasculaires congénitales. L’association la plus fréquente est la coarctation de l’aorte (rétrécissement congénital de l’aorte thoracique descendante) : 75 % des patients avec une coarctation de l’aorte ont une bicuspidie aortique.
De plus, les patients ayant une bicuspidie ont plus de risque de présenter des dilatations de l’aorte thoracique ascendante ainsi que des anévrysmes artériels. Ils sont donc à risque accru de dissection aortique (risque relatif multiplié par 9 pour les dissections de l’aorte ascendante).
Rhumatisme articulaire aigu (RAA)
Les valves sont déformées, rétractées, épaissies, et leur fermeture de même que leur ouverture peuvent en être altérées. Ainsi, on décrit des régurgitations tout comme des rétrécissements aortiques par fusion des commissures, faisant qu’une valve rhumatismale aortique peut être prise à tort pour une valve bicuspide. La valve aortique rhumatismale finit elle aussi par se recouvrir de dépôts calcaires. Ce type d’anomalies peut également s’observer sur la valve mitrale. Le rhumatisme articulaire aigu (RAA) est une complication secondaire à une infection au streptocoque du groupe A (angine ou érysipèle). La prévalence de cette pathologie est surtout importante dans les pays émergents et chez les sujets jeunes.
Le mécanisme des valvulopathies compliquant un RAA n’est pas encore parfaitement établi, mais relèverait d’un phénomène immunologique et non septique : après une infection par streptocoques du groupe A, le système immunitaire développerait des anticorps dirigés contre un antigène de la toxine streptococcique. Or, au sein des valves cardiaques, un antigène partagerait des caractéristiques morphologiques similaires à celles de l’antigène streptococcique, ce qui entraînerait une réaction auto-immune dirigée contre l’endocarde.
________________________________________________________________________________
Valvulopathies rhumatismales
Dans l’étiologie rhumatismale des valvulopathies, l’association de plusieurs valvulopathies est fréquente.
Épidémiologie
Surtout fréquent dans les pays en voie de développement et chez les sujets jeunes, plus rarement observé en Europe.
Terrain
Sujet jeune, vivant dans un pays en voie de développement, présentant des facteurs de risque de RAA : antécédents personnels ou familiaux de RAA, voyages en zone d’endémie, infections multiples à streptocoque du groupe A (angine notamment), facteurs socio-économiques défavorables.
Particularités anatomiques
Épaississement et rétraction des feuillets valvulaires, fusion commissurale en cas de sténose mitrale (spécifique), calcifications plus ou moins étendues.
Particularités cliniques
Les autres complications post-streptococciques sont la chorée de Sydenham, la glomérulonéphrite aiguë, l’érythème noueux, le choc septique post-streptococcique et la scarlatine.
________________________________________________________________________________
Sténoses aortiques non valvulaires (congénitales)
________________________________________________________________________________
Sténoses valvulaires aortiques congénitales
Sténose aortique supravalvulaire
Cette cardiopathie congénitale peut ne pas être diagnostiquée à la naissance. Il s’agit typiquement d’une membrane fibromusculaire circonférentielle touchant le feuillet mitral antérieur et gênant l’éjection aortique. Dans des cas plus rares, une obstruction tunnelaire peut être décrite, plutôt qu’une membrane sous valvulaire. La pathogénie est imparfaitement connue, mais il pourrait s’agir d’une réponse inadaptée à la dynamique du flux à travers de la chambre de chasse VG. Elle peut être associée à d’autres lésions obstructives telles qu’une coarctation aortique. Cette pathologie peut récidiver, y compris après une résection initialement efficace de cette membrane. La sténose aortique sous valvulaire peut être difficile à distinguer d’une cardiomyopathie hypertrophique, en particulier lorsque l’HVG secondaire à la sténose sous aortique est marquée.
Sténose aortique supravalvulaire ou asymétrique
Cette cardiopathie congénitale est rare et peut survenir dans un contexte syndromique tel que le syndrome de Williams dans lequel une mutation du gène à l’élastine a été décrite. Les traits caractéristiques d’un syndrome de Williams incluent hypercalcémie, faciès d’elfe, retard au développement staturo-pondéral et sténoses multiples de l’aorte et des artères périphériques.
________________________________________________________________________________
Sémiologie du rétrécissement aortique
Signes fonctionnels
Les patients sont le plus souvent asymptomatiques. Lorsque le rétrécissement aortique devient serré (ce qui correspond à une surface aortique < 1 cm2, cf. infra, Examens complémentaires), les signes fonctionnels apparaissent : à l’effort dans un premier temps, puis au repos. On peut décrire trois principaux signes fonctionnels : dyspnée, angor, syncope.
Dyspnée
Son mécanisme est lié à l’altération de l fonction diastolique ventriculaire gauche, responsable d’une élévation de la pression dans les capillaires pulmonaires. L’insuffisance ventriculaire gauche peut être aggravée par la présence d’une ischémie myocardique ou d’une atteinte valvulaire mitrale associée.
Angor
C’est une douleur thoracique rétrosternale constrictive par inadaptation de débit coronaire. Il peut s’agir d’un angor fonctionnel, c’est-à-dire survenant sur un réseau coronaire épicardique sain. Deux mécanismes peuvent expliquer cet angor fonctionnel :
- le muscle cardiaque étant hypertrophié, sa consommation en O2 est augmentée ; or le débit cardiaque ne peut pas s’adapter à cette demande accrue : l’ischémie myocardique est donc secondaire à l’insuffisance de la réserve coronaire (fig. 4.12).
- le remplissage des artères coronaires lors de la diastole se fait moins bien lorsque le muscle cardiaque est hypertrophié : en effet, la partie distale des artères coronaires chemine à l’intérieur même du myocarde et non en superficie, c’est cette portion des coronaires dont le remplissage est limité par l’hypertrophie ventriculaire gauche (hypertrophie myocardique qui peut comprimer les artères coronaires).
Dans plus de la moitié des cas, il s’associe un angor par lésions coronaires épicardiques associées (le terrain – sujet âgé – des rétrécissements aortiques dégénératifs est aussi celui des coronaropathies). Il n’est pas possible de distinguer, sur des critères cliniques, le caractère organique ou fonctionnel d’un angor. Le contexte de survenue et les facteurs de risque vasculaire ou une autre localisation athéroscléreuse peuvent orienter le diagnostic.
Syncope
La syncope évocatrice d’un rétrécissement aortique survient typiquement à l’effort. Chez tout patient se plaignant de syncope (à l’effort ou au repos) et ayant un rétrécissement aortique, on doit, cependant, rechercher certaines causes :
- troubles de la conduction : bloc atrioventriculaire car les calcifications de la valve aortique peuvent s’étendre le long du septum interventriculaire, altérant la conduction atrioventriculaire dans le faisceau de His qui est localisé dans le septum interventriculaire ;
- troubles du rythme (tachycardie rapide atriale ou ventriculaire), favorisés par l’hypertrophie myocardique ;
- bas débit cardiaque ;
- iatrogénie : les traitements vasodilatateurs (dérivés nitrés, IEC, etc.) aggravent le gradient de pression systolique ventricule gauche-aorte.
Souffle de rétrécissement aortique (fig. 4.9)
- Foyer : souffle au foyer aortique, irradiant dans les carotides et le long du bord gauche du sternum.
- Temps : mésosystolique (débute après B1, finit avec B2), de forme losangique.
- Caractéristiques :
- rude, râpeux ;
- plus le rétrécissement aortique est serré, plus le souffle est intense et tardif au cours de la systole ;
- il est renforcé après des diastoles longues ou après une extrasystole ventriculaire.
Signes physiques associés
- Pincement de la pression artérielle.
- Galop B4 ou galop présystolique : avant B1, il traduit la perte de la distensibilité ventriculaire secondaire à l’hypertrophie ventriculaire gauche (non spécifique du rétrécissement aortique), au moment de la systole atriale (télédiastole). Le flux, en télédiastole via la systole atriale, de l’oreillette vers le ventriculaire, se heurte à une surcharge de volume et de pression liée à la faible distensibilité ventriculaire.
- Déviation du choc apexien vers le bas et la gauche.
Signes de gravité
Les critères de rétrécissement aortique serré doivent être recherchés à chaque étape de la prise en charge, lors de l’interrogatoire (signes fonctionnels), de l’examen physique (auscultation), et des examens complémentaires (cf. infra, critères de rétrécissement aortique serré à l’échocardiographie Doppler transthoracique) :
- signes fonctionnels : il faut retenir que tout rétrécissement aortique symptomatique est a priori serré (l’inverse n’étant, cependant, pas systématique : un rétrécissement aortique serré peut être asymptomatique) ;
- signes physiques : abolition du B2 à l’auscultation cardiaque, plus rarement dédoublement du B2 à la base. L’abolition du B2 s’explique par la présence de cusps très calcifiées, très peu mobiles, proches l’une de l’autre en systole. Dans ces conditions, leur fermeture en diastole ne produit plus de claquement.
- échocardiographie transthoracique :
- surface aortique < 1 cm2 ou 0,6 cm2/m2 de surface indexée à la surface corporelle ;
- gradient de pression moyen ventricule gauche-aorte > 40 mmHg (élévation du gradient parfois absente en cas de dysfonction ventriculaire gauche systolique avec diminution de la fraction d’éjection ventriculaire gauche) ;
- vitesse maximale transvalvulaire aortique > 4 m/s (correspondant à un gradient maximum instantané, selon l’équation de Bernoulli simplifiée, ΔP = 4 V2 = 4 × (4)2 = 64 mmHg).
Le retentissement sur la géométrie (remodelage ou hypertrophie myocardique) et la fonction cardiaque (FEVG, strain ou déformation myocardique dans l’axe longitudinal) sont variables.
Examens complémentaires
ECG
ECG normal le plus souvent ; on doit, cependant, rechercher :
- une hypertrophie ventriculaire gauche systolique à l’ECG : troubles de la repolarisation avec ondes T négatives dans les dérivations précordiales gauches, indice de Sokolow élevé (S en V1/V2 + R en V5/V6 > 35 mm) ;
- une hypertrophie atriale gauche (Onde P bifide > 120 ms, en DII).
Radiographie thoracique
- Dilatation possible de l’aorte ascendante.
- ± Cardiomégalie.
- Possibles calcifications radio-opaques de la valve aortique.
Échocardiographie Doppler transthoracique
Diagnostic positif
Défaut d’ouverture valvulaire aortique en imagerie bidimensionnelle ou en échocardiographie tridimensionnelle en temps réel (bicuspidie aortique) — en l’absence de calcifications valvulaires ou commissurales trop importantes.
Diagnostic de gravité
- Quantification du rétrécissement aortique :
- calcul de la surface aortique < 1 cm2 non indexée ou 0,6 cm2/m2 de surface indexée à la surface corporelle ;
- planimétrie de la surface aortique anatomique (difficile et imprécise en cas de calcifications valvulaires) : la voie transœsophagienne est plus précise que la voie transthoracique ;
- gradient de pression ventricule gauche-aorte systolique moyen > 40 mmHg (élévation du gradient parfois absente en cas de dysfonction systolique) ;
- vitesse maximale transvalvulaire > 4 m/s (sténose aortique critique si > 5,5 m/s).
- Retentissement et tolérance :
- FEVG et fonction diastolique ventriculaire gauche (pressions de remplissage ventriculaire gauche) ;
- hypertrophie ventriculaire gauche concentrique ;
- hypertension pulmonaire.
Diagnostic étiologique
- Calcifications de la valve aortique.
- Bicuspidie.
- Recherche d’une valvulopathie associée (insuffisance aortique fréquemment associée, rétrécissement mitral si valvulopathie rhumatismale).
- Recherche d’une dilatation de l’aorte thoracique (recherche de bicuspidie).
Histoire naturelle
Sténose aortique des patients asymptomatiques
La progression de la sténose aortique est caractérisée par une phase latente prolongée, période pendant laquelle le patient est asymptomatique. Cette période est associée à une survie normale. Le risque de mort subite chez un patient asymptomatique porteur d’une sténose aortique critique est < 2 %/an. Il faut, cependant, noter la variabilité individuelle importante dans la durée de cette période latente, ainsi que sur l’évolution des paramètres hémodynamiques caractérisant la sténose aortique. En règle générale, les patients asymptomatiques porteurs d’une sténose aortique connaissent une progression évaluée à 7 mmHg/an, une vélocité transvalvulaire maximale qui augmente de 0,1 à 0,3 m/s et par année et une surface aortique valvulaire qui diminue de 0,1 cm2/an. Du fait du caractère variable de la progression de la maladie, tous les patients porteurs d’une sténose aortique doivent être informés de la nécessité de rapporter tout symptôme survenant à l’effort, impliquant alors une évaluation par échocardiographie doppler. Dans les formes asymptomatiques, en cas de sténose aortique hémodynamiquement significative définie par une vélocité maximale transvalvulaire > à 4 m/s, la probabilité de développement de symptôme ou la nécessité d’un remplacement valvulaire aortique augmente dans les deux années qui suivent le diagnostic, conformément au schéma décrit par Braunwald (fig. 4.14).
________________________________________________________________________________
Figure 4.14. Évaluation du pronostic d’une sténose aortique en fonction de son âge de découverte et de l’apparition de symptômes.
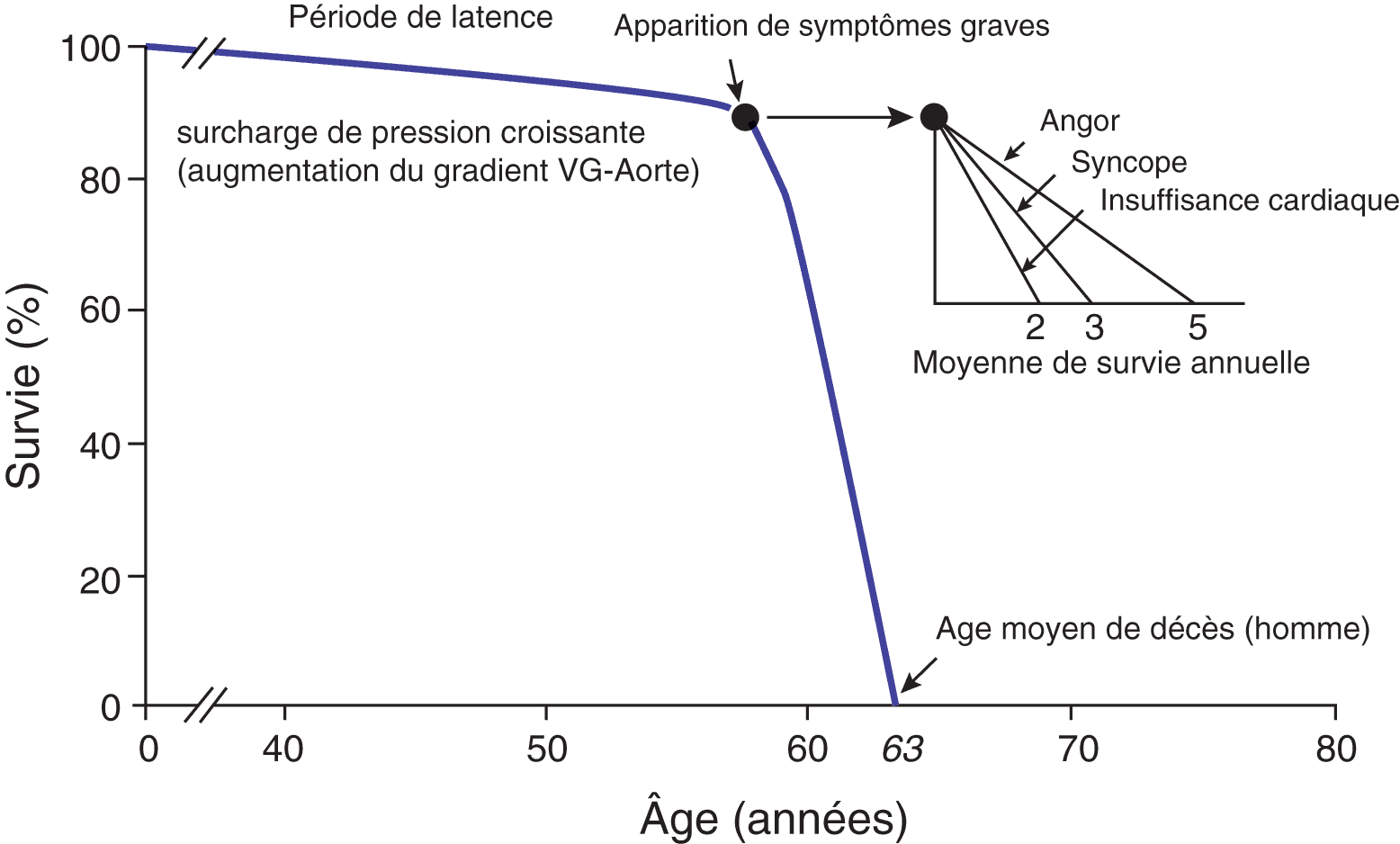
Source : Baumgartner H. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Europ Heart J 2017; 38: 2739–2791.
________________________________________________________________________________
Sténose aortique des patients symptomatiques
Ces patients développant un angor ont une survie à 5 ans de 50 %. En cas de syncope, la survie à 3 ans est de 50 %, et en cas d’apparition de signes d’insuffisance cardiaque, la durée moyenne de survie est < à 2 ans, en cas de traitement médical seul.
En cas de sténose aortique sévère symptomatique, le risque de mort subite est accru en cas d’hypotension artérielle ou d’arythmie ventriculaire liées à l’ischémie, l’HVG ou à l’altération de la fonction VG. À noter que les symptômes de la sténose aortique sévère sont parfois difficiles à reconnaître chez les patients qui ont adapté leur mode de vie à leur symptomatologie, nécessitant donc une évaluation précise par interrogatoire à la recherche d’un retentissement clinique ou hémodynamique dans le contexte d’une sténose aortique asymptomatique.
Traitement du rétrécissement aortique (fig. 4.15)
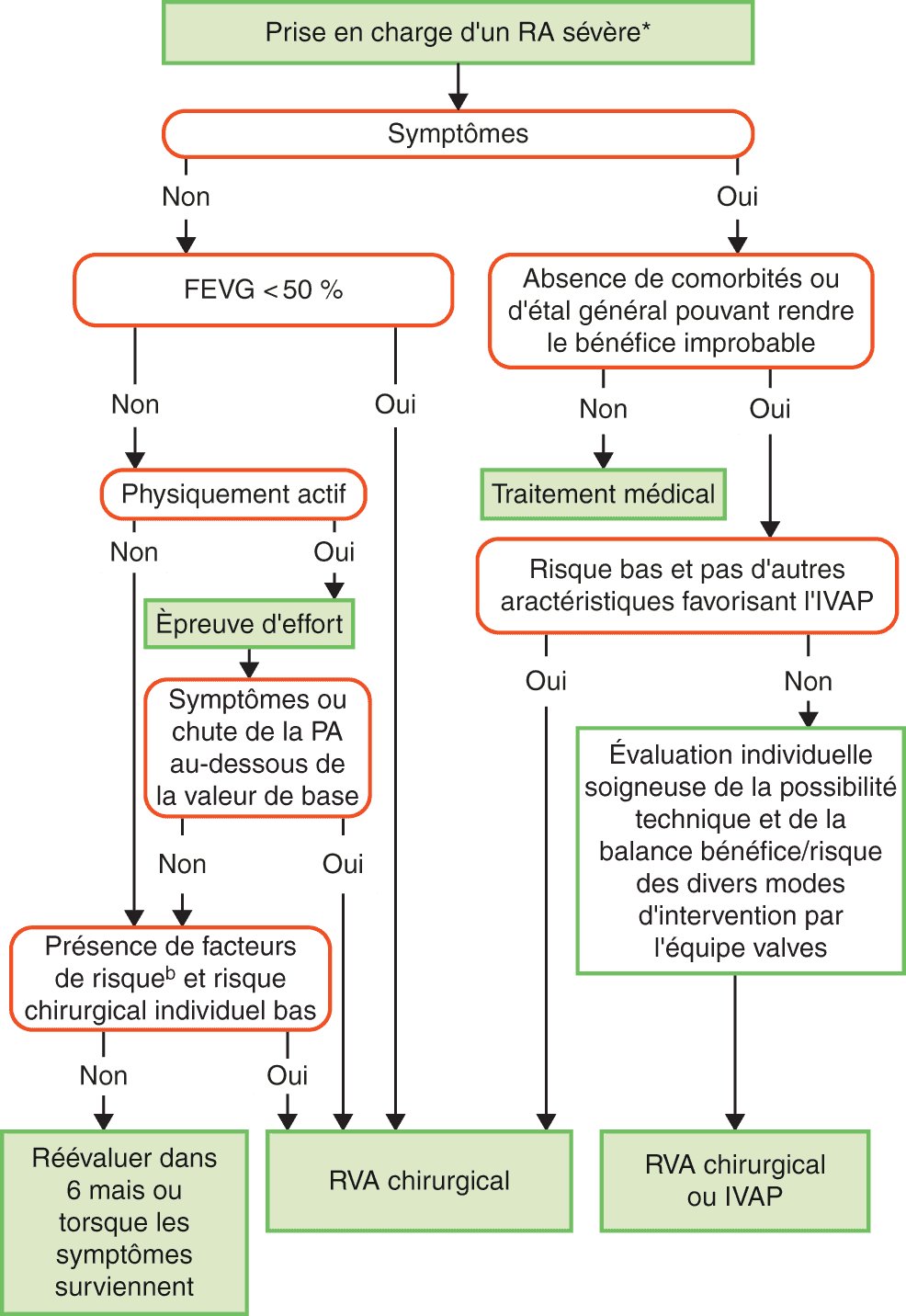
Le remplacement valvulaire aortique chirurgical reste le traitement de première intention dans le rétrécissement aortique. L’alternative plus récente qu’est l’implantation d’une valve aortique par voie percutanée (TAVI ou transcatheter aortic valve implantation) prend, néanmoins, de plus en plus de place et ses indications, initialement les sujets avec une contre-indication à la chirurgie, est élargie aux patients à risque chirurgical élevé et intermédiaire. Des données récentes (PARTNER 3 et EVOLUT) ont apporté des arguments en faveur du TAVI également chez les patients à bas risque chirurgical, et les recommandations des société savantes devraient donc évoluer dans un proche avenir.
________________________________________________________________________________
Figure 4.15. Rétrécissement aortique calcifié : conduite à tenir (recommandations ESC, 2017).
________________________________________________________________________________
Deux scores sont principalement utilisés pour évaluer le niveau de risque opératoire :
- l’EuroSCORE II ;
- le Society of Thoracic Surgeons score (STS).
Modalités
Remplacement valvulaire aortique par prothèse mécanique ou biologique, avec circulation extracorporelle (CEC) ou TAVI.
Indications
- Rétrécissement aortique calcifié serré symptomatique.
- Rétrécissement aortique calcifié serré asymptomatique avec :
- très serré (V max > 5,5 m/s) ;
- RAC d’aggravation rapide lors de la surveillance ;
- en cas d’HVG très importante ;
- en cas d’altération de la FEVG (FEVG < 50 %) ;
- lorsqu’il existe des lésions coronaires justifiant des pontages aorto-coronaires ou des lésions valvulaires associées imposant un geste chirurgical.
Traitement médicamenteux
Médicaments à éviter (ou dont la prescription doit être temporaire et encadrée) :
- digitaliques (risque d’arythmie ventriculaire) ;
- vasodilatateurs artériels et veineux (notamment les dérivés nitrés), qui sont à risque d’hypotension artérielle et qui aggravent le gradient de pression VG-aorte.
Il n’existe pas de traitement médicamenteux spécifique du rétrécissement aortique. Les statines ne modifient pas l’histoire naturelle de la sténose aortique calcifiée et évoluée.
Hygiène de vie
- Éviter les efforts violents et les sports à risque (sport de compétition) ;
- Correction et éducation thérapeutique des facteurs de risque cardiovasculaire associés ;
- Régime pauvre en sel lors des poussées d’insuffisance cardiaque congestive.
Surveillance clinique et échocardiographique
Elle dépend du degré de sténose aortique :
- sténose aortique modérée : surveillance tous les deux ou trois ans ;
- sténose aortique moyenne : surveillance tous les ans ;
- sténose aortique serrée asymptomatique : surveillance tous les six mois.
________________________________________________________________________________
En pratique – Remplacement valvulaire aortique percutané : TAVI
TAVI signifie transcatheter aortic valve implantation (les Anglo-Saxons emploient la terminologie TAVR, transcatheter aortic valve replacement).
Voies d’abord
- Artère fémorale le plus souvent. L’artère subclavière peut également être utilisée (en cas d’athérome fémoral important) et, si la voie fémorale est impossible, les voies trans-apicale (par la pointe du cœur), sous-clavière et parasternale droite sont possibles.
- Deux types de valves aortiques transcutanées peuvent être implantés en France :
- la valve Edwards Sapien 3, en péricarde bovin, montée sur un stent tubulaire en chrome-cobalt, pour laquelle le déploiement requiert une inflation à l’aide d’un ballon (taille 23, 26 et 29 mm), elle est dotée d’une jupette externe qui assure une meilleure étanchéité avec l’anneau ;
- la valve Medtronic CoreValve Evolut R, en péricarde porcin, montée dans une cage auto-expandable en nitinol (alliage nickel-titane à mémoire de forme), récupérable et repositionnable (taille 26, 29, 31/34 mm), sa partie distale élargie la stabilise dans l’aorte ascendante.
Bilan préopératoire
- Le même que celui d’un remplacement valvulaire traditionnel, auquel on ajoute une angio-TDM de l’aorte et de ses branches afin de rechercher de l’athérome sur les parois artérielles, et de mesurer les diamètres artériels afin d’évaluer la faisabilité du cathétérisme artériel rétrograde.
Déroulement de l’intervention
- Au cours d’un cathétérisme artériel rétrograde (fémoral), on place un ballonnet en regard de la valve aortique sténosée. Au cours de la dilatation au ballonnet, la surface de l’orifice aortique augmente progressivement. Puis une bioprothèse est déployée au niveau de la valve aortique.
Indications
- Rétrécissement aortique calcifié serré, plus ou moins symptomatique, chez des patients présentant des contre-indications à la chirurgie de remplacement valvulaire prothétique conventionnel.
- L’indication d’implantation d’une valve aortique percutanée doit être portée par une équipe médicochirurgicale expérimentée et après discussion pluridisciplinaire en staff dédié dans des équipes entraînées (« Heart Team ») constituées de cardiologues interventionnels et médicaux, chirurgiens cardiaques et anesthésistes. La réalisation du TAVI nécessite un centre disposant d’un service de chirurgie cardiaque et des salles avec les spécificités de blocs opératoires.
- Tout rétrécissement aortique serré symptomatique doit bénéficier d’un remplacement valvulaire chirurgical ou percutané compte tenu du risque vital existant et ce, pratiquement sans limite d’âge, sous réserve d’un état général conservé et de l’absence d’une autre pathologie mettant en jeu le pronostic vital à court terme.
Complications
- Accident vasculaire cérébral (1-5 %) et complications emboliques par décollement de plaque d’athérome aortique ou fémorale lors du cathétérisme rétrograde ou lors de l’ouverture de la prothèse sur une valve aortique très calcifiée (AVC, ischémie mésentérique, ischémie aiguë de membre…) dont la prévalence serait élevée, découvertes en particulier lors d’examens d’imagerie effectués systématiquement.
- Implantation d’un pacemaker (de 7 à 40 % selon le type de valve).
- Complications vasculaires (20 %), dominées par les hématomes aux points de ponction. et plus rarement les dissections artérielles.
- Fuite paravalvulaire minime en post-procédure fréquente (> 50 % des cas). Lorsqu’elle supérieure à un grade II (2,5 % à 30 jours avec la Edwards Sapien 3 et 3,4 % à 30 jours avec la Core-Valve Evolut R), elle a un impact sur la survie au long cours.
Taux de mortalité
- À 30 jours varie de 5 à 15 % pour l’approche trans-fémorale, 10 à 20 % pour l’approche trans-apicale.
- À un an, la survie des patients ayant bénéficié d’un TAVI varie de 60 à 80 %.
- À deux ans la survie des patients est estimée à 60 % à 2 ans.
Une amélioration substantielle de l’état clinique et fonctionnel et de la qualité de vie des patients est rapportée. La survie à long terme est largement dépendante des comorbidités. Elle ne semble pas influencée par la durabilité des bioprothèses.
Traitement au décours
Une double anti-agrégation plaquettaire (aspirine 75-100 mg/jour et clopidogrel 75 mg/jour) est recommandée pendant trois mois (absence de preuve de l’efficacité des AOD), suivie d’une mono-anti-agrégation plaquettaire à vie chez les patients ne nécessitant pas de traitement anticoagulant. Une mono-anti-agrégation plaquettaire après TAVI peut être envisagée en cas de haut risque hémorragique élevé. Le traitement anticoagulant par AVK seul est recommandé après un TAVI chez les patients nécessitant un traitement anticoagulant pour une autre indication et n’ayant pas d’indication à un traitement antiagrégant plaquettaire (revascularisation coronaire).
________________________________________________________________________________
Insuffisance mitrale (IM)
Comme dans l’insuffisance aortique, il convient de considérer les formes aiguës et chroniques de façon séparée (encadré pour les IM aiguës, voir ci-dessous).
Physiopathologie de l’insuffisance mitrale chronique
Elle se caractérise par une dilatation VG avec une hypertrophie ventriculaire gauche excentrique. La contrainte pariétale est normalisée avec le développement de l’HVG. La dilatation de l’oreillette gauche peut contribuer à adapter l’augmentation de la précharge à des niveaux de pressions VG de remplissage moindre.
En effet, dans l’insuffisance mitrale, à chaque systole, lorsque la valve mitrale se referme, une partie du volume éjecté dans le ventricule gauche reflue dans l’atrium gauche. Le volume se trouvant dans l’atrium gauche à la fin de la systole est donc le volume arrivant des veines pulmonaires dans l’atrium gauche auquel on additionne le volume régurgité au travers de la valve mitrale incontinente.
Ainsi, dans les insuffisances mitrales chroniques, l’atrium gauche se dilate progressivement, évitant l’augmentation trop rapide de la pression dans l’atrium gauche et donc l’élévation en amont des pressions pulmonaires (insuffisance ventriculaire gauche chronique d’aggravation progressive). Ce mécanisme adaptatif n’a pas le temps de se mettre en place dans les insuffisances mitrales aiguës et l’absence de dilatation de l’atrium gauche explique l’élévation brutale des pressions capillaires pulmonaires, réalisant une scène d’OAP.
Des modifications de la géométrie ventriculaire gauche apparaissent dans les insuffisances mitrales chroniques. La conséquence de l’augmentation du volume présent dans l’atrium gauche est une dilatation ventriculaire gauche par surcharge diastolique (augmentation de la précharge). Lors de la systole, en cas d’insuffisance mitrale, le sang est éjecté du ventricule gauche vers l’atrium gauche sans augmentation de la post-charge, il s’agit d’une fuite mitrale passive.
L’augmentation de la précharge, la post-charge normale ou réduite et l’augmentation de l’activité du système sympathique sont à l’origine d’une accentuation de la contractilité myocardique, contribuant à l’augmentation de la fraction d’éjection VG à la phase initiale (FEVG > 60 %). Le ventricule gauche se dilate progressivement, la FEVG « se normalise » puis une dysfonction systolique (baisse de la FEVG) apparaît secondairement.
À noter que dans l’insuffisance mitrale, la FEVG calculée surestime la réelle FEVG (fraction de sang réellement chassé dans l’aorte), car la FEVG calculée prend en compte la partie de sang éjectée passivement dans l’oreillette gauche via la fuite mitrale.
La dysfonction systolique VG est parallèle à une dilatation cavitaire avec une augmentation de la contrainte pariétale : la dilatation cavitaire et annulaire mitrale contribue de plus à augmenter le volume de l’insuffisance mitrale. La dysfonction contractile VG peut devenir irréversible, soulignant l’importance du choix adapté de la date opératoire pour espérer une réversibilité du remodelage cardiaque.
On classe les insuffisances mitrales selon leur mécanisme en tenant compte de la position des valves lors de la systole ventriculaire (classification anatomo-fonctionnelle de Carpentier) (tableau 4.3).
Tableau 4.3. Classification anatomofonctionnelle de Carpentier des régurgitations mitrales.
| Type I | Type II | Type III (a et b) |
| Mouvements valvulaires normaux | Mouvements valvulaires excessifs | Mouvements valvulaires restreints |
| Perforation valvulaire ou dilatation de l’anneau | Prolapsus valvulaire, rupture de cordages (« flail »)
Rupture de muscle papillaire (IDM, traumatisme) Rupture de cordages (endocardite, idiopathique, etc.) |
IIIa : Restriction systolo-diastolique (IM primitive, organique)
IIIb : Restriction systolique (IM secondaire, fonctionnelle) |
| – Endocardite
– Cardiopathie dilatée (d’origine ischémique ou autre) |
– Maladie de Barlow
– Dégénérescence fibro-élastique |
– Rhumatisme articulaire aigu, valvulopathie toxique, valvulopathie radique (IIIa)
– Cardiopathie dilatée et/ou ischémique (IIIb) |
Causes de l’insuffisance mitrale (tableau 4.4)
________________________________________________________________________________
Causes des insuffisances mitrales
Les causes aiguës sont signalées par un*.
Les mécanismes selon la classification de Carpentier sont indiqués à titre d’information. Ils peuvent être associés.
Atteinte des feuillets valvulaires
- Dégénérescence myxomateuse avec mouvements excessifs des feuillets valvulaires (II, sujet jeune).
- Dégénérescence fibro-élastique (sujet âgé) (II).
- Rhumatisme articulaire aigu (III).
- Endocardite infectieuse (y compris l’atteinte secondaire par lésion de jet de la valve mitrale antérieure) (I).
- Atteinte congénitale : fente valvulaire mitrale, valve à double orifice, cardiomyopathie obstructive.
Anomalies annulaires mitrales
- Dilatation annulaire (I) : secondaire à une dilatation VG, quelle qu’en soit la cause.
- Calcification annulaire mitrale dégénérative, chez le sujet âgé (I).
Anomalies des cordages tendineux
- Rupture de cordages tendineux, en particulier en cas de flail, quelle qu’en soit la cause (idiopathique, infectieuse, traumatique) (II).
Anomalies des muscles papillaires
- Rupture de chef de muscle papillaire dans un contexte d’infarctus du myocarde (II) : totale (muscle papillaire) ou partielle.
- Dysfonction du muscle papillaire : ischémique, en particulier du muscle papillaire postéro médian, vascularisé par une artère postérieure. L’atteinte du muscle papillaire antéro latéral est plus rare, car perfusée par l’IVA et la circonflexe.
- Processus infiltratif, amyloïde ou sarcoïdose.
- Malposition (congénitale), valve mitrale parachute.
________________________________________________________________________________
Tableau 4.4. Caractéristiques différentielles entre maladie de Barlow et dégénérescence fibro-élastique comme causes d’insuffisance mitrale.
| * | Barlow | Dégénérescence fibro-élastique |
| Terrain | Sujets jeunes
(environ 30 ans) |
Sujets plus âgés
(au-delà de 60–70 ans), |
| Prédominance du genre féminin. | Prédominance du genre masculin | |
| Particularités anatomiques | Valve mitrale épaissie
Appareil sous valvulaire fin |
Valve mitrale fine, pellucide, dont les cordages tendineux sont étirés |
| Éversion de tout ou partie des segments valvulaires antérieur et/ou postérieur dans l’atrium gauche en systole | Éversion de tout ou partie du feuillet postérieur le plus souvent atteint. |
Parmi les insuffisances mitrales dégénératives, on distingue la dégénérescence myxoïde appelée la maladie de Barlow, liée à un épaississement des valves mitrales, à l’origine de prolapsus, chez la femme jeune, de la dégénérescence fibro-élastique, à l’origine de ruptures de cordages, chez l’homme âgé.
Sémiologie de l’insuffisance mitrale
Signes fonctionnels
La plupart du temps, l’insuffisance mitrale est asymptomatique. Les signes fonctionnels représentent donc déjà un signe de gravité :
- dyspnée d’effort puis de repos ;
- asthénie (aspécifique).
En cas d’insuffisance mitrale aiguë, un OAP brutal peut être révélateur, succédant parfois à la perception d’un claquement thoracique par le patient (syndrome de rupture de cordage(s)).
Auscultation (fig. 4.9)
- Décubitus latéral gauche.
- Foyer : souffle au foyer mitral.
- Irradiation : aisselle ou sternum, selon la valve (ou feuillet valvulaire) touchée par un prolapsus ou une restriction. L’irradiation du souffle en cas d’IM primaire peut varier selon le feuillet valvulaire atteint. Un prolapsus du feuillet antérieur mitral irradie dans la région axillaire ou vers l’omoplate gauche tandis qu’un prolapsus du feuillet mitral postérieur irradie antérieurement et peut être confondu avec un souffle systolique éjectionnel de sténose aortique.
En cas d’IM secondaire, le souffle est habituellement perçu à l’apex et irradie également dans la région en axillaire.
- Temps : holosystolique.
- Caractéristiques :
- doux, en jet de vapeur ;
- son intensité n’est pas proportionnelle à l’importance du volume de régurgitation. Dans les régurgitations importantes, le souffle est en règle intense. Les manœuvres modifiant le souffle permettent parfois de faire le diagnostic d’insuffisance mitrale par prolapsus ;
- la présence d’un galop protodiastolique ou B3, d’un roulement mésodiastolique et d’un éclat du deuxième bruit au foyer pulmonaire (hypertension artérielle pulmonaire) sont en faveur d’une régurgitation mitrale volumineuse.
- L’auscultation du prolapsus valvulaire mitral associe plusieurs signes inconstants et parfois peu spécifiques :
- click mésosystolique, isolé dans un tiers des cas,
- souffle télésystolique isolé.
L’association pathognomonique click mésosystolique et souffle télésystolique n’est perçue que dans moins d’un tiers des cas. Une fibrillation atriale (FA) rapide peut être présente ce qui peut rendre l’examen clinique plus aléatoire.
Signes associés
- Déviation du choc apexien vers la gauche (lié à la dilatation du ventricule gauche).
- Signes d’insuffisance cardiaque droite : œdèmes des membres inférieurs, turgescence jugulaire, reflux hépatojugulaire.
Signes de gravité
- Signes fonctionnels.
- Insuffisance ventriculaire droite (dysfonction systolique ventriculaire droite, dilatation annulaire tricuspide, HTAP avec retentissement VD).
- Éclat du B2 (HTAP).
Examens complémentaires
ECG
Normal ou hypertrophie atriale gauche, parfois hypertrophie ventriculaire gauche (l’hypertrophie électrique n’est pas systématiquement liée à une véritable hypertrophie morphologique, une dilatation ventriculaire peut parfois entraîner une HVG électrique). La fibrillation atriale est fréquente, en rapport avec la dilatation de l’atrium gauche.
Radiographie thoracique
- « Silhouette mitrale ».
- Accentuation de la convexité de l’arc moyen gauche par dilatation de l’atrium gauche.
- Double contour de l’arc inférieur droit également lié à la dilatation de l’atrium gauche.
- Arc inférieur gauche accentué par dilatation du ventricule gauche.
- Cardiomégalie.
- ± Surcharge pulmonaire.
Échocardiographie des insuffisances mitrales (vidéo 4.5, vidéo 4.6)
Diagnostic positif
Visualisation de la régurgitation mitrale en Doppler couleur.
Diagnostic de gravité (tableau 4.5)
- Quantification de la fuite :
-
- PISA (proximal isovelocity surface area, étude de la zone de convergence) : son évaluation permet de calculer le débit régurgitant, la surface de l’orifice régurgitant (SOR) (insuffisance mitrale importante pour SOR > 40 mm2), le volume régurgité (VR, (insuffisance mitrale importante pour VR > 60 ml)), la fraction de régurgitation (FR > 50 %) ;
- diamètre du jet régurgitant à son origine (vena contracta > 7 mm : insuffisance mitrale volumineuse).
- Retentissement de l’insuffisance mitrale :
-
- retentissement sur l’atrium gauche qui est dilaté (l’importance de la dilatation de l’atrium n’est, cependant, pas proportionnelle à l’importance de la fuite valvulaire, pas plus à son ancienneté et à la présence d’une FA) ;
- retentissement sur le ventricule gauche : dans l’insuffisance mitrale chronique, le ventricule gauche finit par se dilater ; la diminution de la FEVG et de la fraction de raccourcissement du ventricule gauche témoigne d’un retentissement myocardique débutant lié à l’insuffisance mitrale ; la détection plus précoce de l’altération de la fonction myocardique VG est accessible par la mesure du strain longitudinal global qui est altéré alors même que la FEVG peut rester longtemps normale.
- retentissement sur les cavités droites, HTAP, dilatation ventriculaire droite, dilatation annulaire tricuspide et ses conséquences (insuffisance tricuspide, signes cliniques d’insuffisance cardiaque droite).
Tableau 4.5. Comparaison des caractéristiques des insuffisances mitrales chroniques compensées et aiguës.
| Caractéristiques | Insuffisance mitrale chronique importante (compensée) | Insuffisance mitrale aiguë |
| Cause | ||
| Anomalie vasculaire, de l’appareil sous-valvulaire et/ou de l’anneau mitral | Anomalie vasculaire, de l’appareil sous-valvulaire, myocardique et/ou de l’anneau mitral (endocardite infectieuse, rupture de cordages, rupture de pilier postérieur) | |
| Physiopathologie | ||
| Volume VG | Augmenté | Normal |
| Volume AG | Augmenté | Normal |
| Pressions pulmonaires | Normales ou augmentées (effort) | Augmentées |
Diagnostic étiologique
L’échocardiographie transœsophagienne (reconstruction tridimensionnelle en temps réel) est plus précise que l’échocardiographie transthoracique pour préciser le mécanisme et la cause de l’insuffisance mitrale :
- prolapsus de la valve mitrale (préciser le ou les feuillets atteints, la taille de l’anneau mitral, la texture de la valve) ou au contraire rétraction valvulaire (RAA, anorexigènes, etc.) ;
- rupture de cordage/muscle papillaire (le plus souvent postérieur) ;
- trouble de la cinétique segmentaire et du muscle papillaire (insuffisance mitrale ischémique) ;
- végétation valvulaire ;
- recherche d’une valvulopathie associée (évocateur d’une étiologie rhumatismale ou plus rarement dystrophique).
Histoire naturelle
Elle est influencée par :
- la sévérité de la fuite ;
- l’étiologie ;
- la rapidité de la constitution de l’IM ;
- la fonction ventriculaire gauche ;
- les lésions associées.
Les complications sont dominées par les arythmies auriculaires et le risque d’insuffisance cardiaque gauche (et/ou droite en cas d’HTAP et de retentissement cardiaque droit), favorisé par les arythmies atriales rapides. Le risque d’endocardite infectieuse est à prendre en compte (voir Endocardite infectieuse).
Le risque de mort subite concerne la maladie de Barlow, dans sa forme dystrophique sévère, souvent à forme familiale, avec fréquemment une disjonction annulo-mitrale, à rechercher en échocardiographie.
________________________________________________________________________________
Prolapsus valvulaire mitral (PVM)
Le prolapsus valvulaire mitral correspond à l’éversion de tout ou partie d’un feuillet mitral dans l’OG à 2 mm en arrière du plan de l’anneau mitral, dans l’OG, en systole, et un point de coaptation valvulaire en deçà du plan annulaire mitral.
Le prolapsus valvulaire mitral touche 2 % de la population, avec une prévalence égale entre les genres.
Étiopathogénie
Le PVM primitif est en rapport avec une prolifération myxomateuse des feuillets valvulaires, caractérisé par un épaississement des feuillets et des cordages tendineux, du fait de l’accumulation anormale de mucopolysaccharides, avec prépondérance de la couche spongieuse des feuillets valvulaires, aboutissant à une anomalie de la cinétique valvulaire et tendineuse. Une élongation des cordages aboutit à un prolapsus valvulaire, avec perte de la coaptation valvulaire. Le prolapsus valvulaire mitral typique est caractérisé par un épaississement des feuillets valvulaires ≥ 5 mm, et est associé à un risque accru de complications.
Diagnostic
La plupart des prolapsus valvulaires mitraux sont asymptomatiques. La découverte à l’occasion d’une complication est la plus fréquente, arythmie auriculaire et/ou ventriculaire, régurgitation mitrale de volume variable, troubles du rythme auriculaire, et beaucoup plus rarement endocardite infectieuse.
Le diagnostic clinique auscultatoire est basé sur la perception d’un clic mésosystolique dans la forme classique, suivie d’un souffle mésotélésystolique, modifié dans certaines situations physiopathologiques : la réduction du retour veineux, l’augmentation de la contractilité ou du volume systémique aboutissent à la perception d’un clic plus précocement dans la systole, avec augmentation de la durée du souffle. Une reproduction de ces modifications hémodynamiques peut être produite par la position debout, la manœuvre de Valsalva. Elles ne sont guère plus utilisées depuis la diffusion des appareils d’échographie y compris ultraportables
Deux présentations cliniques sont décrites :
- Le syndrome de Barlow concerne des patients jeunes, et est caractérisé par une dilatation annulaire, une redondance des feuillets valvulaires et un prolapsus qui peut concerner plusieurs segments de la valve mitrale. La prédisposition génétique du prolapsus valvulaire mitral primitif est caractérisée, avec des formes familiales, et un mode de transmission autosomale dominant avec une pénétrance variable. Des loci ont été caractérisés sur les chromosomes 11-13 et 16 au sein de famille ayant des atteintes touchant plusieurs membres. Enfin, le prolapsus valvulaire mitral est identifié de façon plus fréquente dans le syndrome de Marfan, de Loeys-Dietz, d’Ehlers-Danlos et dans l’ostéogenèse imparfaite. Le risque d’arythmies ventriculaires, de mort subite est accru dans les formes sévères avec disjonction annulo-mitrale (diagnostic échocardiographique).
- La dégénérescence ou déficience fibro-élastique survient chez les patients plus âgés, et concerne de façon prépondérante la valve mitrale postérieure, en particulier le segment P2, et est associée à un amincissement des feuillets valvulaires et des cordages tendineux, avec un risque accru de rupture de ceux-ci.
Les caractéristiques cliniques électrocardiographiques et radiographiques n’ont pas de particularité.
Le diagnostic est donc basé sur l’échographie cardiaque par voie transthoracique qui caractérise le segment valvulaire atteint de façon prépondérante, les dimensions annulaires mitrales, et le retentissement auriculaire et/ou VG, le volume de la fuite, son retentissement sur les dimensions et les fonctions des cavités gauches et l’éventuelle atteinte du cœur droit (voir ci-dessous).
Traitement
Les patients se plaignant de palpitations sont traités par bêtabloquant de façon symptomatique.
Le traitement chirurgical est une chirurgie conservatrice de la valve mitrale dont les modalités sont déterminées par le type d’atteinte valvulaire. Ainsi, à type d’exemple, en cas de prolapsus valvulaire postérieur lié à un excès tissulaire, il est proposé une résection quadrangulaire, avec une annuloplastie, un raccourcissement des cordages tendineux et dans certaines situations également du muscle papillaire. En cas de prolapsus valvulaire antérieur lié à une pathologie dystrophique, un transfert de cordage ou un raccourcissement de ceux-ci, l’utilisation de cordage synthétique est proposée. En cas de prolapsus bi valvulaire, il est proposé une résection valvulaire, un transfert de cordage tendineux et l’utilisation éventuelle de cordage synthétique. La présence d’une dilatation annulaire mitrale conduit à la pose d’un anneau, l’annuloplastie faisant partie alors intégrante de la correction du vice valvulaire.
________________________________________________________________________________
Insuffisance mitrale ischémique
La vascularisation du muscle papillaire antérolatéral est double, liée à un apport par l’artère interventriculaire antérieure et circonflexe, diffère de celle du muscle papillaire postéromédian, vascularisé par la seule coronaire droite ou l’artère circonflexe, en fonction de la dominance coronaire.
L’insuffisance mitrale ischémique peut se présenter cliniquement comme une insuffisance mitrale aiguë, à la phase aiguë d’un infarctus du myocarde, ou être une cause d’insuffisance mitrale chronique, dans une maladie coronaire chronique.
L’ischémie myocardique ou l’infarctus du myocarde peut être à l’origine d’une dysfonction de muscle papillaire, d’une altération de la géométrie VG à l’origine d’une malposition du muscle papillaire, ou d’une élongation du muscle papillaire infarci, avec contraction exagérée de la zone non infarcie du muscle papillaire.
Les mécanismes à l’origine d’une insuffisance mitrale ischémique chronique sont une nécrose du muscle papillaire avec dysfonction myocardique segmentaire, prédominant sur la paroi postéro-inférieure, à l’origine d’un défaut de coaptation lié à une anomalie de la cinétique valvulaire, une réduction des forces régissant la fermeture de la valve mitrale, en rapport avec une dysfonction systolique VG et, par ailleurs, la dilatation cavitaire peut être à l’origine d’une dilatation annulaire, qui pérennise la régurgitation mitrale.
________________________________________________________________________________
Insuffisance mitrale aiguë
L’insuffisance mitrale aiguë est plus fréquemment liée à des anomalies mécaniques (rupture de cordages mitraux, rupture de muscle papillaire à la phase aiguë d’un IDM, etc.).
Il n’y a pas de caractéristique ECG en dehors de la documentation d’une séquelle d’infarctus du myocarde dans les IM chroniques d’origine ischémique, avec un risque accru de fibrillation atriale, dans le contexte d’insuffisance mitrale chronique, en particulier.
La radiographie thoracique documente un œdème pulmonaire, sans cardiomégalie dans un contexte d’insuffisance mitrale aiguë, sans dilatation de l’oreillette gauche, anomalies qui sont documentées en cas d’insuffisance mitrale chronique.
L’échographie cardiaque caractérise le mécanisme de la fuite mitrale et évalue le retentissement structural (pas de dilatation OG et VG, FEVG supranormale, sauf en cas de phase aiguë d’IDM) et fonctionnel (HTAP). L’échographie transœsophagienne joue un rôle important dans ce contexte aigu, permettant d’authentifier le mécanisme et de confirmer le caractère aigu et sévère de la régurgitation mitrale.
Il n’y a pas d’indication au cathétérisme cardiaque pour évaluer le niveau de pression intracardiaque ou le La coronarographie est indispensable lorsque le contexte ischémique est au premier plan.
Le traitement associe une approche médicamenteuse visant à réduire la post-charge VG à l’aide de vasodilatateur artériel et/ou veineux, sous réserve de préserver le débit cardiaque, et permettant d’accompagner le patient vers une solution chirurgicale, la seule permettant d’espérer un bon pronostic.
________________________________________________________________________________
Traitement de l’insuffisance mitrale
Traitement chirurgical
Modalités (fig. 4.16 et 4.17)
- Plastie reconstructrice : chirurgie conservatrice privilégiée chaque fois que possible confrontation échochirurgicale :
- Indications : toute insuffisance mitrale sévère, si la plastie est réalisable, sous contrôle échographique per-opératoire, en particulier sur prolapsus valvulaire, en particulier du feuillet postérieur : chirurgie de première intention.
- Avantages :
-
- résultat anatomique meilleur ;
- pas de traitement anticoagulant au long cours ;
- moindre morbi-mortalité péri-opératoire.
- Inconvénients :
-
- insuffisance mitrale résiduelle postopératoire ;
- taux de réintervention à distance accru ;
- difficile si valvulopathie mitrale rhumatismale avec calcifications annulaires importantes (contre-indication relative).
- Gestes associés :
-
- annuloplastie mitrale en cas de dilatation de l’anneau mitral associé ;
- plastie tricuspide si insuffisance tricuspide importante associée ou dilatation annulaire tricuspide (vidéo .4.13).
- plastie tricuspide si insuffisance tricuspide importante associée ou dilatation annulaire tricuspide (vidéo .4.13).
________________________________________________________________________________
Figure 4.16. Algorithme des recommandations de l’ESC, 2017.
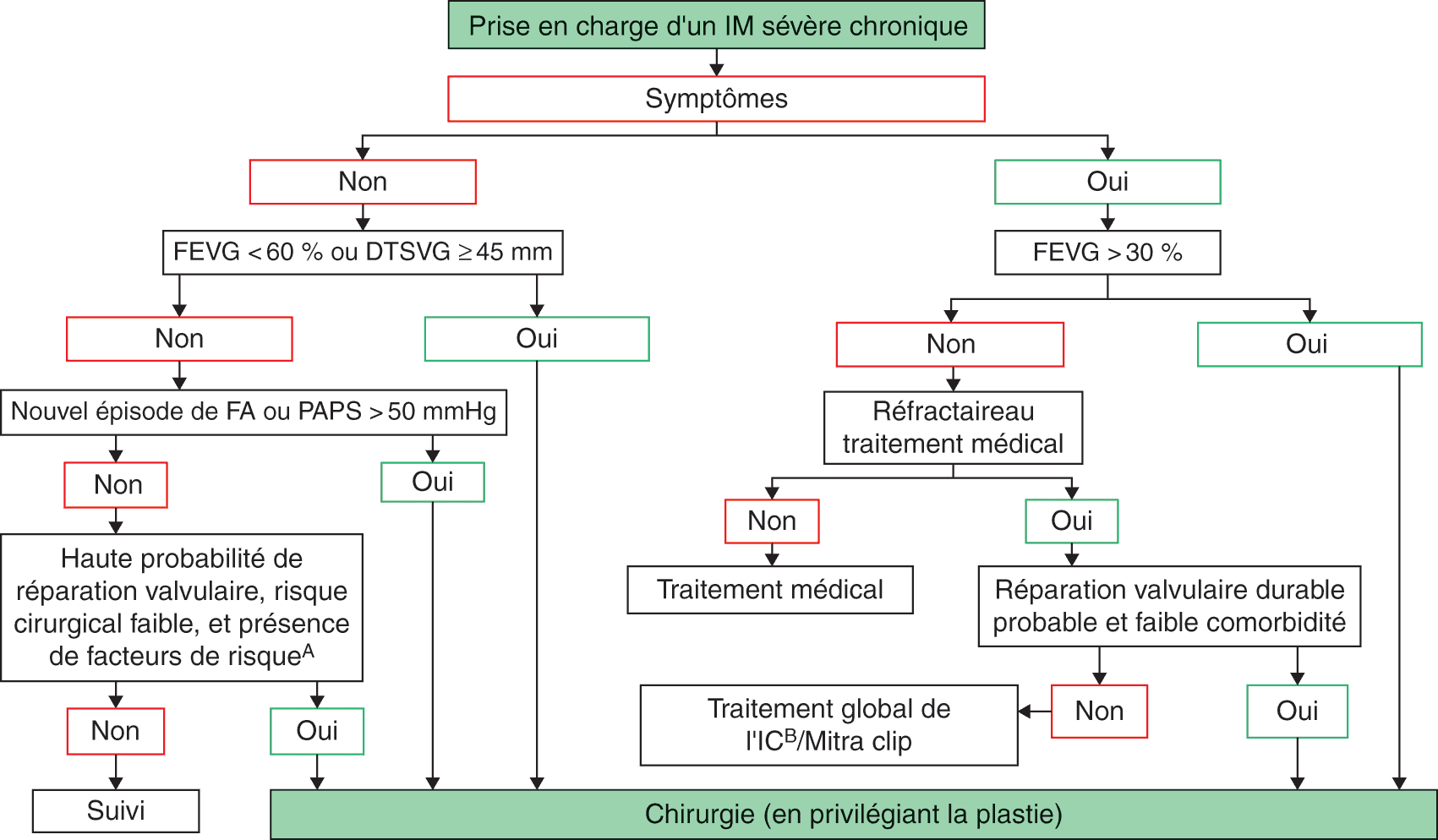
________________________________________________________________________________
Figure 4.17. Rôle des différents médecins dans la prise en charge d’une insuffisance mitrale.
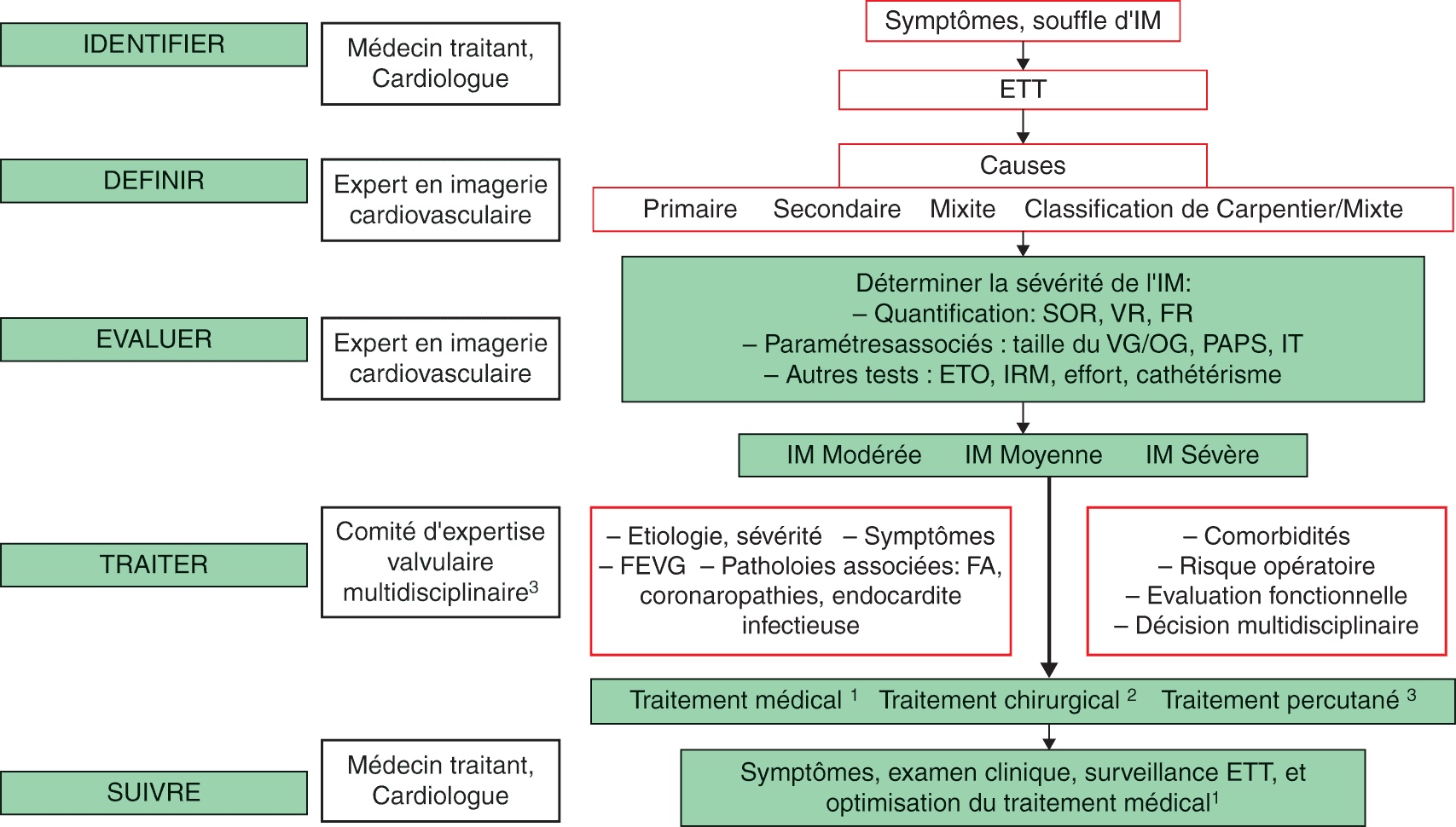
________________________________________________________________________________
Remplacement valvulaire mitral prothétique
Si la plastie est impossible ou ses résultats insuffisants.
Interventions percutanées
Les interventions percutanées sur la valve mitrale sont en plein essor. Actuellement, la réparation percutanée mitrale bord à bord (Mitra Clip®) bénéficie d’une expérience plus importante par rapport à d’autres techniques percutanées.
Indications
- Insuffisance mitrale sévère chez les patients symptomatiques avec :
-
- FEVG > 30 % ;
- FEVG < 30 %, réfractaires au traitement médical, avec une anatomie mitrale favorable à une valvuloplastie réparatrice, et en l’absence de comorbidités sévères.
- Insuffisance mitrale sévère chez les patients asymptomatiques mais avec retentissement hémodynamique :
-
- FEVG ≤ 60 % ou diamètre télésystolique du ventricule gauche ≥ 45 mm ;
- nouvel épisode de fibrillation atriale secondaire à l’insuffisance mitrale ;
- pression artérielle pulmonaire systolique > 50 mmHg.
- Diamètre télésystolique du ventricule gauche ≥ 40 mm avec un prolapsus valvulaire ou un volume de l’oreillette gauche > 60 ml/m2 en rythme sinusal, et un faible risque chirurgical. La réparation percutanée mitrale bord à bord (Mitra Clip®) est recommandée dans le traitement de l’insuffisance mitrale primaire chez des patients symptomatiques avec une FEVG < 30 % réfractaire au traitement médical, qui remplissent les critères d’éligibilité échocardiographiques et qui présentent un risque chirurgical élevé. Un élargissement des indications à l’IM secondaire, en comparaison avec la chirurgie est en cours d’évaluation, avec les résultats récents mais contradictoires de deux essais randomisés.
Traitement médicamenteux
- Vasodilatateurs artériels : IEC.
- Associés à un diurétique de l’anse en cas de signes congestifs.
En réduisant la post-charge du ventricule gauche, la fraction de sang régurgité vers l’atrium gauche est réduite. Ces traitements retarderaient l’apparition des signes fonctionnels liés à l’insuffisance mitrale, ainsi que l’apparition d’une dilatation et d’une hypertrophie ventriculaire gauche.
Hygiène de vie
Régime pauvre en sel en cas de signes d’insuffisance cardiaque congestive (voir chapitre 5, Sémiologie de l’insuffisance cardiaque).
Surveillance clinico-échographique
Elle dépend du degré de l’insuffisance aortique :
- insuffisance mitrale modérée à moyenne : surveillance tous les ans ;
- insuffisance mitrale sévère : surveillance tous les semestres.
Insuffisance aortique (IA)
Une régurgitation aortique (IA) peut se développer suite à une atteinte des feuillets valvulaires aortiques et/ou à une anomalie de la racine aortique ou de l’aorte ascendante. Il est important de distinguer les formes aiguës et chroniques d’insuffisance aortique, dont le mécanisme, le retentissement, la physiopathologie, les causes et les modalités de prise en charge diffèrent.
Physiopathologie de l’insuffisance aortique
En cas d’insuffisance aortique, à chaque diastole, lorsque la valve aortique se referme, une partie du volume éjecté dans l’aorte reflue dans le ventricule gauche. Le volume se retrouvant dans le ventricule gauche à la fin de la diastole est donc le volume provenant de l’éjection de l’atrium vers le ventricule gauche auquel on additionne le volume régurgité par la valve aortique. Ainsi, le volume télédiastolique (volume présent dans le ventricule gauche à la fin de la diastole) est augmenté dans l’insuffisance aortique, c’est-à-dire que la précharge augmente (fig. 4.18). Mais la post-charge est elle aussi augmentée au cours de l’insuffisance aortique : en effet, le volume devant être éjecté par le ventricule gauche à chaque systole est plus important, donc un plus grand volume doit passer à travers un orifice aortique dont l’ouverture n’est pas modifiée, représentant ainsi une augmentation fonctionnelle de la post-charge. Cette surcharge diastolique a deux conséquences importantes sur le ventricule gauche :
- la dilation du ventricule gauche : elle est directement liée à l’élévation de la précharge du ventricule gauche ; le ventricule gauche est ainsi à l’origine d’un volume d’éjection plus important, préservant donc la perfusion périphérique ;
- la réponse ventriculaire gauche est le développement d’une hypertrophie compensatrice excentrique, avec une adaptation du volume ventriculaire gauche, sans élévation initiale de la pression télédiastolique ventriculaire gauche. L’hypertrophie du ventricule gauche. En effet, selon la loi de Laplace, si le ventricule gauche se dilate et que la post-charge augmente, l’épaisseur du ventricule gauche doit elle aussi augmenter afin d’éviter l’élévation de la tension pariétale.
________________________________________________________________________________
Figure 4.18. Schéma de la physiopathologie de la régurgitation aortique.
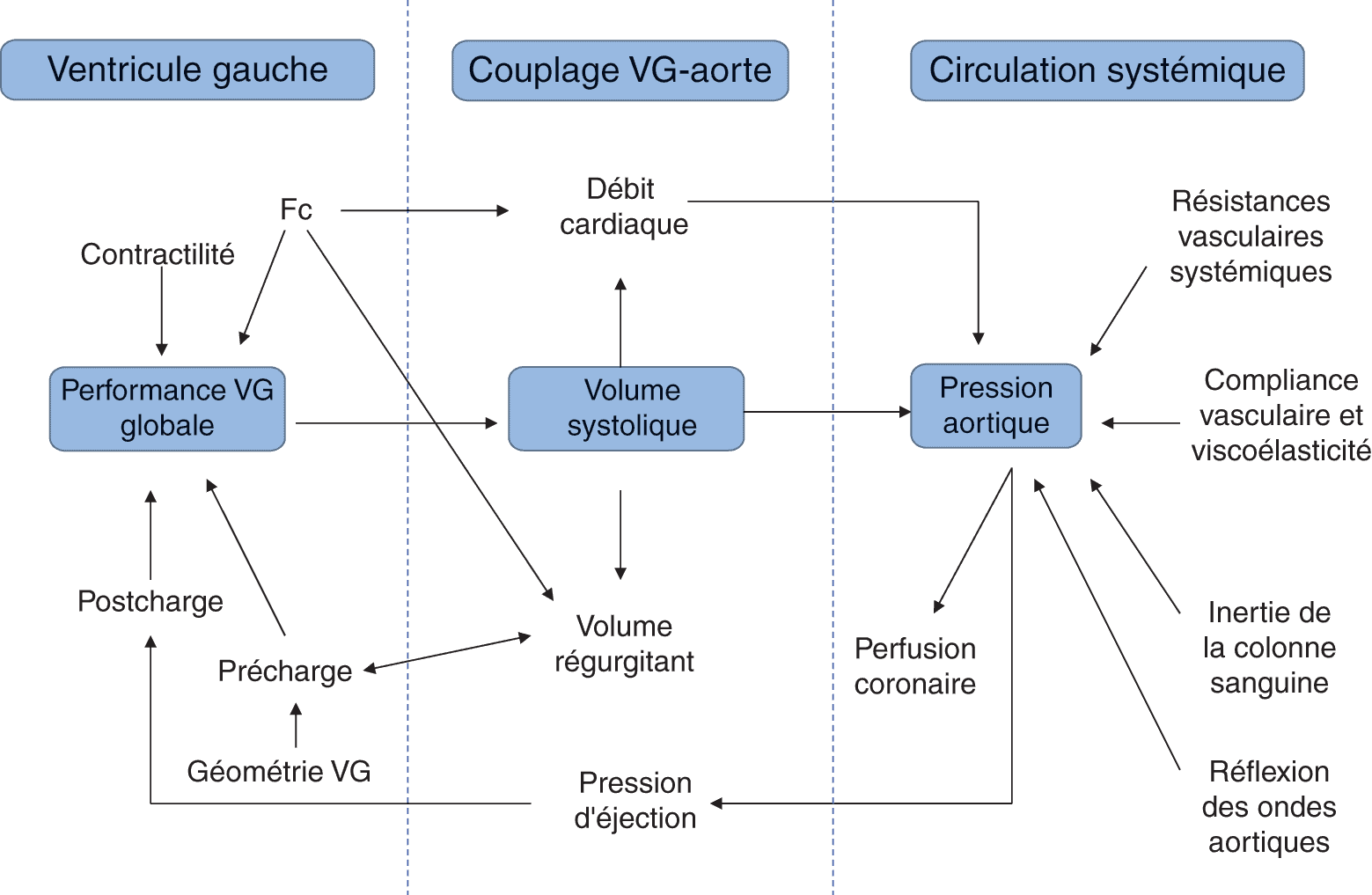
________________________________________________________________________________
Au cours de l’évolution, une fibrose interstitielle contribue à réduire la compliance ventriculaire gauche, conduisant à une décompensation de cette phase chronique. La surcharge volumique chronique aboutit à une altération de la vidange ventriculaire gauche, à une augmentation du volume télédiastolique et de la pression télédiastolique ventriculaire gauche, à l’origine d’une accentuation de la dilatation du ventricule gauche et à une réduction de la fraction d’éjection et du débit cardiaque, qui apparaissent tardivement.
L’apparition d’une dysfonction ventriculaire gauche est à l’origine de l’apparition de symptômes, dyspnée à l’effort, orthopnée et dyspnée paroxystique nocturne. L’angor est rare dans l’insuffisance aortique, mais peut survenir en l’absence de lésion coronaire épicardique significative en rapport avec une diminution de la pression de perfusion coronaire diastolique, la bradycardie et la baisse de la pression artérielle diastolique ainsi que l’hypertrophie ventriculaire gauche, à l’origine d’une ischémie myocardique sous endocardique.
Causes de l’insuffisance aortique (tableau 4.6)
________________________________________________________________________________
Principales causes d’insuffisance aortique
Les causes aiguës sont signalées par un*
Anomalie des feuillets valvulaires aortiques
- Maladie aortique annulo-ectasiante (ou maladie aortique dégénérative dystrophique).
- RAA. Cette maladie peut entraîner une insuffisance aortique par action à différents niveaux : valve, anneau, aorte ascendante.
- Endocardite infectieuse.
- Traumatique (traumatisme fermé du thorax).
- Dégénérescence myxoïde.
- Bicuspidie aortique.
- Valvulopathies auto-immunes et systémiques : lupus érythémateux systémique, polyarthrite rhumatoïde, spondylarthrite ankylosante, artérite de Takayasu, maladie de Whipple ; maladie de Crohn.
- Valvulopathie aortique médicamenteuse.
Atteinte de la racine aortique ou de l’aorte ascendante
- Maladie aortique annulo-ectasiante (ou maladie aortique dégénérative dystrophique).
- Nécrose médiale kystique aortique (bicuspidie valvulaire aortique ou syndrome de Marfan).
- HTA.
- Dissection aortique.
- Aortite (syphilis, artérite à cellules géantes).
- Valvulopathies auto-immunes et systémiques : syndrome de Reiter, spondylarthrite ankylosante, syndrome de Behçet, arthrite psoriasique, ostéogénose imparfaite, polychondrite atrophiante, syndrome d’Ehlers-Danlos.
Dysfonction de prothèse valvulaire aortique
- Valvuloplastie aortique au ballon.
- Fuite périvalvulaire ou déhiscence de prothèse valvulaire (TAVI).
________________________________________________________________________________
Maladie de Marfan
La fibrilline de type 1 est une protéine synthétisée par les fibroblastes (cellules du tissu conjonctif). Elle est le principal composant des microfibrilles, éléments majeurs de la matrice extracellulaire du tissu conjonctif (élastique et non élastique). Elle est donc présente dans le tissu cardiaque (principalement au niveau de la racine de l’aorte), mais elle existe également dans le squelette, les yeux, la peau. La fibrilline est une protéine de grande taille codée par le gène FBN1 (chromosome 15). Lorsque se produit une mutation de ce gène, comme c’est le cas dans la maladie de Marfan (maladie autosomique dominante, prévalence d’un pour 5 000 à un pour 10 000, sex-ratio de 1), le sujet développe une maladie du tissu conjonctif :
- atteinte cardiaque, qui est la manifestation la plus grave de la maladie :
-
- valvulaire : insuffisance mitrale, insuffisance aortique ;
- vasculaire : anévrisme/dilatation de l’aorte ascendante, dissection aortique (critères majeurs) ;
- atteinte ophtalmique : subluxation du cristallin (critère majeur), cataracte ;
- atteinte articulaire : déformation de la cage thoracique, hyperlaxité ligamentaire.
D’autres gènes, TGFBR1 (chromosome 3) et TGFBR1 (chromosome 9), sont impliqués dans la maladie de Marfan.
Spécificité de la prise en charge en cas de maladie de Marfan :
- prise en charge en centre spécialisé (centre de référence et de compétences) ;
- dépistage familial ;
- prescription de bêtabloquant qui réduit la pression artérielle, donc la contrainte pariétale s’exerçant sur l’aorte, ce qui retarde la dilatation de l’aorte ascendante.
________________________________________________________________________________
Tableau 4.6. Causes des principales valvulopathies gauches, en fonction du contexte aigu ou chronique pour les régurgitations.
| Valve aortique | Valve mitrale | |||
| Insuffisance aortique | Rétrécissement aortique | Insuffisance mitrale | Rétrécissement mitral | |
| Causes aiguës | Dissection aortique
Endocardite infectieuse Traumatisme fermé du thorax |
– | Endocardite infectieuse
Infarctus du myocarde inférieur et rupture de cordage/pilier Syndrome de rupture sur insuffisance mitrale dystrophique sous-jacente (Barlow ou dégénérescence fibro-élastique) avec ou sans maladie de Marfan |
– |
| Causes chroniques | Maladie annulo-ectasiante
RAA Bicuspidie Aortite HTA Marfan Ehler-Danlos Rhumatisme inflammatoire (polyarthrite rhumatoïde, spondylarthrite ankylosante) |
Maladie de Mönckeberg : rétrécissement aortique dégénératif du sujet âgé le plus fréquent
Cause la plus fréquente chez les moins de 70 ans : bicuspidie Cause la plus fréquente dans les pays émergents : RAA |
Organique :
Maladie de Barlow (sujet jeune) Dégénérescence fibro-élastique (sujet âgé) RAA |
RAA (> 95 %)
Congénital (exceptionnel) |
| Fonctionnelle :
Insuffisance mitrale ischémique Insuffisance mitrale restrictive Dilatation de l’anneau |
||||
Sémiologie de l’insuffisance aortique
Signes fonctionnels
Les patients peuvent être asymptomatiques pendant de nombreuses années, jusqu’à ce que les phénomènes adaptatifs soient dépassés (cf. supra Physiopathologie de l’insuffisance aortique). Dans les insuffisances aortiques aiguës, cette symptomatologie peut s’installer brutalement. Les symptômes présentés par les patients souffrant d’une insuffisance aortique sont le plus souvent aspécifiques, tels que :
- asthénie ;
- dyspnée ;
- douleurs angineuses. Ces douleurs ne sont pas corrélées à la présence de lésions coronaires, mais sont le plus souvent fonctionnelles : en effet, dans l’insuffisance aortique il existe une hypertrophie ventriculaire gauche secondaire à la surcharge diastolique du ventricule gauche ; il apparaît alors une inadéquation entre les besoins accrus en oxygène d’un myocarde hypertrophié et les capacités de perfusion inchangées d’un réseau coronaire devenu insuffisant pour assurer un débit coronaire corrélé aux besoins myocardiques.
Souffle d’insuffisance aortique (fig. 4.9 et tableau 4.7) :
- foyer : souffle au foyer aortique, irradiant vers le long du bord gauche du sternum ;
- temps : protodiastolique decrescendo ;
- caractéristiques : doux, humé, aspiratif, augmenté à l’inspiration profonde et en procubitus.
Tableau 4.7. Modifications des souffles systoliques.
| Rétrécissement
aortique |
Insuffisance
mitrale |
Prolapsus
valvulaire mitral |
|
| Épreuve de Valsalva | ↓ | ↓= | ↑ ou ↓ |
| Position debout | ↑= | ↓ | ↑ |
| Épreuve d’effort mineure | ↓= | ↑ | ↓ |
| Position couchée, jambes élevées | ↑= | = | ↓ |
| Exercice physique | ↑= | ↓ | ↑ |
↑ Augmentation de l’intensité du souffle. =, pas de modification de l’intensité du souffle. ↓ Diminution de l’intensité du souffle.
Signes physiques associés et signes de gravité
Plusieurs signes physiques peuvent être observés dans les insuffisances aortiques importantes :
- élargissement de la pression artérielle différentielle, avec baisse de la pression artérielle diastolique ;
- hyperpulsatilité artérielle ;
- déviation du choc de pointe à gauche secondaire à l’hypertrophie du ventricule gauche ;
- galop B3 (protodiastolique) au foyer mitral ;
- pistol shot mésosystolique subclavier droit (claquement sec lié à la distension brusque de l’aorte ascendante) ;
- roulement diastolique de Flint au foyer mitral : le flux de régurgitation aortique lors de la diastole se répercute jusqu’à la valve mitrale entraînant une gêne à la bonne ouverture de cette dernière, responsable de la perception d’un souffle ressemblant à un rétrécissement mitral fonctionnel.
Examens complémentaires
ECG
- Hypertrophie ventriculaire gauche diastolique : augmentation de l’indice de Sokolow (S en V1/V2 + R en V5/V6 > 35 mm) et ondes T positives dans les dérivations précordiales gauches et/ou latérales.
- Hypertrophie ventriculaire gauche systolique (lorsque l’insuffisance aortique évolue depuis plus longtemps) : apparition d’ondes T négatives dans les dérivations précordiales gauches et/ou latérales.
- Bloc de branche gauche incomplet fréquent (± déviation axiale gauche : au-delà de – 30°).
Radiographie thoracique
- Arc supérieur droit dilaté du fait de la dilatation de l’aorte ascendante.
- Concavité de l’arc moyen gauche plus marquée.
- Arc inférieur gauche élargi secondairement à l’HVG.
- Cardiomégalie (en cas de dilatation du VG).
- ± Surcharge pulmonaire* (fig. 4.16).
Échocardiographie (vidéo 4.1, vidéo 4.2, vidéo 4.3), vidéo 4.4)
Diagnostic positif
Les anomalies valvulaires et/ou de la racine aortique sont décrites, le mécanisme de la régurgitation est précisé ainsi que la cause, anomalie des feuillets valvulaires et/ou de la racine aortique. L’ETO peut apporter un complément dans l’analyse du mécanisme, lorsque l’ETT est en échec ou insuffisante à caractériser les lésions.
Le diagnostic est le plus souvent fait au cours de l’étude en Doppler couleur de la valve aortique : on découvre un jet de régurgitation aortique holodiastolique de forte vélocité (> 4 m/s) refluant de l’aorte vers le ventricule gauche.
La régurgitation aortique est visualisée en Doppler couleur, l’origine et la direction du jet orientent vers le mécanisme de la régurgitation : jet homolatéral en cas de restriction valvulaire, jet controlatéral en cas de prolapsus valvulaire, jet central en cas de dilatation annulaire aortique.
Diagnostic de gravité
Les différents paramètres nécessaires au diagnostic de gravité sont recueillis au cours de l’échoDoppler cardiaque transthoracique :
- la quantification de la fuite par PISA (étude de la zone de convergence) permet de calculer :
-
- diamètre du jet à son origine > 6 mm en faveur d’une régurgitation sévère (vena contracta) ;
- SOR : surface de l’orifice régurgitant ; > 30 mm2 en faveur d’une régurgitation sévère ;
- VR : volume régurgitant ; > 60 ml en faveur d’une régurgitation sévère ;
- FR : fraction de régurgitation > 40 % en faveur d’une régurgitation sévère ;
- retentissement :
-
- pressions pulmonaires ;
- fonctions diastolique (pressions de remplissage ventriculaire gauche) et systolique du ventricule gauche (fraction d’éjection ventriculaire gauche, FEVG). Une altération précoce du strain longitudinal global (SLG) est rapportée alors même que la FEVG est longtemps normale.
Diagnostic étiologique
Les lésions anatomiques valvulaires sont caractérisées en échocardiographie transœsophagienne (2D et 3D), technique plus précise que l’échocardiographie transthoracique :
- maladie aortique dégénérative dystrophique voir encadré: épaississement valvulaire avec calcifications des feuillets ;
- bicuspidie (cf. supra), sténose aortique : visualisation uniquement de deux feuillets valvulaires semi-lunaires ; la bicuspidie est surtout vue en incidence parasternale gauche « petit axe » ;
- dilatation de l’aorte ascendante (préciser le ou les sites de dilatation : racine aortique, jonction sinotubulaire, aorte ascendante dans son segment tubulaire, crosse, aorte descendante) ;
- RAA : sigmoïdes calcifiées, épaissies, rétractées (rechercher une valvulopathie mitrale associée) ;
- Endocardite infectieuse : présence d’une végétation valvulaire ; elle peut s’accompagner d’un éventuel abcès de la valve aortique ou de l’anneau aortique ; la présence d’une végétation isolée confirme le diagnostic d’endocardite, sans pour autant affirmer son caractère infectieux (cf. supra).
Histoire naturelle de l’insuffisance aortique chronique
L’insuffisance aortique est longtemps asymptomatique.
La régurgitation aortique moyenne à sévère à un bon pronostic pendant de nombreuses années, à la condition que le patient soit asymptomatique et qu’il n’y ait pas d’apparition de signe de dysfonction ventriculaire gauche à l’échocardiographie ou à l’imagerie de déformation. En effet, le strain myocardique longitudinal peut s’altérer dans les cas de retentissement myocardique, en l’absence d’altération de la FEVG.
Il faut noter que 90 % des patients sont asymptomatiques à trois ans et 75 % à 7 ans après un diagnostic d’insuffisance aortique chronique. Les patients porteurs d’une régurgitation modérée à moyenne ont un taux de survie à 10 ans supérieur à 85. Les patients ayant une régurgitation moyenne à sévère sous traitement médical ont un taux de survie de 75 %, à 5 ans et de 50 % à 10 ans.
Après l’apparition de signes de dysfonction ventriculaire gauche, la progression vers l’apparition de symptômes est accélérée (25 % par an).
Chez les patients ayant une dyspnée classe fonctionnelle NYHA 3 à 4, en l’absence de correction chirurgicale, le taux de survie à 4 ans n’est que de 28 %.
________________________________________________________________________________
Insuffisance aortique aiguë
Physiopathologie
L’insuffisance aortique aiguë est une urgence hémodynamique, du fait de l’incapacité du ventricule gauche à s’adapter à la surcharge de volume aigu, à l’origine de l’augmentation du volume ventriculaire gauche. En effet, le volume d’éjection antérograde et le débit cardiaque chutent rapidement, à l’origine d’une hypotension artérielle et d’un choc cardiogénique. L’augmentation aiguë et brutale de la pression diastolique du ventricule gauche est à l’origine d’une fermeture prématurée de la valve mitrale en protodiastole, protégeant ainsi la vascularisation pulmonaire d’une élévation de la pression diastolique. Cependant, la décompensation ventriculaire gauche conduit à l’apparition d’une fuite mitrale diastolique, qui est à l’origine d’une transmission de l’élévation de la pression diastolique ventriculaire gauche au lit vasculaire pulmonaire, à l’origine d’un œdème pulmonaire.
La tachycardie qui accompagne cette altération de la fonction cardiaque contribue à réduire la durée de la diastole et donc la période de remplissage ventriculaire gauche pendant laquelle la valve mitrale est ouverte.
Diagnostic
La présentation clinique d’une insuffisance aortique aiguë se caractérise par une altération hémodynamique aiguë et brutale avec dyspnée sévère, OAP ou syncope avec un risque progressif d’évolution rapide vers un choc cardiogénique (hypotension artérielle, tachycardie, pâleur, cyanose, extrémités froides, signes congestifs et syndrome confusionnel).
L’examen périphérique est pauvre, avec en particulier l’absence de signes d’hyperpulsatilité et une pression artérielle normale ou faiblement réduite.
L’examen clinique peut être utile en cas de suspicion de dissection aortique, avec la caractérisation et la documentation d’une asymétrie tensionnelle, inconstante.
Le B1 peut être diminué du fait de la fermeture prématurée de la valve mitrale ; l’apparition d’un B3 est synonyme de décompensation cardiaque.
Le souffle diastolique d’insuffisance aortique est plus court que dans les formes chroniques. En cas d’insuffisance aortique aiguë sévère, le souffle diastolique peut ne pas être audible lorsque les pressions diastoliques du ventricule gauche et de l’aorte s’équilibrent. Le souffle systolique d’accompagnement, traduisant l’augmentation du flux transvalvulaire, peut être entendu, mais de façon inconstante.
Traitement
Le traitement médical ne peut être que symptomatique précédant le geste chirurgical urgent dans ce contexte de retentissement hémodynamique plus ou moins sévère, avec réduction du débit cardiaque. Le contexte peut conduire à un traitement spécifique, traitement d’une endocardite infectieuse par antibiotiques, stabilisation de la pression artérielle en cas de dissection aortique…
Le traitement chirurgical s’impose rapidement après stabilisation de l’état hémodynamique.
________________________________________________________________________________
Traitement
Traitement chirurgical
Sa prise en charge thérapeutique repose essentiellement sur la chirurgie de remplacement valvulaire aortique prothétique (fig. 4.19).
________________________________________________________________________________
Figure 4.19. Insuffisance aortique aiguë : conduite à tenir (recommandations ESC, 2017).
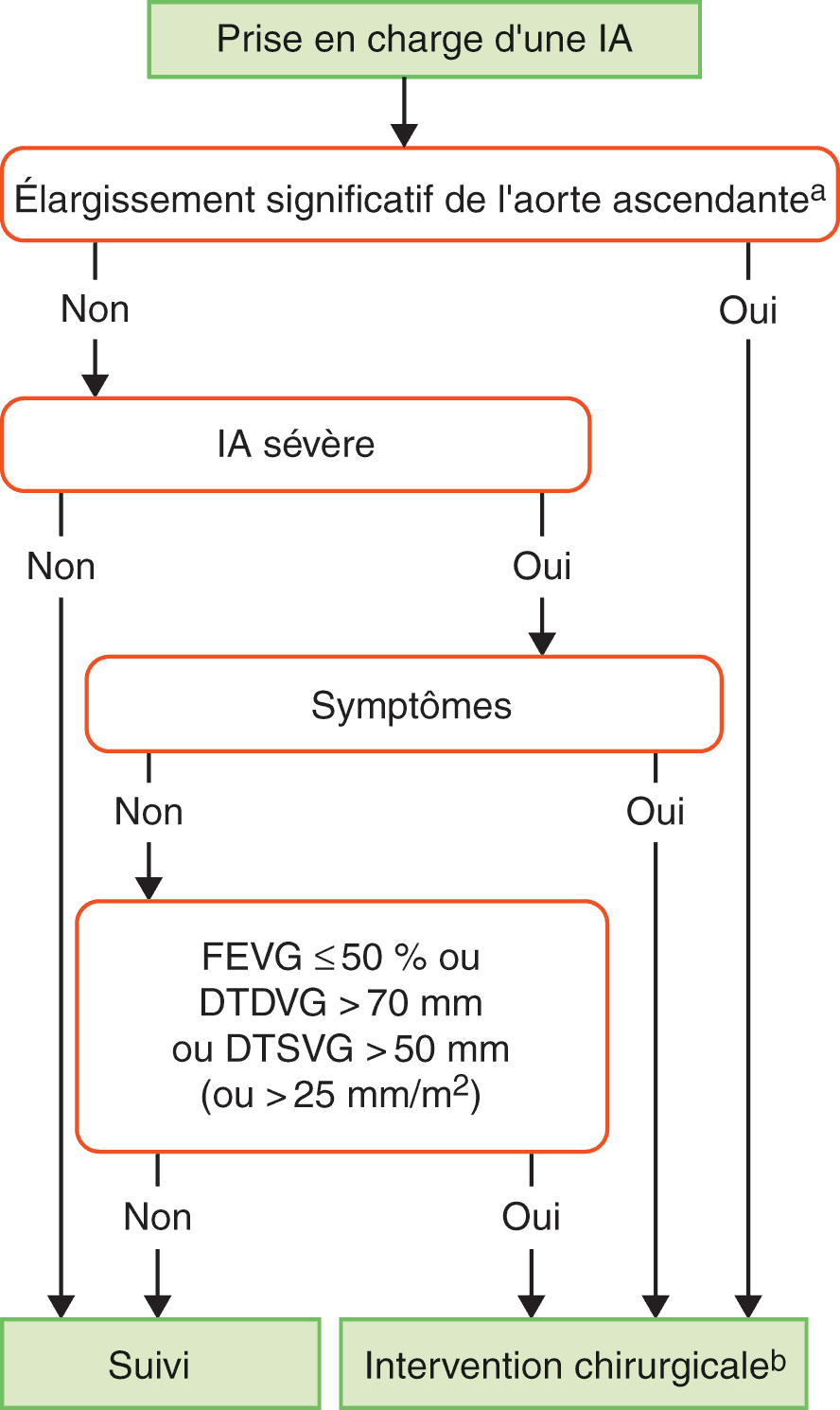
Source : Baumgartner H. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Europ Heart J 2017; 38: 2739–2791.
________________________________________________________________________________
Indications
- Indications du remplacement valvulaire aortique prothétique :
- insuffisance aortique sévère symptomatique ;
- insuffisance aortique sévère asymptomatique avec retentissement sur le ventricule gauche : fraction d’éjection du ventricule gauche ≤ 50 %, diamètre télédiastolique du ventricule gauche > 70 mm ou diamètre télésystolique du ventricule gauche > 50 mm (ou 25 mm/m2).
- Indications du remplacement de l’aorte ascendante associée :
- dilatation de l’aorte ascendante > 55 mm chez le sujet sain ou avec bicuspidie sans facteurs de risques ;
- dilatation de l’aorte ascendante > 50 mm en cas de bicuspidie aortique et facteurs de risques associés ou en cas de maladie de Marfan sans facteurs de risques ;
- dilatation de l’aorte ascendante > 45 mm en cas de maladie de Marfan et de facteur de risque.
Ces dernières indications peuvent être retenues à titre préventif (prévention de la dissection aortique) en respectant ces valeurs seuils et en précisant l’évolutivité.
Modalités
Remplacement valvulaire aortique par prothèse mécanique ou biologique, plus ou moins associé à un remplacement de l’aorte ascendante par un tube prothétique avec réimplantation des artères coronaires sur le tube prothétique (intervention de Bentall) en cas de dilatation de l’aorte ascendante associée (selon les valeurs seuils précisées ci-dessus).
Médicaments
Vasodilatateurs artériels : IEC, nifédipine.
En réduisant la post-charge du ventricule gauche, ces traitements préviennent la dilatation du ventricule gauche ainsi que l’hypertrophie ventriculaire gauche. Ils sont également associés à une moindre altération de la FEVG, à un retard dans l’apparition des signes fonctionnels liés à l’insuffisance aortique et donc des indications chirurgicales qui peuvent être différées sous surveillance clinique, biologique (BNP) et échocardiographique stricte.
Hygiène de vie
Régime pauvre en sel en cas de signes d’insuffisance cardiaque (cf. chapitre 5, Sémiologie de l’insuffisance cardiaque).
Surveillance clinique et échocardiographique
Tous les six mois à un an en cas d’insuffisance aortique sévère asymptomatique.
Insuffisance tricuspide (IT) (hors programme)
L’insuffisance tricuspide se manifeste par un reflux sanguin du ventricule droit à l’oreillette droite au travers de l’orifice tricuspide lors de la systole.
Valvulopathie la plus rare par ordre de fréquence, elle est souvent associée à une atteinte cardiaque gauche.
Physiopathologie
Insuffisance tricuspide fonctionnelle secondaire à une HTAP
La vitesse d’installation de l’HTAP, brutale ou progressive, détermine l’importance du retentissement clinique et la capacité d’adaptation du ventricule droit à l’augmentation de la post-charge.
HTAP aiguë
Une HTAP aiguë a pour conséquence une dilatation brutale du ventricule droit à l’origine d’une élévation rapide des pressions de remplissage. La surcharge volumique diastolique du ventricule droit, dans un péricarde physiologiquement peu compliant, entraîne des troubles du remplissage du ventricule gauche, eux-mêmes à l’origine d’une diminution du volume diastolique et de la fraction d’éjection du ventricule gauche.
L’insuffisance tricuspide est secondaire à une dilatation de l’anneau. Les mécanismes de compensation, tel que l’hypertrophie ventriculaire droite, n’ont pas le temps de se mettre en place.
HTAP d’installation progressive
L’insuffisance tricuspide est d’apparition tardive et concomitante à la survenue d’une dysfonction ventriculaire droite. L’hypertrophie ventriculaire droite est le principal mécanisme de compensation et d’adaptation du cœur à l’augmentation de la pression artérielle pulmonaire. La dilatation cavitaire est plus tardive.
Le mécanisme de l’insuffisance tricuspide est alors une dilatation de l’anneau et une altération de la cinétique de l’appareil sous-valvulaire secondaire à la dysfonction systolique ventriculaire droite.
Insuffisance tricuspide organique
Il existe une altération primitive de l’appareil valvulaire et sous-valvulaire associant inconstamment une destruction des valves, piliers, cordages ou muscles papillaires.
Les causes organiques sont principalement représentées par la valvulopathie rhumatismale à l’origine d’un remaniement valvulaire avec épaississement de l’extrémité des feuillets, une fusion commissurale, une rétraction et une limitation de la mobilité valvulaire. Les autres causes sont plus rares (tableau des causes)
Causes
Voir tableau 4.8.
Tableau 4.8. Causes d’insuffisance tricuspide.
| Primaires | Secondaires |
| – Rhumatisme articulaire aigu
– Endocardite infectieuse – Tumeurs carcinoïdes, myxome, – Endocardite infectieuse ou marastique – Prolapsus valvulaire tricuspide dystrophique – IDM aigu inférieur avec extension au ventricule droit (nécrose ou dysfonction d’un muscle papillaire) – Maladies congénitales : maladie d’Ebstein, dysplasie/hypoplasie valvulaire tricuspide, double orifice valvulaire tricuspide – Traumatisme : (traumatisme pénétrant ou non, pathologie iatrogène, pacemaker, biopsie endomyocardique) |
– Surcharge volumétrique du VD : communication interauriculaire
– Surcharge barométrique du VD : atteintes du cœur gauche (valvulopathies mitrales > aortiques, pathologies myocardiques), cœur pulmonaire, sténose pulmonaire, HTAP primitive, infarctus du myocarde ventriculaire droit – Fibrillation atriale, dilatation de l’oreillette droite, dilatation annulaire tricuspide – Stimulation ventriculaire droite (asynchronisme) – Dysplasie arythmogène du ventricule droit (DVDA) |
Diagnostic
Signes fonctionnels
L’insuffisance tricuspide est longtemps marquée par une symptomatologie pauvre, aspécifique, voire absente, et l’apparition de signes fonctionnels témoigne souvent d’un stade sévère : asthénie, fatigabilité, hépatalgie d’effort, pulsations cervicales et dans les globes oculaires, perte de poids voire cachexie, oligurie.
On retrouve fréquemment des symptômes en lien avec les valvulopathies associées notamment gauches, plus volontiers symptomatiques.
Signes d’examen clinique
L’inspection peut mettre en évidence des signes d’insuffisance ventriculaire droite (œdèmes des membres inférieurs et des lombes, ascite, turgescence jugulaire). Dans les formes évoluées peuvent apparaître une cyanose ou un ictère.
La palpation recherche une hépatosplénomégalie douloureuse, un reflux hépato-jugulaire, une expansion systolique du foie. Il peut exister un pouls veineux jugulaire voire un thrill systolique veineux avec souffle cervical en cas de forme sévère.
L’auscultation cardiaque caractéristique met en évidence un souffle de régurgitation holosystolique, maximal au foyer xiphoïdien ou à la partie basse du bord gauche du sternum et irradiant au bord gauche du sternum. Il est de timbre doux et d’intensité faible, celle-ci se majorant à l’inspiration profonde (signe de Carvalho) ou lors des manœuvres d’accroissement du retour veineux (compression hépatique, position de Trendelenburg) et se minorant en position verticale ou lors d’une manœuvre de Valsalva.
On peut également observer un éclat du B2 au foyer pulmonaire en cas d’hypertension pulmonaire ou un galop protodiastolique B3.
Examens complémentaires
Électrocardiogramme
L’électrocardiogramme peut être normal ou montrer des signes aspécifiques de surcharge droite : hypertrophie auriculaire droite (augmentation de l’amplitude de l’onde P en D2, D3 > 2,5 mm), hypertrophie ventriculaire droite (axe droit, ondes R amples, rapport onde R / onde S supérieur à 1 en V1, S1Q3, déviation axiale droite).
D’autres signes non spécifiques sont souvent décrits en cas d’insuffisance tricuspide comme une fibrillation atriale (qui est également une cause de majoration de la régurgitation) ou un bloc incomplet droit.
Radiographie thoracique
La radiographie thoracique peut-être normale ou montrer des signes aspécifiques, une cardiomégalie avec débord de l’arc inférieur droit (dilatation de l’oreillette droite), une surélévation de la pointe du cœur au-dessus de la coupole diaphragmatique (dilatation du ventricule droit). Peuvent également être décrits une dilatation des artères pulmonaires en cas d’hypertension artérielle pulmonaire, un épanchement pleural et une ascite avec ascension des coupoles diaphragmatiques.
Échocardiographie Doppler
L’échocardiographie transthoracique demeure l’examen de référence pour le diagnostic positif, le diagnostic étiologique, la quantification, l’évaluation du retentissement et la recherche de valvulopathies associées
Échocardiographie bidimensionnelle, 3D et en mode M (mécanismes et causes)
L’insuffisance tricuspide physiologique est caractérisée par des valves de structures et de cinétique normales et une absence de dilatation des cavités droites
Dans l’insuffisance tricuspide secondaire, les valves sont également de structure et de cinétique normales mais il existe une dilatation des cavités droites et de l’anneau tricuspide (≥ 35 mm ou > 21 mm/m2 en diastole en coupe apicale 4 cavités) avec une augmentation du tenting des feuillets tricuspides, c’est-à-dire une attraction du point de coaptation vers l’avant générant une diminution de la surface de coaptation voire un défaut de coaptation
Les insuffisances tricuspides organiques ont un aspect spécifique en fonction de la cause (tableau 4.8)
Doppler cardiaque : quantification de l’IT
Il est important de noter que le degré d’insuffisance tricuspide est fortement dépendant des conditions de charge et qu’il faut savoir répéter les évaluations notamment après déplétion hydrosodée.
Le mode Doppler couleur permet de mesurer :
- le diamètre du jet de la vena contracta qui correspond à la portion la plus étroite du jet de régurgitation en aval de l’orifice tricuspide. Une valeur de vena contracta ≥ 7 mm définit une insuffisance tricuspide sévère ;
- le rayon de la zone de convergence hémisphérique (r).
Le Doppler continu permet de mesurer la Vmax et l’ITV tricuspide.
Ceci permet les calculs suivants : débit régurgitant (Qr), surface de l’orifice régurgitant (SOR), volume régurgitant (VR) = SOR x ITV, fraction de régurgitation (FR)
Une insuffisance tricuspide sévère est définie par une SOR supérieure à 40 mm2 et un volume régurgitant supérieur à 45 ml.
Le retentissement de l’insuffisance tricuspide est évalué sur la dilatation des cavités droites (oreillette et ventricule droits, anneau tricuspide, veine cave inférieure, veines sus-hépatiques) et l’altération de la fonction systolique du ventricule droit
Il est essentiel de rechercher et de quantifier d’autres valvulopathies associées, en particulier mitrales et aortiques.
Autres examens en fonction du contexte
Échocardiographie transœsophagienne
L’ETO est rarement indiquée dans l’exploration des valvulopathies droites (position antérieure de la valve tricuspide). Elle est utile pour caractériser certains mécanismes et causes : endocardites, traumatique, malposition de pace-maker, etc.
Imagerie en coupe
En cas d’insuffisance tricuspide sévère avec évaluation sous-optimale en ETT bidimensionnelle, on peut également utiliser l’IRM cardiaque (examen de référence) ou l’ETT tridimensionnelle qui permet une meilleure évaluation des dimensions et de la fonction des cavités droites.
Modalités thérapeutiques (fig. 4.20)
Le traitement d’une pathologie responsable d’une insuffisance tricuspide secondaire peut permettre la régression de la régurgitation.
________________________________________________________________________________
Figure 4.20. Algorithme de prise en charge des IT (recommandation 2017 de l’ESC).
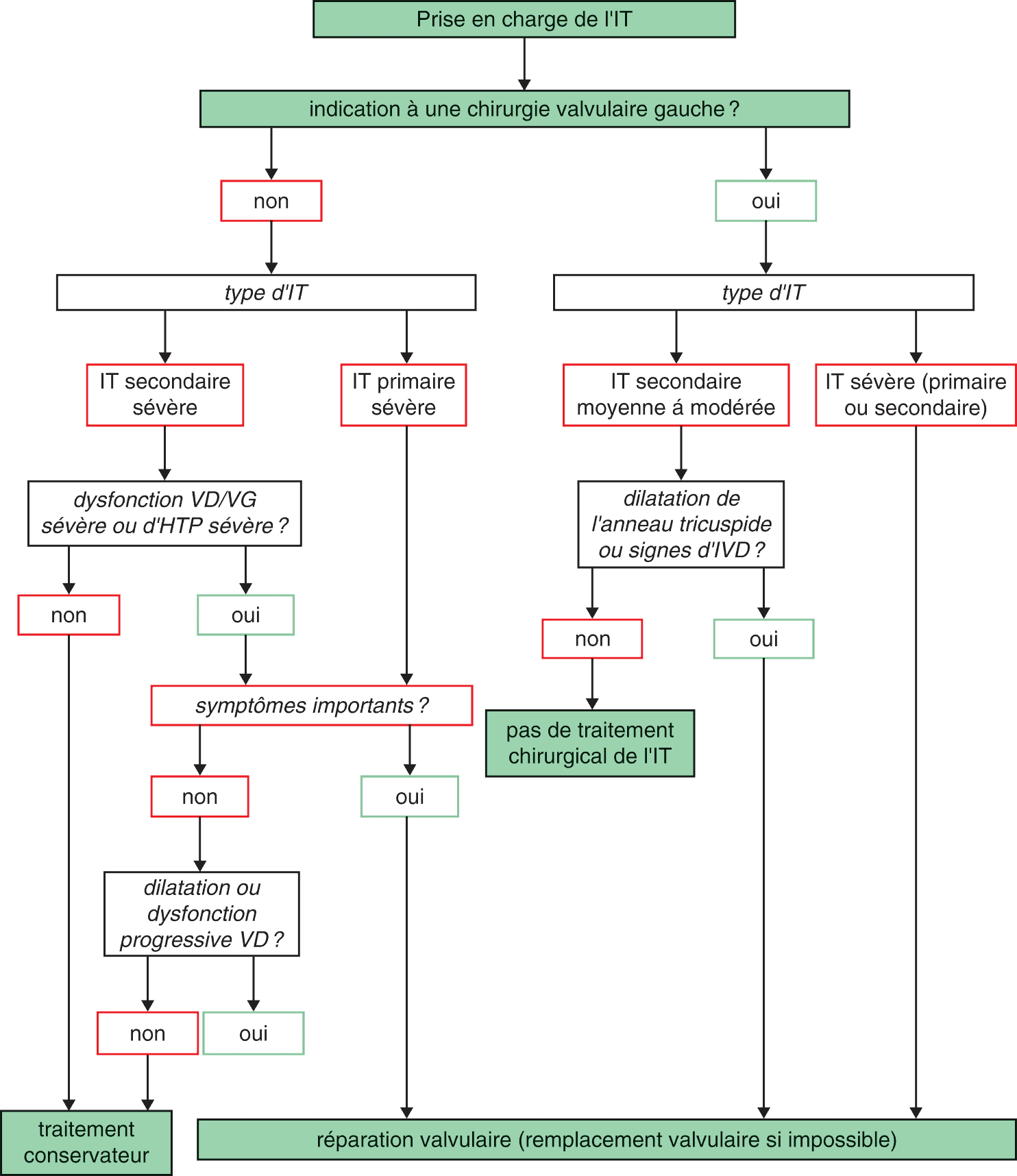
Source : Baumgartner H. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Europ Heart J 2017; 38: 2739–2791.
________________________________________________________________________________
Les diurétiques en association avec une restriction hydrique et sodée permettent une régression des œdèmes.
La correction de la régurgitation tricuspide est la seule modalité efficace dans le traitement des formes symptomatiques.
Les deux techniques envisageables sont la plastie valvulaire (chirurgie conservatrice), qui doit être privilégiée à chaque fois que la situation le permet, et le remplacement valvulaire tricuspide par bioprothèse ou prothèse mécanique (exceptionnellement), plus rarement retenu. L’émergence des techniques de correction par voie percutanée pourrait contribuer à élargir les indications des gestes isolés sur la valve tricuspide.
________________________________________________________________________________
Valvulopathies médicamenteuses
Étiopathogénie
Les valves excisées ont un aspect blanc, avec à l’histologie, un processus infiltrant concernant les feuillets valvulaires et les cordages tendineux, similaires aux lésions décrites dans le carcinoïde, secondaire à la sécrétion d’amines vaso-actives.
Les médicaments rendus responsables d’une atteinte valvulaire ont une activité de stimulation des récepteurs sérotoninergiques, en particulier la 5-hydroxytryptamine (5-HT) 2B récepteur à la sérotonine. La stimulation des récepteurs 5-HT 2B serait une cause authentifiée de valvulopathie
Causes
- Dérivés de l’alcaloïde, ergotamine et méthysergide.
- Fenfluramine et dexfenfluramine (anorexigènes).
- Agonistes dopaminergiques dérivés de l’ergot, pergolide, et cabergoline.
- MDMA pour 3,4-Methyl enedioxy méthamphétamine.
Prévalence
La prévalence des atteintes valvulaires médicamenteuses est diversement appréciée. Les études rapportent une prévalence variable, peut-être surestimée de 10 à 20 % après consommation d’anorexigènes.
Les facteurs associés à une prévalence accrue de l’atteinte valvulaire sont la durée du traitement, l’utilisation d’associations médicamenteuses. La prévalence de l’atteinte valvulaire est particulièrement élevée lorsque le médicament a été consommé plus de six mois.
Diagnostic clinique
L’atteinte valvulaire régurgitante est prépondérante, pouvant toucher la valve aortique, mitrale ou tricuspide. L’atteinte valvulaire tricuspide est fréquente mais il faut noter que les dérivés de l’ergot peuvent affecter les valves gauches, à l’origine d’une régurgitation valvulaire significative.
L’atteinte aortique régurgitante est rapportée avec une fréquence élevée chez les patients ayant consommé des anorexigènes, comparativement aux autres localisations valvulaires.
Diagnostic morphologique
L’échographie cardiaque décrit des lésions proches des lésions rhumatismales ou liées à un carcinoïde avec un épaississement des feuillets valvulaires, un aspect en dôme de la valve mitrale et un épaississement des valves aortique et tricuspide. Malgré l’aspect restrictif de la cinétique valvulaire, la sténose valvulaire est rare, contrairement à ce qui est observé dans le carcinoïde.
________________________________________________________________________________
Rétrécissement (sténose) mitral(e) (RM) (hors programme)
Voir vidéo 4.7, vidéo 4.8.
Voir vidéo 4.7, vidéo 4.8.
La description précise de la sévérité de l’atteinte des différents éléments constitutifs de l’appareil valvulaire mitral est indispensable à la décision médico-interventionnelle (commissurotomie mitrale percutanée ou remplacement valvulaire par prothèse valvulaire).
Mécanisme
La sténose mitrale réalise un défaut d’ouverture valvulaire mitrale en imagerie bidimensionnelle ou en échocardiographie tridimensionnelle en temps réel. La description précise de la sévérité de l’atteinte des différents éléments constitutifs de l’appareil valvulaire mitral est indispensable à la décision médico-interventionnelle. La surface mitrale diminue de 0,1 à 0,3 cm2 par an.
Il réalise une fusion des commissures, une rétraction des feuillets et des cordages ; les lésions sont plus ou moins associées et réalisent une diminution permanente de calibre de l’orifice mitral. L’association de ces différentes lésions avec la fibrose, la calcification des feuillets valvulaires et la rétraction de l’appareil sous valvulaire réalisent un rétrécissement de l’orifice mitral en forme d’entonnoir ou de bouche de poisson.
Chez un adulte normal, l’orifice mitral a une surface de 4 à 6 cm2. La pression auriculaire gauche augmente lorsque la surface mitrale atteint 2 cm2 et de façon significative lorsque la surface orificielle est inférieure à 1,5 cm2.
Épidémiologie
Pathologie devenue très rare dans les pays développés (prévalence de 0,02 à 0,2 %), le RM a une prévalence élevée dans les pays en voie de développement du fait de son association avec le rhumatisme articulaire aigu (RAA). Un quart des patients ayant un rhumatisme articulaire aigu développent un RM pur (5 à 20 ans après la poussée initiale) et 40 % supplémentaires ont une maladie mitrale. Les deux tiers des patients ayant eu un rhumatisme articulaire aigu sont des femmes.
Physiopathologie
Augmentation de la pression auriculaire gauche
L’oreillette gauche se distend progressivement avec épaississement de l’endocarde auriculaire responsable de l’hypertrophie auriculaire notée à l’électrocardiogramme et à l’échocardiographie ; la dilatation favorise la stase sanguine et donc la thrombose intra-auriculaire gauche (en particulier dans l’auricule gauche).
La tachycardie diminue la période de remplissage diastolique du ventricule gauche. L’apparition d’une fibrillation atriale (FA) fait disparaître la composante atriale, diminue le débit cardiaque d’au moins 20 % et augmente la pression auriculaire gauche.
La tachycardie et la FA rapide augmentent de façon importante le gradient de pression à travers l’orifice mitral nécessaire au maintien du débit cardiaque ; elles sont souvent responsables de l’apparition des signes congestifs.
Lors de l’exercice physique, les symptômes de congestion pulmonaire sont également présents du fait de l’augmentation du gradient transvalvulaire (épreuve d’effort, échocardiographie d’effort).
Hypertension artérielle pulmonaire
Initialement, les résistances artérielles pulmonaires sont normales avec une faible élévation de la pression artérielle pulmonaire (PAP) et un maintien du gradient pression artérielle pulmonaire – pression capillaire pulmonaire < 10 mmHg.
La PAP et la pression capillaire pulmonaire augmentent de façon parallèle, réalisant une hypertension artérielle pulmonaire post-capillaire.
Plus tardivement, l’apparition d’une hypertension artérielle pulmonaire précapillaire avec gradient pression artérielle pulmonaire-pression capillaire pulmonaire > 15 mmHg du fait du développement d’une artériolite pulmonaire.
L’hypertension artérielle pulmonaire sévère est tardive (PAP moyenne > 40 mmHg), responsable d’une insuffisance ventriculaire droite. La dilatation des cavités droites prédomine (oreillette droite) du fait d’une insuffisance tricuspide associée (plus fréquemment fonctionnelle qu’organique), aggravée par la FA.
À l’état basal, le débit cardiaque est normal ou diminué.
À l’effort, il augmente insuffisamment par rapport à la consommation d’oxygène (évaluation possible par échocardiographie-Doppler lors d’un effort).
Le ventricule gauche est normal, en dehors d’une valvulopathie régurgitante (insuffisance mitrale ou insuffisance aortique) ou d’une cardiomyopathie associée.
Diagnostic
Signes fonctionnels
Ils sont inconstants :
- dyspnée d’effort à chiffrer (classification fonctionnelle NYHA), palpitations ;
- à l’occasion parfois d’une complication révélatrice d’un œdème pulmonaire ou équivalent mineur survenant à l’effort ;
- hémoptysie ; embolie systémique (10 à 20 % des RM se compliquent d’une embolie artérielle au cours de l’évolution) ; FA ; insuffisance cardiaque droite plus tardive (HTAP, IT, défaillance ventriculaire droite).
Signes d’examen clinique
Inspection
Le faciès mitral typique (pommettes rouges chez une patiente chétive) est exceptionnel
Palpation de l’aire précordiale
Frémissement cataire apexien diastolique, éclat palpable du B1 (en l’absence de calcifications massives).
Auscultation des foyers cardiaques
Temps essentiel de l’examen clinique.
- Technique rigoureuse : au repos puis après un effort modéré, patient assis puis en décubitus latéral gauche.
- Sémiologie apexienne respectant la systole : la triade affirme le diagnostic (rythme de Durozier) :
- roulement diastolique : maximum à l’apex, irradiant peu ; Séparé de B2 par un intervalle silencieux ; d’emblée maximum, decrescendo ; Avec renforcement présystolique en rythme sinusal (disparition en fibrillation auriculaire) ; Intensité variable, timbre rude et tonalité basse ;
- éclat de B1 (valves souples) réalisant un bruit sec, éclatant et vibrant ;
- claquement d’ouverture de la mitrale (valves souples).
Cependant, la sémiologie est souvent incomplète ou atténuée. L’auscultation sera reprise, éventuellement après ralentissement chez des patients tachycardes ou en FA rapide.
- L’auscultation des autres foyers est systématique :
- à la base, recherche des signes d’hypertension artérielle pulmonaire (éclat de B2 au foyer pulmonaire), et plus rarement d’un souffle diastolique pulmonaire (souffle de Graham-Steel) ;
- à la xiphoïde, recherche d’une insuffisance tricuspide associée (signe de Carvalho).
Auscultation des deux champs pulmonaires
- Recherche des signes d’œdème pulmonaire.
- L’examen clinique doit être complet.
Examens complémentaires
Électrocardiogramme
- Rythme sinusal normal fréquent.
- FA fréquente au cours de l’évolution (à haut risque embolique), extrasystoles auriculaires.
- Hypertrophie auriculaire gauche, d’apparition inconstante et plus tardive : P > 0,1 s ; P1 > P2 > P3.
- Aspect bifide en D1-D2-V5-V6 et diphasique avec négativité prédominante en V1-V2.
- Hypertrophie-dilatation ventriculaire droite R/S > 1 en V1-V2.
Radiographie du thorax
- Clichés de face et de profil.
- parfois le cœur est de taille normale (mesure du rapport cardio-thoracique) ;
- la silhouette mitrale typique est peu fréquente sauf dans les formés évoluées et anciennes ;
- de face, silhouette triangulaire avec : arc moyen rectiligne, convexe, parfois aspect en double bosse correspondant à la saillie de l’oreillette gauche.
- Oreillette gauche dilatée : double contour concentrique voire festonné avec au maximum une oreillette gauche énorme formant tout le bord droit du cœur.
- Recherche de signes d’œdèmes interstitiel et/ou alvéolaire
Échocardiographie Doppler
L’échocardiographie Doppler est l’examen clé permettant :
- de rattacher une sémiologie non évocatrice à un rétrécissement mitral ;
- une description précise de l’anatomie valvulaire et des lésions valvulaires associées (aortique, tricuspide), indispensables à la discussion thérapeutique. Il peut être facilement réalisé et répété mais exige un opérateur entraîné ;
- de quantifier le degré de sténose, son retentissement (OG, VD) et sa tolérance (PAP, RAP, débit cardiaque) ;
- la surveillance évolutive (avant et après une commissurotomie mitrale percutanée).
Échocardiographie bidimensionnelle, 3D et en mode M
- Épaississement et/ou calcification des feuillets valvulaires dont on précise l’épaississement, le degré de souplesse (aspect en « genou fléchi ») et la mobilité (mouvement « en fléau » de la valve antérieure et immobilité de la valve postérieure avec réduction de l’ouverture diastolique mitrale) ; fusion des commissures ;
- Planimétrie soigneuse de l’orifice mitral permettant d’évaluer la surface mitrale anatomique ;
- État de l’appareil sous valvulaire : épaississement, calcification et rétraction valvulaire, longueur des cordages, recherche de calcifications de l’anneau (RM vieilli ou dégénératif).
Doppler cardiaque
- Quantification de la sévérité du rétrécissement mitral : planimétrie de l’orifice mitral (3D), gradient transvalvulaire OG-VG, surface par équation de continuité
- Quantification du retentissement et de la tolérance du rétrécissement mitral : volume OG, taille des cavités droites, PAP, RAP, Qc
- Signes échocardiographiques-Doppler d’une valvulopathie associée :
- recherche et quantification d’une valvulopathie aortique associée (insuffisance aortique dans 1/3 des cas) ;
- recherche et quantification d’une insuffisance tricuspide (IT) dont on précise : le caractère organique (feuillets épaissis) ou fonctionnel avec dilatation prédominante de l’anneau tricuspide. La mesure de sa taille aide à poser les indications d’une annuloplastie chirurgicale lors du geste curatif sur le rétrécissement mitral.
Autres examens échographiques en fonction du contexte
- Échocardiographie transœsophagienne (ETO) : préalable à toute décision opératoire (CMP ; en cas d’accident embolique ou de difficulté de quantification du degré de sténose mitrale et/ou du volume de la régurgitation mitrale associée).
- Échocardiographie d’effort ; en cas de RM asymptomatique et en cas de discordance entre le retentissement fonctionnel et les paramètres hémodynamiques au repos
Histoire naturelle et évolution
Les accidents évolutifs du rétrécissement mitral sont graves, engageant parfois le pronostic vital à brève échéance. Ils marquent un tournant évolutif, traduisant l’existence d’un rétrécissement mitral serré, indication à une commissurotomie mitrale percutanée ou à un traitement chirurgical en fonction de l’état anatomique des lésions valvulaires mitrales, de l’âge, du terrain et des souhaits du patient.
Complications liées au retentissement sur la circulation d’amont
Hyperpression dans la petite circulation corrélée au degré de sténose valvulaire mitrale et à la pression dans l’oreillette gauche : dyspnée d’effort à quantifier ; OAP, épisodes infectieux récidivants, embolie pulmonaire. L’hypertension artérielle pulmonaire précapillaire est tardive, à l’origine des signes d’insuffisance ventriculaire droite.
Accidents atriaux gauches
Une embolie systémique en particulier cérébrale survient dans 20 % des cas de EM ; elle est favorisée par les troubles du rythme atriale (présents dans 80 % des cas) et la dilatation atriale gauche, facteur de stase (contraste spontané à l’échocardiographie transœsophagienne dans 70 % des RM serrés).
Troubles du rythme atrial fréquents : FA, flutter, tachycardie atriale, qui imposent le traitement anticoagulant (AOD contre-indiqués, uniquement HBPM temporaire puis AVK), indiquées en cas de RM avec dilatation de l’OG > 50 mm (mode M échographique).
Embolies artérielles
Elles sont secondaires à la thrombose auriculaire gauche (10-20 % des cas, localisées dans l’auricule gauche dans 91 % des cas), favorisées par :
- le passage en FA et la dilatation de l’oreillette gauche ;
- la stase sanguine dans l’oreillette et surtout l’auricule gauche et la perte mécanique de la fonction auriculaire.
Elles affectent tous les territoires en particulier cérébral (50 % des embolies), rénal, splénique, mésentérique, membres inférieurs, rétine. Ces embolies sont multiples et récidivantes dans un quart des cas.
Le risque embolique justifie la réalisation systématique d’une échocardiographie transœsophagienne avant toute tentative de cardioversion médicamenteuse ou électrique, en présence d’une valvulopathie mitrale (fig. 4.21).
________________________________________________________________________________
Valvuloplastie (ou commissurotomie) mitrale percutanée
Principe
Les modalités sont comparables à celles de la commissurotomie mitrale chirurgicale : ouverture des symphyses commissurales ± fracture des calcifications valvulaires.
Deux techniques sont utilisables et réalisées sous anesthésie locale (+ voie veineuse) :
- le cathétérisme transeptal est le plus répandu, en l’absence de contre-indications ;
- le cathétérisme artériel rétrograde est moins diffusé du fait du risque majoré de complications (abord artériel, insuffisance mitrale, etc.).
La technique de dilatation est, au mieux, choisie par les centres spécialisés :
- ballon d’Inoue, auto-positionnable, extensible à la pression, d’utilisation simple et permettant des inflations progressives. Cette procédure est rapide et sûre (moindre taux de complications) ;
- double ballon, nécessitant deux procédures (technique moins utilisée) ;
- la taille du ballon est adaptée au patient ;
- la durée de la procédure est de 60 à 90 min.
Surveillance hospitalière
- Avant la procédure :
-
- vérifie l’absence de contre-indications ;
- confrontation avec les échographistes pour la description précise de l’anatomie valvulaire ;
- traitement anticoagulant efficace par héparine (relais AVK-héparine) ;
- informer le patient des avantages et risques.
- En cours de procédure : contrôles hémodynamiques (et éventuellement échocardiographiques).
- Au décours immédiat de la procédure, surveillance clinique, biologique et échocardiographique.
Clinique
Points de ponction veineux et artériel, auscultation cardiopulmonaire, etc.
Biologique
Hémostase (traitement anticoagulant par héparine à doses efficaces), hémogramme, ionogramme et fonction rénale.
Échocardiographie Doppler
Succès de la procédure (surface, gradients), insuffisance mitrale (quantification), communication inter-auriculaire, etc.
Une ETO de contrôle est parfois préconisé (24-48e heure).
Contre-indications
- Thrombose intra-auriculaire gauche (échocardiographie par voie transœsophagienne systématique).
- Fuite mitrale volumineuse au moins de volume modéré.
- Surface valvulaire mitrale > 1,5 cm2.
- Absence de fusion commissurale.
- Coronaropathie associée nécessitant un pontage aorto-coronaire.
- Contre-indication au cathétérisme trans-septal (cyphoscoliose).
- Oreillette gauche ectasique.
- Embolie ou accident hémorragique récents.
- Calcifications massives des valves et des commissures du fait du risque de déchirure para-valvulaire.
- Valvulopathie aortique sévère associée.
- Maladie tricuspide sévère.
Complications immédiates
- Thrombo-emboliques (0,5 à 5 %) :
-
- accidents vasculaires cérébraux transitoires par embolie ;
- plus rarement embolie gazeuse.
- Insuffisance mitrale volumineuse (> modérée) dans 2 à 10 % des cas.
- Communication interauriculaire (< 10 % en oxymétrie, > 50 % en Doppler couleur), résolutive en moins d’un an dans 70 % des cas.
- Hémopéricarde : 1 %.
- Décès : 0,5 %.
- Locales : 1 %.
- Arythmies : 1 %.
- Thrombose veineuse profonde et embolie pulmonaire (un cathétérisme veineux fémoral est effectué pour réaliser le cathétérisme trans-septal).
Résultats
- Immédiats : entre des mains expertes dans des centres spécialisés, le gradient de pression diminue de 50 %. La surface mitrale augmente de 50-100 % et le débit cardiaque de 80 %. Les pressions pulmonaires diminuent dans des délais variables. Le résultat initial est très influencé par le degré initial d’altération de l’appareil valvulaire et sous-valvulaire mitral.
- À distance :
-
- l’amélioration fonctionnelle se maintient à 1 an dans 90 % des cas ;
- le taux de resténose est faible : 10 à 20 % à 5 ans, dépendant étroitement de l’anatomie valvulaire et du résultat initial ;
- la survie à 5 ans est > 95 %.
- Facteurs prédictifs du résultat :
-
- âge ;
- anatomie valvulaire (absence de calcifications, mobilité valvulaire, degré de sténose, etc.) ;
- antécédents de commissurotomie chirurgicale ;
- gain initial post-commissurotomie.
Indications
- Patient symptomatique avec caractéristiques anatomiques favorables à la commissurotomie mitrale percutanée.
- Patient symptomatique avec contre-indication à la chirurgie ou risque chirurgical élevé.
- Traitement initial chez un patient symptomatique avec anatomie défavorable et absence de caractéristiques cliniques défavorables.
- Patient asymptomatique avec caractéristiques favorables* et haut risque thromboembolique ou haut risque de décompensation hémodynamique :
- Antécédent d’embolie.
- Contraste spontané dense dans l’oreillette gauche (état préthrombotique).
- Fibrillation atriale récente ou paroxystique.
- PAPs > 50 mmHg.
- Nécessité de chirurgie non cardiaque majeure.
- Désir de grossesse.
Surveillance ultérieure
- Examens clinique, électrocardiographique, radiologique.
- Surveillance de l’hémostase en cas de traitement par les AVK (INR tous les 15 jours puis tous les mois).
- Examen échocardiographique-Doppler annuel initialement permettant :
-
- de mesurer le gradient transmitral ;
- d’évaluer la surface fonctionnelle ;
- de surveiller l’insuffisance mitrale ;
- de surveiller une éventuelle communication interauriculaire (rarement significative).
________________________________________________________________________________
Évaluation préthérapeutique (confrontation médico-chirurgicale, « Heart Team »)
Évaluation de la sévérité de la valvulopathie
Elle se fait actuellement essentiellement sur les données cliniques et de l’échocardiographie avec Doppler. La symptomatologie fonctionnelle dépend du type et de la sévérité de la valvulopathie aortique et/ou mitrale.
Clinique
- Signes fonctionnels d’effort : insuffisance ventriculaire gauche, angor, syncope, embolie artérielle.
- Caractéristiques du souffle.
- Présence d’un galop (B3).
Électrocardiogramme
- Hypertrophie ventriculaire gauche (valvulopathies aortiques, régurgitation mitrale chronique).
- Hypertrophie atriale gauche (valvulopathies mitrales).
Radiographie de thorax
- Rapport cardiothoracique (normal (< 0,5) en cas de rétrécissement aortique, augmenté > 0,5 de façon variable en cas de régurgitation et/ou de dilatation du ventricule gauche et de l’atrium gauche à un degré moindre).
- Vascularisation pulmonaire (œdème interstitiel et/ou alvéolaire en cas d’insuffisance cardiaque congestive).
Échocardiographie transthoracique et transœsphagienne, bidimensionnelle et 3D
- Degré et type d’hypertrophie ventriculaire gauche en l’absence d’autres causes d’hypertrophie ventriculaire gauche (HTA) : détermination de la masse ventriculaire gauche indexée, épaisseur pariétale relative.
- Dilatation du ventricule gauche (volume et diamètres augmentés, en cas de valvulopathies régurgitantes hémodynamiquement significatives).
- Dilatation de l’atrium gauche (en cas de valvulopathies mitrales significatives, de fibrillation atriale ou d’élévation des pressions de remplissage VG).
- Détermination de la FEVG (2D, méthode de Simpson biplan, 3D plus fiable mais de réalisation parfois difficile chez les patients peu échogènes).
Doppler cardiaque
- Surface valvulaire (anatomique, mesurée en planimétrie ; fonctionnelle, déterminée en couplant échocardiographie et Doppler) en cas de sténose valvulaire.
- Gradient moyen transvalvulaire en cas de sténose (ventricule gauche-aorte en cas de rétrécissement aortique ; atrium gauche-ventricule gauche en cas de sténose mitrale).
- Surface de l’orifice régurgitant (SOR) et volume régurgitant (VR) en cas de régurgitations (méthode de la PISA).
- Pressions pulmonaires (systolique, diastolique, moyenne et résistances pulmonaires), débit cardiaque (indexé).
Cathétérisme cardiaque (± angiographies)
Ses indications sont devenues rares car remplacées par l’hémodynamique Doppler.
Les injections de contraste iodé dans les cavités cardiaques (aorte pour quantifier une régurgitation aortique, ventriculaire gauche pour quantifier une régurgitation mitrale) sont d’indication exceptionnelle.
Coronarographie
Elle dépiste des lésions coronaires significatives (> 50 % de réduction de diamètre).
Elle reste indiquée en préopératoire dans les cas suivants :
- patients âgés de plus de 40 ans et femmes ménopausées ;
- dysfonction systolique ventriculaire gauche ;
- patients présentant un angor (examen coronarographique systématique) ou des arguments paracliniques pour une ischémie myocardique ;
- patients présentant des facteurs de risque cardiovasculaire (≥ 2).
Recherche de foyers infectieux
- Interrogatoire soigneux à la recherche d’une fièvre inexpliquée, d’un foyer infectieux récent négligé.
- Consultation ORL après radiographie (ou scanner) des sinus.
- Consultation stomatologique après panoramique dentaire (radiographie ou scanner).
- Consultation gynécologique et/ou néphrologique en cas de signes d’appel.
- Recherche de bactéries multirésistantes (BMR) par écouvillonnage nasal.
Examen clinique général
- Recherche d’un angor, d’une pathologie artérielle périphérique, de facteurs de risque de l’athérosclérose.
- Recherche d’antécédents d’ulcère gastroduodénal, d’insuffisance respiratoire, d’insuffisance rénale, de diabète.
- Traitements en cours (diurétiques, vasodilatateurs, digitaliques).
Examens biologiques
- Groupe, Rhésus, agglutinines.
- Ionogrammes sanguin et urinaire, urée et créatinine plasmatiques, clairance de la créatinine (Cockcroft, MDRD, CKD-EPI).
- Hémogramme, plaquettes, CRP.
- Biologie phosphocalcique.
- Glycémie, cholestérol total et fractions, triglycérides.
- INR, TCA, fibrinogène.
- Sérologie VIH (patient prévenu et consentant).
- Sérologies hépatites A, B, C.
Autres examens orientés par le contexte
Écho-Doppler cervical
Indications larges :
- antécédents neurovasculaires (AVC/AIT) ;
- facteurs de risques athéromateux (≥ 2) ;
- âge > 50 ans ;
- mise en évidence d’autres localisations de la maladie athéroscléreuse.
Échographie-Doppler des membres inférieurs et de l’aorte abdominale
Il est indiqué avant le cathétérisme artériel en présence d’un souffle iliaque ou fémoral ou d’une claudication intermittente en cas de symptomatologie évocatrice d’une artériopathie oblitérante des membres inférieurs ou de la présence d’un souffle fémoral ou de façon systématique chez les patients diabétiques ou ayant au moins deux facteurs de risque vasculaire.
En cas de remplacement percutané de la valve aortique (TAVI), l’échographie-Doppler est systématiquement complétée par un angioscanner de l’aorte abdominale et des axes artériels, qui guide le choix de la voie d’abord.
Épreuves fonctionnelles respiratoires, gazométrie artérielle (systématiques)
Ces examens permettent de détecter une insuffisance respiratoire, dont le type et la sévérité seront caractérisés. La détection d’une hypoventilation alvéolaire et de ses conséquences permet de planifier les soins postopératoires et rarement de récuser l’indication chirurgicale (VEMS < 1 litre), privilégiant alors un geste percutané, s’il est faisable.
Consultation anesthésique
Au terme d’un examen non invasif, il est possible de poser les indications du traitement adapté à chaque patient.
Les explorations ultrasonores et l’examen général suffisent le plus souvent à porter une indication opératoire discutée lors d’une confrontation médico-chirugicale (Heart Team). Les examens invasifs sont programmés en fonction de la décision et des résultats de l’investigation initiale.
________________________________________________________________________________
Figure 4.21. Algorithme de prise en charge du RM (recommandations 2017 de l’ESC).
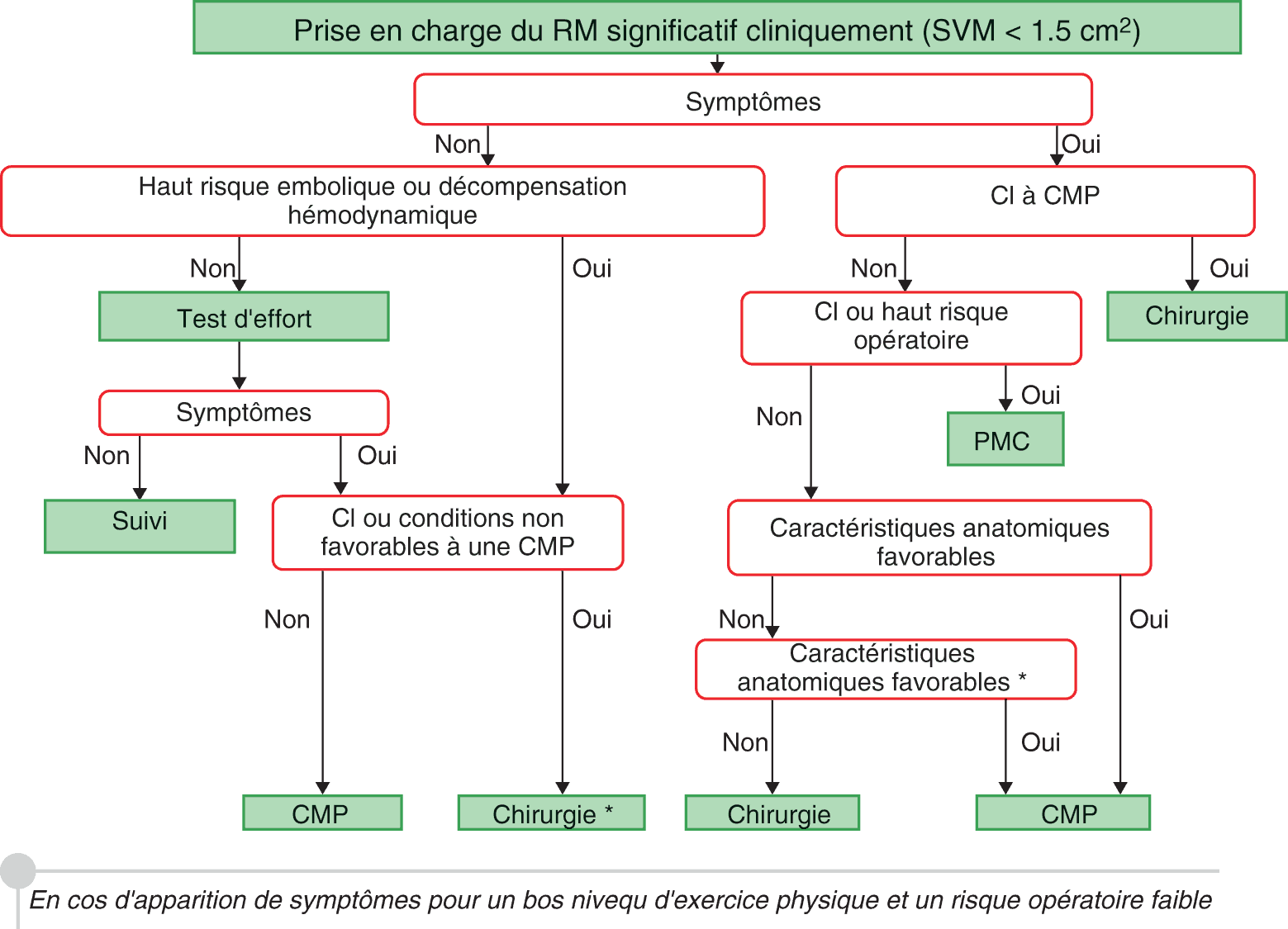
________________________________________________________________________________
Synthèse
Voir tableaux 4.9 à 4.11.
Tableau 4.9. Caractéristiques physiopathologiques et de l’examen physique dans les principales valvulopathies gauches.
| Rétrécissement aortique | Insuffisance aortique | Insuffisance mitrale | |
| Physiopathologie | Hypertrophie ventriculaire gauche concentrique liée à une élévation de la post-charge selon la loi de Laplace entraînant une dysfonction diastolique. | Dilatation ventriculaire gauche et hypertrophie ventriculaire | Dilatation ventriculaire gauche liée à une élévation de la pré-charge selon la loi de Franck-Starling entraînant une dysfonction systolique |
| Signes fonctionnels | Syncope
Angor Dyspnée |
Angor
Dyspnée |
Dyspnée |
| Signes physiques | PA pincée | PA élargie
Hyperpulsatilité |
Choc de pointe dévié à gauche en dôme de Bard |
Tableau 4.10. Caractéristiques différentielles de l’auscultation des valvulopathies aorto-mitrales.
| Rétrécissement aortique | Insuffisance aortique | Insuffisance mitrale | Rétrécissement mitral | |
| Position d’examen | Assis, penché en avant, expiration | Assis, penché en avant, bras levés expiration | Décubitus latéral gauche | Décubitus latéral gauche |
| Type | Éjectionnel | Holodiastolique | Régurgitation | Roulement |
| Temps | Systolique (maximum en mésosystole) | Diastolique | Systolique | Diastolique |
| Au cours du cycle | Mésosystolique | Decrescendo
Maximum protodiastolique |
Holosystolique
Pas de variation |
Decrescendo à renforcement présystolique |
| Variation après diastole longue | Importante majoration | Aucune | Aucune | Aucune |
| Foyer max | Foyer aortique | Foyer aortique | Apexo-axillaire | Apexo-axillaire |
| Siège | Second espace intercostal droit | Bord gauche sternal | Pointe (irradiations) | Pointe (irradiations) |
| Timbre | Rude, râpeux | Doux, humé, aspiratif | Jet de vapeur (musical, piaulant) | Roulant |
| Intensité | Variable, souvent intense | Souvent modérée | Variable | Variable |
| Irradiation | Ascendante vers les carotides | Descendante vers la pointe | Vers l’aisselle (parfois la base) | |
| Signes d’accompagnement | Souffle éjectionnel de débit | Éclat de B1, claquement d’ouverture mitrale
– Roulement diastolique – Éclat du B2 |
||
| Critères de sévérité | Abolition du B2 | Pistol-Shot mésosystolique sous clavier droit
click protosystolique Roulement diastolique de Flint – B3 surajouté |
B3, éclat de B2 par HTAP, roulement mésodiastolique | Claquement d’ouverture mitrale très proche du B2 |
| Diagnostic différentiel | Souffle de débit, insuffisance mitrale, communication interventriculaire, rétrécissement pulmonaire
RA sous valvulaire RA supra-valvulaire |
Frottement péricardique | Rétrécissement aortique
Frottement péricardique |
Roulement de Flint |
Tableau 4.11. Place des examens complémentaires et principales indications opératoires dans les principales valvulopathies gauches.
| Rétrécissement aortique | Insuffisance aortique | Insuffisance mitrale | |
| ECG | HVG systolique (indice de Sokolow positif associé à des ondes T négatives en V5-V6). Hypertrophie auriculaire gauche (onde P bifide en DII, diphasique en V1, > 120 ms). | HVG diastolique (indice de Sokolow positif associé à des ondes T positives en V5-V6) | Hypertrophie auriculaire gauche (Onde P bifide en DII, diphasique en V1, > 120 ms)
HVG diastolique (indice de Sokolow positif associé à des ondes T positives en V5-V6) |
| Radiographie thoracique
(la silhouette cardiaque peut être normale) |
Dilatation possible de l’aorte ascendante
± Cardiomégalie Possibles calcifications radio-opaques de la valve aortique |
Arc supérieur droit dilaté du fait de la dilatation de l’aorte ascendante
-Concavité de l’arc moyen gauche plus marquée. Arc inférieur gauche élargi secondairement à l’HVG. Cardiomégalie (en cas de dilatation du VG) ± Surcharge pulmonaire |
« Silhouette mitrale »
Accentuation de la convexité de l’arc moyen gauche par dilatation de l’atrium gauche Double contour de l’arc inférieur droit également lié à la dilatation de l’atrium gauche Arc inférieur gauche accentué par la dilatation du ventricule gauche Cardiomégalie ± Surcharge pulmonaire |
| Critères échocardiographiques de sévérité | Gradient moyen > 40 mmHg
Vmax > 4 m/s Surface aortique < 1 cm2 ou < 0,6 cm2/m2 |
Surface de l’orifice régurgitant (SOR) > 30 mm2.
Volume régurgité > 60 ml. |
Surface de l’orifice régurgitant (SOR) > 40 mm2.
Volume régurgité > 60 ml. |
| Indications chirurgicales simples | Rétrécissement aortique sévère associé à au moins un des critères suivants :
Signe fonctionnel FEVG < 50 % Épreuve d’effort positive (contre-indiqué en cas de symptômes) |
Insuffisance aortique sévère associée à au moins un des critères suivants :
DTSVG > 50 mm (diamètre télésystolique du ventricule gauche). DTDVG > 70 mm (diamètre télédiastolique du ventricule gauche). FEVG < 50 %. |
Insuffisance mitrale sévère associée à au moins un des critères suivants :
Signes fonctionnels. FEVG < 60 %. DTSVG > 45 mm (diamètre télésystolique du ventricule gauche). PAPs > 50 mmHg. FA récente. |
Endocardite infectieuse (EI)
Définitions et notions épidémiologiques
Il s’agit d’une infection d’une ou plusieurs valves cardiaques (plus rarement de l’endocarde pariétal) par un micro-organisme (bactérie le plus souvent, plus rarement un germe intracellulaire ou levure).
Les endocardites touchent le plus souvent les valves du cœur gauche, c’est-à-dire les valves aortique et mitrale (atteinte aortique plus fréquente que mitrale), plutôt que la valve tricuspide (toxicomanie intraveineuse, stimulateurs et défibrillateurs cardiaques).
L’incidence annuelle de l’endocardite est estimée à 1 500 cas par an, plus élevée chez les hommes que chez les femmes et maximale après 75 ans.
Physiopathologie
L’endocardite infectieuse est initiée par une bactériémie survenant sur une valve native normale ou, plus souvent, pathologique. L’endocardite résulte d’interactions complexes entre le micro-organisme, l’endothélium valvulaire et la réaction immunitaire de l’hôte. L’agrégation plaquettaire précoce forme un thrombus colonisé par les micro-organismes.
La végétation est un thrombus infecté dont la principale complication est le risque embolique qui augmente avec la taille de la végétation. Les embolies sont le plus souvent cérébrales pour les endocardites du cœur gauche et pulmonaires pour les endocardites du cœur droit.
L’autre conséquence principale de l’endocardite infectieuse est le développement de lésions valvulaires (déchirures, perforations) à l’origine de régurgitations aiguës (fig. 4.22), ou péri-valvulaires
________________________________________________________________________________
Figure 4.22. Algorithme de prise en charge d’une endocardite infectieuse (recommandations 2015 de l’ESC).
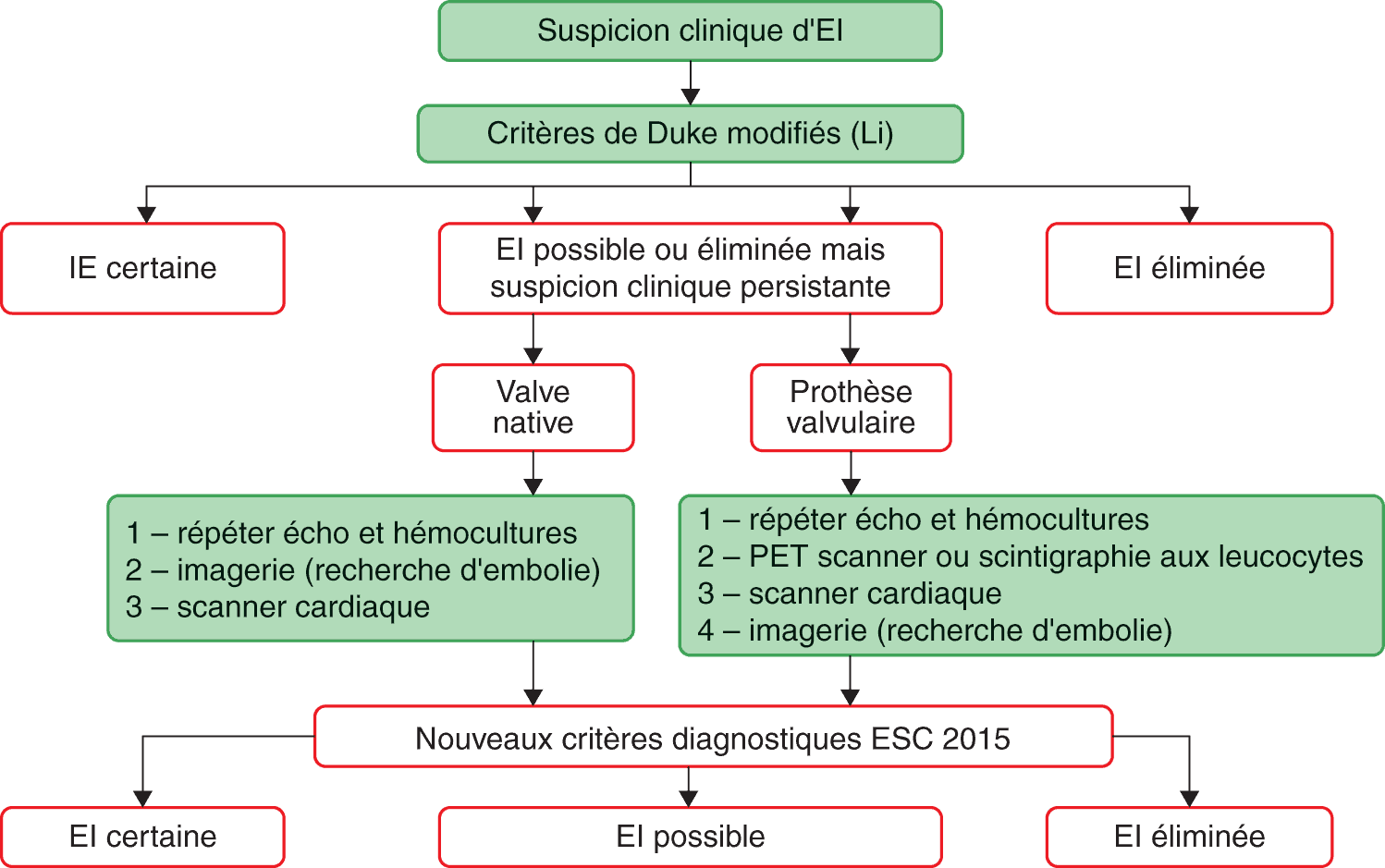
Source : Habib. 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Eur Heart J. 2015 21;36:3075-3128.
________________________________________________________________________________
Terrain à risque
Deux groupes de patients ont été définis, afin de repérer les patients les plus à risque d’endocardite :
- groupe A, à haut risque d’endocardite :
- patient porteur de prothèse valvulaire (biologique ou mécanique) ou de matériel intracardiaque ;
- patient présentant des antécédents d’endocardite infectieuse ;
- cardiopathies congénitales cyanogènes non opérées (ou opérée mais avec shunt persistant ou dans les six mois après l’opération) ;
- groupe B, à risque moins élevé :
- valvulopathie : insuffisance aortique, rétrécissement aortique, insuffisance mitrale, prolapsus valvulaire mitral, bicuspidie aortique ;
- cardiomyopathie hypertrophique obstructive ;
- cardiopathie congénitale non cyanogène (sauf communication interauriculaire).
Diagnostic de l’endocardite infectieuse
Diagnostic clinique
Le polymorphisme de la présentation de l’endocardite infectieuse est à l’origine de difficultés diagnostiques et donc d’un retard à la prise en charge.
Le diagnostic d’endocardite et le plus souvent suspecté devant la conjonction d’un syndrome infectieux sans origine évidente et de signes d’atteinte valvulaire, témoignant soit d’une cardiopathie à risque, soit de l’atteinte des valves par le processus infectieux.
Signes typiques
L’association d’un syndrome fébrile (quasi constant) à un souffle valvulaire nouvellement apparu (ou connu mais aggravé, ce qui est pour le moins subjectif) doit faire systématiquement rechercher une endocardite infectieuse.
Signes immunologiques
Splénomégalie, protéinurie à la bandelette urinaire signant une glomérulonéphrite, nodule de Roth au fond d’œil (nodules cotonneux de la rétine), faux panaris d’Osler (nodules de la pulpe des doigts, douloureux et fugaces).
Signes vasculaires
Placard érythémateux de Janeway (lésions papillaires érythémateuses non douloureuses siégeant sur l’éminence thénar ou hypothénar), purpura vasculaire pétéchial, hémorragie intracérébrale, hémorragie conjonctivale, embolie artérielle, embolie pulmonaire septique, anévrisme mycotique, hémorragie intracérébrale.
Diagnostic biologique et bactériologique
Les examens biologiques associent une hyperleucocytose et un syndrome inflammatoire non spécifiques.
La mise en évidence du micro-organisme responsable est un des éléments essentiels du diagnostic. Il est recommandé de prélever trois paires d’hémocultures aérobies et anaérobies espacées d’au moins une heure, ce qui permet l’identification du germe responsable dans plus de 95 % des cas (tableau 4.12). La bactériémie étant constante, il n’y a pas d’intérêt à prélever les hémocultures lors de pics fébriles.
Tableau 4.12. Micro-organismes avec leur prévalence approximative en fonction du type d’endocardite.
| Organisme | EVN (%) | ToxIV (%) | EPV précoce (%) | EPV tardive (%) |
| Streptocoque | 60 | 15–25 | 5 | 35 |
| Streptocoque Viridans | 30–40 | 5–10 | < 5 | 25 |
| Streptocoque bovis | 10 | < 5 | < 5 | < 5 |
| Enterocoque | 10 | 10 | < 5 | < 5 |
| Staphylocoque | 25 | 50 | 50 | 30 |
| Coagulase positive | 23 | 50 | 20 | 10 |
| Coagulase négative | < 5 | < 5 | 30 | 20 |
| Gram-negative (aérobies) | < 5 | 5 | 20 | 10 |
| Champignons | < 5 | < 5 | 10 | 5 |
| Culture négative | 5–10 | < 5 | < 5 | < 5 |
Le laboratoire de bactériologie doit être prévenu de la suspicion d’endocardite infectieuse, afin de conserver des prélèvements plus longtemps, éventuellement sur des milieux enrichis. Les techniques de spectrométrie de masse permettent une identification bactérienne plus précoce que les cultures conventionnelles :
- streptocoque alpha-hémolytique (S. viridans) ou non groupable : la porte d’entrée infectieuse est alors buccodentaire ;
- streptocoque D (S. gallolyticus) et entérocoques : la porte d’entrée est alors digestive (recherche d’un cancer colorectal indispensable) ;
- staphylocoque (S. aureus ou S. epidermidis) : la porte d’entrée est alors le plus souvent cutanée (terrain : toxicomanie intraveineuse).
On peut, cependant, observer dans plus 10 % des cas des endocardites à hémocultures négatives. Il faut alors évoquer :
- une endocardite infectieuse mais :
-
- dont l’infection est décapitée (antibiothérapie préalable),
- à germe de culture difficile (streptocoques déficients),
- à germe du groupe « HACEK » : Haemophilus, Actinobacillus, Cardiobacterium, Eikenella, Kingella,
- à germe inhabituel : Brucella, maladie de Lyme,
- à germe intracellulaire : Coxiella burnetti et Bartonella (B. quintana : y penser devant une pédiculose corporelle), Chlamydiae et Mycoplasma pneumoniae,
- fongique,
- EVN : endocardite infectieuse sur valve native,
- ToxIV : toxicomanie intraveineuse ;
- une endocardite non infectieuse :
-
- endocardite marastique : endocardite liée aux cancers (hémopathies, en particulier),
- endocardite de Liebman-Sachs : endocardite chez les patients lupiques.
Diagnostic morphologique
Échocardiographie (transthoracique et transœsophagienne)
Les végétations sont les lésions le plus souvent rencontrées dans l’endocardite. Il s’agit d’une masse valvulaire hyperéchogène, mobile et vibratile, appendue à la valve, le plus souvent sur son versant basse pression (atriale pour les valves atrioventriculaires et ventriculaires pour les valves sigmoïdes). La spécificité de l’échocardiographie transthoracique est élevée (> 90 %) pour le diagnostic de végétations mais sa sensibilité n’est que d’environ 70 %. L’échocardiographie transœsophagienne (ETO) à une sensibilité nettement plus élevée (> 90 %) tout en conservant une spécificité > 90 %. L’apport de l’imagerie 3D temps réel est appréciable, surtout en cas de prothèses valvulaires.
Les autres lésions valvulaires sont des abcès valvulaires ou annulaires (en particulier aortiques), déchirures ou des perforations dues à la destruction du tissu valvulaire par le processus infectieux. Elles sont le plus souvent diagnostiquées par leur conséquence qui est la régurgitation. Les perforations peuvent également être visualisées directement, en particulier par l’ETO. L’infection peut également être responsable de lésions non spécifiques comme une rupture de cordages de la valve mitrale.
Autres techniques d’imagerie cardiaque
Le scanner cardiaque et surtout utilisé en complément de l’ETO pour le diagnostic des lésions péri-valvulaires. L’acquisition doit être synchronisée sur l’électrocardiogramme. Les nouveaux scanners à haute définition et acquisition volumétrique pourraient se révéler utiles pour le diagnostic des végétations lorsque l’ETO est contre-indiquée.
La tomographie par émission de positons a surtout été étudiée dans les endocardites sur prothèse ou matériel de stimulation. Sa sensibilité semble assez faible pour le diagnostic d’endocardite sur valve native, mais est en cours de réévaluation. La scintigraphie aux leucocytes marqués est plus spécifique mais moins sensible que la tomographie par émission de positons.
L’imagerie extracardiaque (scanner ou IRM thoraco-abdominal cérébral…) est surtout utilisée afin de préciser les complications emboliques ou septiques de l’endocardite. Elle présente aussi un intérêt diagnostique lorsqu’elle détecte des lésions emboliques non suspectées sur la clinique, les pseudo-anévrismes, les perforations valvulaires, les fistules, les anévrysmes valvulaires, la désinsertion d’une prothèse valvulaire, surtout mécanique. (vidéo 4.9, vidéo 4.10).
L’imagerie extracardiaque (scanner ou IRM thoraco-abdominal cérébral…) est surtout utilisée afin de préciser les complications emboliques ou septiques de l’endocardite. Elle présente aussi un intérêt diagnostique lorsqu’elle détecte des lésions emboliques non suspectées sur la clinique, les pseudo-anévrismes, les perforations valvulaires, les fistules, les anévrysmes valvulaires, la désinsertion d’une prothèse valvulaire, surtout mécanique. (vidéo 4.9, vidéo 4.10).
Critères diagnostiques (critères de Duke modifiés)
Le diagnostic est posé grâce aux critères de Duke modifiés :
- on parle d’endocardite infectieuse s’il existe :
-
- deux critères majeurs,
- ou un critère majeur et trois critères mineurs,
- ou encore cinq critères mineurs ;
- l’endocardite infectieuse est possible en cas :
-
- d’association d’un critère majeur et d’un mineur,
- ou d’association de trois critères mineurs isolés.
________________________________________________________________________________
Critères diagnostiques de Duke modifié dans l’endocardite infectieuse
Critères majeurs
Hémocultures positives
- Présence dans deux hémocultures différentes de micro-organismes communément rencontrésdans l’EI : Streptococcus viridans, Streptococcus bovis, micro-organismes du groupe HACEK, Staphylococcus aureus ; ou entérocoques (en l’absence de foyer primaire).
- Ou hémocultures positives de façon persistante pour des micro-organismes susceptibles d’engendrer une EI : au moins 2 hémocultures prélevées à plus de 12 heures d’intervalle ; ou 3 sur 3, ou la majorité d’au moins 4 hémocultures prélevées à plus d’une heure d’intervalle entre la première et la dernière.
- Ou une seule hémoculture positive à Coxiella burnetii ou titre d’anticorps antiphase I IgG > 1/800.
Imagerie en faveur d’une EI
- Échocardiographie montrant des signes d’EI : végétation, abcès, pseudo-anévrisme, fistule intracardiaque, perforation ou anévrisme valvulaire ; ou désinsertion partielle, nouvellement apparue, d’une prothèse valvulaire ;
- Activité anormale autour du site d’implantation d’une prothèse valvulaire, détectée par un PET-scanner au 18FDG (uniquement si la prothèse a été implantée depuis plus de 3 mois) ou un SPECT-scanner aux leucocytes marqués.
- Lésion para-valvulaire certaine au scanner cardiaque.
La présence d’un souffle n’est plus un critère majeur
Critères mineurs
Prédisposition
Atteinte cardiaque prédisposante ou toxicomanie par voie intraveineuse.
Fièvre
Température ≥ 38 °C.
Phénomènes vasculaires (y compris ceux détectés uniquement par un examen d’imagerie)
- Embolie artérielle majeure, infarctus pulmonaire septique, anévrisme mycotique, hémorragie.
- Intracrânienne, hémorragies conjonctivales, lésions de Janeway.
Phénomènes immunologiques
Glomérulonéphrite, nodosités d’Osler, taches de Roth, facteur rhumatoïde.
Évidence microbiologique
Hémoculture(s) positive(s) ne réunissant pas les critères majeurs ci-dessus, ou évidence sérologique d’une infection en évolution due à un micro-organisme pouvant causer une EI.
________________________________________________________________________________
Complications
Les complications de l’endocardite infectieuse sont hémodynamiques, infectieuses et emboliques et sont responsables de la plupart des décès en phase hospitalière.
Complications hémodynamiques
L’insuffisance cardiaque est la complication la plus grave de l’endocardite, multipliant entre 2 et 3 fois la mortalité hospitalière. Des signes d’insuffisance cardiaque congestive sont observés dans environ un tiers des endocardites infectieuses. Les complications hémodynamiques sont la conséquence de régurgitations aiguës dues aux mutilations valvulaires.
Complications infectieuses
La persistance de l’infection systémique est définie par la positivité des hémocultures après une semaine de traitement antibiotique.
Les complications infectieuses sont favorisées par la virulence du micro-organisme et par l’extension de l’infection. L’extension péri-valvulaire est la complication infectieuse la plus fréquente mais elle est plus rare dans les endocardites sur valve native que sur prothèse. Elle est favorisée par la virulence du microorganisme (staphylocoques notamment). Elle concerne plus souvent la valve aortique que la valve mitrale et se traduit surtout par un abcès, plus rarement une fistule ou un faux anévrisme. Leur diagnostic repose surtout sur l’ETO.
Complications emboliques
Les complications emboliques sont la conséquence de la migration des végétations. Les embolies cliniques compliquent 20 à 40 % des endocardites. Les embolies peuvent être cliniquement silencieuses et sont donc plus fréquentes lorsqu’elles sont dépistées par une imagerie systématique. L’IRM diagnostique des embolies chez 40 à 50 % des patients pour les localisations cérébrales et 30–40 % pour les localisations abdominales, surtout spléniques et rénales.
Autres complications
Toute suspicion de complication neurologique doit conduire à une imagerie cérébrale (IRM > scanner injecté) urgente. L’icmagerie extracardiaque est le plus souvent systématique à la recherche de lésions emboliques. Outre les AVC emboliques, l’endocardite peut entraîner des hémorragies cérébrales, parenchymateuses ou méningées dans 5 à 15 % des cas et des abcès dans moins de 10 %, ces complications pouvant être asymptomatiques. Les complications hémorragiques sont dues à une rupture d’anévrisme mycotique ou au ramollissement hémorragique d’un AVC initialement ischémique. Les complications neurologiques sont associées une augmentation de la mortalité de l’endocardite,
Les arthrites et spondylodiscites sont observées dans 10 à 15 % des endocardites. Le diagnostic repose sur l’imagerie et parfois le diagnostic microbiologique par ponction. Une antibiothérapie prolongée est nécessaire en cas de spondylodiscite.
L’insuffisance rénale est fréquente et souvent multifactorielle. Les causes iatrogènes sont fréquentes et impliquent la toxicité des antibiotiques et l’injection d’agents de contraste iodés. L’insuffisance rénale est rarement secondaire à une glomérulopathie spécifique.
Les troubles conductifs (BAV de tout degré) sont surtout observés en cas d’endocardite aortique, en particulier compliquée de lésions péri-valvulaires, ce qui justifie une surveillance régulière de l’électrocardiogramme.
Traitement de l’endocardite infectieuse
Le traitement repose principalement sur l’antibiothérapie. Il faut différencier le traitement curatif (traitement de l’endocardite infectieuse) du traitement prophylactique (ce dernier évite l’apparition d’endocardite infectieuse chez des patients à risque).
Traitement curatif
Il consiste en une bi-antibiothérapie bactéricide active sur le germe mis en évidence sur les hémocultures (tableau 4.13). Ce traitement doit être administré par voie intraveineuse, prolongé (en moyenne quatre à six semaines de traitement minimum) et adapté au type de valve touchée (native ou prothétique).
Tableau 4.13. Bi-antibiothérapie des endocardites infectieuses (recommandations européennes, 2015).
| Bactérie | Sur valve native | Sur valve prothétique |
| Streptocoque | Amoxicilline ou ceftriaxone ou pénicilline G (4 semaines)
Si allergie : vancomycine (4 semaines) Ajout de gentamycine en cas de streptocoque modérément résistant à la pénicilline |
Idem que valve native |
| Staphylocoque méticilline-sensible | Oxacilline (4 à 6 semaines) | Oxacilline (≥ 6 semaines)
+ rifampicine (≥ 6 semaines) + gentamycine (2 semaines) |
| Staphylocoque méticilline-résistant (ou Staphylocoque méticilline-sensible avec allergie à la pénicilline) | Vancomycine (4 à 6 semaines) | Vancomycine (≥ 6 semaines)
+ rifampicine (≥ 6 semaines) + gentamycine (2 semaines) |
| Traitement probabiliste avant résultat des hémocultures
EI sur valve native, ou sur valve prothétiques plus de 12 mois après la pose |
Amoxicilline
+ oxacilline + gentamycine |
Vancomycine
+ gentamycine |
| Traitement probabiliste avant résultat des hémocultures.
EI associée aux soins ou sur valve prothétique dans les 12 mois suivants la pose |
Vancomycine
+ rifampicine + gentamycine |
Vancomycine
+ rifampicine + gentamycine |
Le traitement chirurgical (éradication des tissus infectés et remplacement valvulaire) fait partie intégrante du traitement curatif en association avec l’antibiothérapie. Il n’est pas systématique, et est discuté au cas par cas.
Le remplacement valvulaire est la technique la plus utilisée et elle a pour but de restaurer la fonction valvulaire mais aussi d’exciser tous les tissus infectés. En position mitrale, la faisabilité d’une plastie dépend de l’extension des lésions et de l’expertise chirurgicale. Le principe général est d’exciser tous les tissus infectés, ce qui peut conduire à des gestes complexes en cas de lésions péri-valvulaires étendue. Le risque ultérieur d’endocardite ne diffère pas entre prothèse mécanique et bioprothèse. Les bioprothèses sont toutefois favorisées en cas de complications neurologiques ou de complications pouvant nécessiter des interventions ultérieures.
Les indications de la chirurgie valvulaire dans l’endocardite infectieuse aiguë visent à prévenir ou traiter les principales complications, hémodynamiques, infectieuses et emboliques. Les indications les plus formelles et les plus urgentes sont d’ordre hémodynamique
La durée de l’antibiothérapie est comptée à partir du premier jour du traitement efficace (antibiotiques et doses). En cas de chirurgie, la durée de l’antibiothérapie est comptée à partir de la date de la chirurgie lorsque la culture de valve est positive.
Traitement prophylactique
Les patients du groupe A (uniquement) relèvent d’une antibiothérapie prophylactique en cas de geste dentaire impliquant une effraction gingivale, péri-apicale ou de la muqueuse orale, par amoxicilline 2 g, 30 à 60 minutes avant le geste (ou clindamycine 600 mg en cas d’allergie à la pénicilline)
Les raisons de la limitation des indications d’antibioprophylaxie sont le manque de données scientifiques concernant la réelle efficacité préventive de cette antibioprophylaxie et le risque de développer des résistances bactériennes dans le cas de traitement abusif.
Compléments en ligne
Des compléments numériques sont associés à cet ouvrage. Ils proposent des vidéos. Pour voir ces compléments, connectez-vous sur http://www.em-consulte.com/e-complement/ 475848 et suivez les instructions.
Vidéo 4.1 Échocardiographie bidimensionnelle, incidence parasternale gauche « grand axe ». Zoom sur la valve aortique montrant un épaississement et un défaut de coaptation diastolique, chez un patient présentant une insuffisance aortique.
Vidéo 4.2 Échographie bidimensionnelle, incidence parasternale gauche « grand axe », Doppler bidimensionnel à codage couleur.Visualisation d’un jet de régurgitation aortique de l’aorte vers le ventricule gauche, dans une insuffisance aortique massive (même patient que dans la vidéo 4.1).
Vidéo 4.3 Échographie bidimensionnelle, incidence parasternale gauche « petit axe », Doppler bidimensionnel à codage couleur.
Visualisation du jet de régurgitation aortique, moulant les sigmoïdes aortiques, avec un défaut de coaptation diastolique.
Vidéo 4.4 Échocardiographie bidimensionnelle, incidence parasternale gauche « petit axe ».Sténose aortique, avec épaississement et calcification des sigmoïdes, et réduction de l’ouverture systolique. La planimétrie de l’orifice en systole permet de déterminer la surface aortique anatomique.
Vidéo 4.5 Échographie bidimensionnelle, incidence parasternale gauche « grand axe », chez un patient ayant une insuffisance mitrale.Noter le défaut de coaptation systolique, en rapport avec un prolapsus de la valve mitrale postérieure. Noter également l’épaississement dystrophique des feuillets valvulaires.
Vidéo 4.6 Échographie bidimensionnelle, incidence parasternale gauche « grand axe », Doppler bidimensionnel à codage couleur.Chez le même patient que dans la vidéo 3.5, visualisation du jet de régurgitation mitrale excentré, dirigé vers la face atriale de la valve antérieure, chez un patient ayant un prolapsus de la valve mitrale postérieure (prédominant sur le segment P2).
Vidéo 4.7 Échographie bidimensionnelle, incidence parasternale gauche « grand axe », avec zoom sur la face mitrale.Sténose mitrale, en rapport avec une fusion commissurale, un épaississement des feuillets valvulaires mitraux, avec calcifications nodulaires, et limitation de l’ouverture diastolique. Les feuillets valvulaires restent relativement souples et l’appareil sous-valvulaire modérément remanié. Ce patient est porteur d’une sténose mitrale.
Vidéo 4.8 Échographie bidimensionnelle, incidence parasternale gauche « petit axe » chez le même patient que dans la vidéo 4.7.Cette incidence permet de préciser le degré d’atteinte commissurale (antérolatérale à droite, postéromédiale à gauche) et de déterminer la surface mitrale anatomique, en réalisant la planimétrie de l’orifice mitrale en protodiastole. Chez ce patient, la sténose mitrale est définie par une surface mitrale à 1,2 cm2, définissant une sténose
Vidéo 4.9 Échographie transoesophagienne, incidence à 120°, chez un patient ayant une endocardite infectieuse.À noter la présence d’une végétation sur la sigmoïde antérieure droite, prolabant dans la chambre de chasse ventriculaire gauche. À noter le défaut de coaptation, à l’origine d’une insuffisance aortique chez ce patient.
Vidéo 4.10Échographie transoesophagienne, incidence à 120°, obtenue chez le même patient que dans la vidéo 4.9.Le Doppler bidimensionnel à codage couleur permet de visualiser la régurgitation aortique, jet de l’aorte vers le ventricule gauche, en rapport avec le défaut de coaptation, et la présence de la végétation sur la sigmoïde antérieure droite.
Vidéo 4.11Échographie bidimensionnelle, incidence parasternale gauche « grand axe ».Visualisation d’une masse valvulaire appendue à la sigmoïde postérieure, faisant discuter une végétation. Dans le contexte, il s’agissait d’un fibroélastome, tumeur valvulaire bénigne, caractérisée par ailleurs en échographie transoesophagienne (vidéo 4.12).
Vidéo 4.12Échographie transoesophagienne, incidence à 120°, chez le même patient que la dans la vidéo 4.11.Visualisation du fibroélastome, appendu à la sigmoïde postérieure, sans dysfonction valvulaire. Cette tumeur valvulaire fait discuter comme diagnostic différentiel une végétation infectieuse.
Vidéo 4.13Échographie bidimensionnelle, incidence apicale « quatre cavités » (centrée sur la valve tricuspide) avec Doppler bidimensionnel à codage couleur.Le Doppler permet de visualiser une régurgitation tricuspide, jet depuis le ventricule droit vers l’atrium droit. L’insuffisance tricuspide donne également accès, avec le Doppler continu, à la détermination de la PAP systolique (non montrée dans cet exemple).
________________________________________________________________________________
Points importants
- Le cœur est composé de quatre valves : mitrale séparant l’atrium gauche du ventricule gauche, tricuspide séparant l’atrium droit du ventricule droit, aortique séparant le ventricule gauche de l’aorte thoracique ascendante et pulmonaire séparant le ventricule droit du tronc de l’artère pulmonaire.
- La valve aortique est tricuspide, composée de trois feuillets ou cuspides semi-lunaires.
- L’aorte thoracique est segmentée en trois parties, aorte ascendante, horizontale (crosse aortique) et descendante.
- Les trois segments de l’aorte thoracique sont couverts par le péricarde sauf à partir de l’aorte thoracique horizontale.
- La valve mitrale est bicuspide, les deux feuillets sont de taille inégale, valve antérieure ou grande valve mitrale et valve postérieure ou petite valve mitrale.
- Chacun des deux feuillets de la valve mitrale est segmenté en trois sous parties, délimitant les segments paracommissuraux antérieur, médial et paracommissuraux postérieurs.
- Ces deux feuillets de la valve mitrale se rejoignent par une commissure antérieure ou antérolatérale à la jonction de A1 et P1 et par une commissure postérieure ou postéromédiale à la jonction de A3 et P3.
- L’appareil valvulaire mitral comprend par ailleurs un squelette fibreux et le système sous valvulaire comprend des piliers et cordages, amarrant le feuillet de la valve mitrale aux piliers postéromédial et antérolatéral, en regard respectivement de la commissure postérieure et antérieure.
- La valve tricuspide est composée de trois feuillets, antérieur, postérieur et septal.
- La valve pulmonaire est composée de trois feuillets sigmoïdes, deux postérieurs et un feuillet antérieur.
- Au centre du cœur se trouve le squelette fibreux, composé de fibres de collagène et comprenant les éléments anatomiques suivants : anneaux fibreux sur lesquels s’insèrent les feuillets valvulaires, cordages tendineux, trigones fibreux et muscles papillaires postéromédial et antérolatéral.
- Le premier bruit du cœur ou B1 marque le début de la systole et représente les bruits liés à la contraction myocardique associée à la fermeture des valves atrioventriculaires. Il est maximal à l’apex du cœur.
- Le deuxième bruit du cœur ou B2 marque le début de la diastole et correspond à la fermeture des valves pulmonaire et aortique.
- Le troisième bruit du cœur ou B3, diastolique, survient après le deuxième bruit et est inconstant, toujours pathologique sauf chez l’enfant et le jeune adulte.
- En cas de dysfonction ventriculaire gauche, la perception d’un B3 est un bruit de galop ventriculaire ou galop protodiastolique.
- Le quatrième bruit du cœur ou B4 correspond à la contraction atriale et traduit la perte de la distensibilité ventriculaire.
- L’échographie cardiaque est la méthode anatomique de référence non invasive pour caractériser la géométrie, la fonction et l’hémodynamique cardiaque.
- Il existe plusieurs modalités d’échographie en fonction de la fenêtre utilisée, transthoracique, transœsophagienne, épicardique, intracardiovasculaire
- Il existe plusieurs modalités de Doppler cardiaque, Doppler pulsé, continu, couleur, tissulaire.
- Une échocardiographie Doppler peut être effectuée au repos, à l’effort ou après injection d’une molécule reproduisant les conditions d’un stress (échographie de stress).
- L’échographie de contraste rehausse le signal cavitaire et documente la présence d’un shunt intracardiaque.
- Le Doppler cardiaque donne accès à la caractérisation de l’hémodynamique non invasive, débit, fonction et pressions intracardiaques.
- L’hémodynamique invasive caractérise les pressions intracardiaques, le débit cardiaque et l’injection d’iode permettent de caractériser la fonction ventriculaire et la présence éventuelle d’une régurgitation valvulaire.
- La sténose aortique est à l’origine d’une surcharge de pression ventriculaire gauche aboutissant à un remodelage cardiaque, à un certain degré de dysfonction diastolique à une discordance entre les apports et les besoins en oxygène du myocarde.
- La maladie de Monckeberg est la première cause de sténose aortique après 70 ans (sténose aortique dégénérative).
- La bicuspidie aortique est l’anomalie congénitale la plus fréquente, associée dans un cas sur deux à une dilatation de l’aorte thoracique, à rechercher systématiquement.
- La bicuspidie aortique est la pathologie congénitale cardiaque le plus commune, affectant 0,5 à 2 % de la population, trois fois plus fréquente chez les hommes.
- Le rhumatisme articulaire aigu se caractérise par un épaississement valvulaire et une fusion des commissures.
- La sténose valvulaire orificielle aortique doit être distinguée d’une sténose aortique supra valvulaire liée à la présence d’une membrane fibromusculaire circonférentielle et d’une sténose aortique supra valvulaire (congénitale), beaucoup plus rare.
- Les signes fonctionnels évocateurs d’une sténose aortique hémodynamiquement significative sont la dyspnée, l’angor et la syncope, survenant à l’effort.
- Le souffle de sténose aortique se caractérise par son temps mésosystolique, son siège au foyer aortique, ses irradiations carotidiennes et la disparition du B2, en cas de calcification valvulaire.
- L’échocardiographie Doppler caractérise la sténose aortique, sévère lorsque la vélocité maximale transvalvulaire est > 4 m/s, le gradient moyen VG-aorte > 40 mmHg, et la surface aortique < 1 cm2 ou < 0,6 cm2/m2 de surface indexée à la surface corporelle.
- Le risque de mort subite chez un patient asymptomatique porteur d’une sténose aortique critique est inférieur à 2 % par an.
- En cas de sténose aortique symptomatique, la survie est déterminée par la présence de signes fonctionnels : survie à cinq ans de 50 % dans le cas d’apparition d’un angor et survie de 50 % à trois ans en cas d’apparition d’une syncope.
- En l’absence de remplacement valvulaire aortique, la survenue d’une insuffisance cardiaque est associée à une survie inférieure à deux ans.
- Le remplacement valvulaire aortique chirurgical, est fonction du contexte et du risque opératoire, est le traitement de référence de la sténose aortique.
- Le remplacement valvulaire aortique percutané (TAVI ou TAVR) est proposé en cas de sténose aortique calcifiée serrée symptomatique chez les patients à risque opératoire élevé ou intermédiaire ; les indications pourraient être élargies dans un proche avenir.
- L’insuffisance mitrale chronique se caractérise par une dilatation ventriculaire gauche avec hypertrophie ventriculaire gauche excentrique.
- Le souffle d’insuffisance mitrale est holosystolique, perçu à l’apex, parfois associé à un galop protodiastolique ou B3.
- L’échographie cardiaque est la méthode de référence de quantification d’une régurgitation mitrale en déterminant la surface de l’orifice régurgitant, le volume et régurgitant et la fraction de régurgitation, et en appréciant le retentissement atrial et ventriculaire gauche, sur les cavités droites, ainsi que l’hémodynamique intracardiaque.
- Le prolapsus valvulaire mitral correspond à l’éversion de tout ou partie d’un feuillet mitral dans l’oreillette gauche en arrière du plan de l’anneau mitral en systole, le point de coaptation valvulaire étant situé en deçà du plan annulaire mitral.
- Deux présentations cliniques correspondent au PVM : le syndrome de Barlow, intéressant les sujets jeunes et la dégénérescence ou déficience fibro-élastique, intéressant les sujets plus âgés.
- Le traitement conservateur de la valve mitrale (avec anneau mais sans prothèse valvulaire) est proposé chaque fois que possible devant une insuffisance mitrale, après en avoir précisé le mécanisme.
- L’insuffisance aortique, surcharge diastolique, aboutit à une dilatation du ventricule gauche, à une hypertrophie compensatrice excentrique avec un retentissement variable sur l’hémodynamique intracardiaque.
- La maladie de Marfan est liée à une mutation du gène FBN1, situé sur le chromosome 15, et codant pour une protéine, synthétisée par les fibroblastes, la fibrilline de type 1.
- Le souffle d’insuffisance aortique est maximum au foyer aortique protodiastolique, irradiant vers le bord gauche du sternum, associé à un élargissement de la pression artérielle différentielle et parfois à un galop B3.
- L’échographie cardiaque caractérise le mécanisme de l’insuffisance aortique et la quantifie : diamètre du jet à l’origine, surface de l’orifice régurgitant, volume régurgité, et fraction de régurgitation ainsi que le retentissement sur la géométrie et la fonction ventriculaire gauche ainsi que sur l’hémodynamique intracardiaque.
- L’insuffisance aortique, comme l’insuffisance mitrale, peut correspondre à un mécanisme aigu, en particulier lors d’une endocardite infectieuse et d’un traumatisme thoracique.
- L’insuffisance tricuspide, le plus souvent secondaire ou fonctionnelle, est alors associée à une atteinte cardiaque gauche.
- L’insuffisance tricuspide fonctionnelle est secondaire à une hypertension pulmonaire.
- L’insuffisance tricuspide organique a plusieurs causes, dominées par le rhumatisme articulaire aigu, l’endocardite infectieuse (IT primaire ou organique), beaucoup plus rare que les IT secondaires, secondaires à une surcharge volumétrique ou barométrique du ventricule droit, à une fibrillation atriale ou un asynchronisme cardiaque.
- L’échographie cardiaque caractérise le mécanisme de la régurgitation tricuspide, sa cause ainsi que son volume par le Doppler et son retentissement (dimensions des cavités droites et de la veine cave inférieure).
- Certains médicaments peuvent être associés à une valvulopathie : dérivés de l’alcaloïde, ergotamine et méthysergide, fenfluramine et dexfenfluramine (anorexigènes retirés du commerce), agonistes dopaminergiques, dérivés de l’ergot, pergolide, cabergoline, MDMA.
- La sténose mitrale réalise un défaut d’ouverture valvulaire mitrale en diastole, elle est le plus souvent liée à un rhumatisme articulaire aigu, caractérisé par une fusion commissurale.
- Le retentissement d’une sténose mitrale est auriculaire gauche avec une élévation de la POG et d’une hypertension pulmonaire, ainsi qu’à son retentissement secondaire sur les dimensions et la fonction du ventricule droit.
- L’échocardiographie Doppler caractérise la sténose mitrale, la quantifie ainsi que son retentissement atrial gauche et hémodynamique (pressions artérielles pulmonaires).
- Le risque d’une sténose mitrale est surtout lié à la thrombose intra-atriale gauche, à l’origine d’embolies artérielles.
- Le traitement de référence de la sténose mitrale est la valvuloplastie mitrale percutanée, qui donne d’excellents résultats fonctionnels à moyen et à long terme (en l’absence de régurgitation mitrale significative et lorsque l’anatomie valvulaire s’y prête).
- L’endocardite infectieuse est une infection d’une ou plusieurs valves cardiaques, par un micro-organisme, bactérie le plus souvent, et touche le plus souvent les valves du cœur gauche, avec une incidence annuelle de 1 500 cas.
- Les atteintes valvulaires à haut risque de complication de l’endocardite infectieuse sont : les prothèses valvulaires biologiques ou mécaniques, les matériels intracardiaques, sonde de stimulation, les patients ayant des antécédents d’endocardite infectieuse et les patients porteurs de cardiopathies congénitales cyanogènes non opérés ou opérés mais avec un shunt persistant, ou dans les 6 mois au décours d’une intervention chirurgicale.
- Le diagnostic d’endocardite infectieuse est le plus souvent évoqué devant la conjonction d’un syndrome infectieux avec des signes d’atteinte valvulaire, régurgitation le plus souvent.
- Dans les endocardites infectieuses sur valve native, le streptocoque est le germe prépondérant ; en revanche dans les endocardites sur prothèse valvulaire, le staphylocoque est prépondérant.
- L’échocardiographie est un examen essentiel dans la recherche de végétations infectieuses et des complications d’une endocardite infectieuse, abcès valvulaire, abcès annulaire ou fistule intracardiaque.
- Les critères diagnostiques de l’endocardite infectieuse comprennent des critères majeurs (hémocultures positives, imagerie en faveur de l’endocardite infectieuse) et des critères mineurs (prédisposition, température ≥ 38°, phénomènes vasculaires, phénomènes immunologiques, preuve microbiologique).
- Les complications de l’endocardite infectieuse comprennent la dysfonction valvulaire, le risque d’insuffisance cardiaque, les complications infectieuses, rénales, emboliques et le développement d’anévrysmes artériels cérébraux.
- Le traitement d’une endocardite infectieuse repose sur une bi-antibiothérapie bactéricide active sur le germe mis en évidence dans les hémocultures.
- Le traitement est administré par voie intraveineuse prolongée, en moyenne 4 à 6 semaines, adapté au germe et type de valves, native ou prothétique.
- Le traitement chirurgical dépend de la clinique (contrôle du processus infectieux, insuffisance cardiaque, lésions valvulaires – taille de la végétation, abcès, fistule) et de son retentissement et est discuté cas par cas lors d’une confrontation médico-chirurgicale.
________________________________________________________________________________
Exercices en ligne
Les exercices relatifs à ce chapitre sont disponibles en ligne à l’adresse suivante : http://www.em-consulte.com/ e-complement/475848
Des vidéos sont également disponibles pour illustrer ce chapitre. Pour y accéder, connectez-vous sur http://www.em-consulte.com/e-complement/475848 et suivez les instructions.
________________________________________________________________________________
Vidéo 4.1
Échocardiographie bidimensionnelle, incidence parasternale gauche « grand axe ».Zoom sur la valve aortique montrant un épaississement et un défaut de coaptation diastolique, chez un patient présentant une insuffisance aortique.
________________________________________________________________________________
Vidéo 4.2
Échographie bidimensionnelle, incidence parasternale gauche « grand axe », Doppler bidimensionnel à codage couleur.Visualisation d’un jet de régurgitation aortique de l’aorte vers le ventricule gauche, dans une insuffisance aortique massive (même patient que dans la vidéo 4.1).
________________________________________________________________________________
Vidéo 4.3
Échographie bidimensionnelle, incidence parasternale gauche « petit axe », Doppler bidimensionnel à codage couleur.Visualisation du jet de régurgitation aortique, moulant les sigmoïdes aortiques, avec un défaut de coaptation diastolique.
________________________________________________________________________________
Vidéo 4.4
Échocardiographie bidimensionnelle, incidence parasternale gauche « petit axe ».Sténose aortique, avec épaississement et calcification des sigmoïdes, et réduction de l’ouverture systolique. La planimétrie de l’orifice en systole permet de déterminer la surface aortique anatomique.
________________________________________________________________________________
Vidéo 4.5
Échographie bidimensionnelle, incidence parasternale gauche « grand axe », chez un patient ayant une insuffisance mitrale.Noter le défaut de coaptation systolique, en rapport avec un prolapsus de la valve mitrale postérieure. Noter également l’épaississement dystrophique des feuillets valvulaires.
________________________________________________________________________________
Vidéo 4.6
Échographie bidimensionnelle, incidence parasternale gauche « grand axe », Doppler bidimensionnel à codage couleur.Chez le même patient que dans la vidéo 4.5, visualisation du jet de régurgitation mitrale excentré, dirigé vers la face atriale de la valve antérieure, chez un patient ayant un prolapsus de la valve mitrale postérieure (prédominant sur le segment P2).
________________________________________________________________________________
Vidéo 4.7
Échographie bidimensionnelle, incidence parasternale gauche « grand axe », avec zoom sur la face mitrale.Sténose mitrale, en rapport avec une fusion commissurale, un épaississement des feuillets valvulaires mitraux, avec calcifications nodulaires, et limitation de l’ouverture diastolique.Les feuillets valvulaires restent relativement souples et l’appareil sous-valvulaire modérément remanié. Ce patient est porteur d’une sténose mitrale.
________________________________________________________________________________
Vidéo 4.8
Échographie bidimensionnelle, incidence parasternale gauche « petit axe » chez le même patient que dans la vidéo 4.7.Cette incidence permet de préciser le degré d’atteinte commissurale (antérolatérale à droite, postéromédiale à gauche) et de déterminer la surface mitrale anatomique, en réalisant la planimétrie de l’orifice mitrale en protodiastole. Chez ce patient, la sténose mitrale est définie par une surface mitrale à 1,2 cm2, définissant une sténose.
________________________________________________________________________________
Vidéo 4.9
Échographie transoesophagienne, incidence à 120°, chez un patient ayant une endocardite infectieuse.À noter la présence d’une végétation sur la sigmoïde antérieure droite, prolabant dans la chambre de chasse ventriculaire gauche. À noter le défaut de coaptation, à l’origine d’une insuffisance aortique chez ce patient.
________________________________________________________________________________
Vidéo 4.10
Échographie transoesophagienne, incidence à 120°, obtenue chez le même patient que dans la vidéo 4.9.Le Doppler bidimensionnel à codage couleur permet de visualiser la régurgitation aortique, jet de l’aorte vers le ventricule gauche, en rapport avec le défaut de coaptation, et la présence de la végétation sur la sigmoïde antérieure droite.
________________________________________________________________________________
Vidéo 4.11
Échographie bidimensionnelle, incidence parasternale gauche « grand axe ». Visualisation d’une masse valvulaire appendue à la sigmoïde postérieure, faisant discuter une végétation.Dans le contexte, il s’agissait d’un fibroélastome, tumeur valvulaire bénigne, caractérisée par ailleurs en échographie transoesophagienne (vidéo 4.12).
________________________________________________________________________________
Vidéo 4.12
Échographie transoesophagienne, incidence à 120°, chez le même patient que la dans la vidéo 4.11.Visualisation du fibroélastome, appendu à la sigmoïde postérieure, sans dysfonction valvulaire. Cette tumeur valvulaire fait discuter comme diagnostic différentiel une végétation infectieuse.
________________________________________________________________________________
Vidéo 4.13
Échographie bidimensionnelle, incidence apicale « quatre cavités » (centrée sur la valve tricuspide) avec Doppler bidimensionnel à codage couleur.Le Doppler permet de visualiser une régurgitation tricuspide, jet depuis le ventricule droit vers l’atrium droit. L’insuffisance tricuspide donne également accès, avec le Doppler continu, à la détermination de la PAP systolique (non montrée dans cet exemple).
Partagez cette publication
Written by : SFC
Plus de publications de la SFC

CARDIOLOGIE PÉDIATRIQUE Tetralogy of Fallot: electrophysiology-guided surgical ablation during pulmonary valve replacement | Lire [...]

CARDIOLOGIE PÉDIATRIQUE 📌 À LA UNE : Tetralogy of Fallot: electrophysiology-guided surgical ablation during [...]


