Suivez-nous sur les réseaux sociaux !
Sommaire du chapitre :
Dernières publications
Publications
Chapitre 5 – Insuffisance cardiaque
Auteurs : J.-N. Trochu, J.-J. Mercadier, C. Toquet, G. Lamirault, T. Le Tourneau
Définitions, épidémiologie
La Société européenne de cardiologie définit l’insuffisance cardiaque comme une anomalie de la structure ou de la fonction cardiaque, responsable de l’impossibilité pour le cœur de délivrer l’oxygène de façon adaptée aux besoins métaboliques des tissus à un niveau de pressions de remplissage normal (ou alors seulement au prix d’une augmentation des pressions de remplissage, voir chapitre 1, Physiologie, Coeur). En d’autres termes, cela revient à l’incapacité du cœur à générer un débit cardiaque suffisant, au repos ou à l’effort, pour assurer le transport de la quantité d’oxygène nécessaire au fonctionnement normal de l’organisme.
L’insuffisance cardiaque est un syndrome clinique au cours duquel les patients ont des symptômes (dyspnée, fatigue, etc.) qui peuvent être accompagnés de signes cliniques typiques (râles crépitants, déplacement du choc de pointe, turgescence jugulaire, œdème des chevilles, etc.) résultant d’une anomalie de la fonction ou de la structure du cœur, elles-mêmes responsables d’une baisse du débit cardiaque ou d’une augmentation des pressions intracardiaques au repos ou à l’effort.
L’insuffisance cardiaque est fréquente, sa prévalence atteignant 1 à 2 % de la population adulte dans les pays développés et dépassant 10 % chez les sujets de plus de 70 ans. Chez les sujets de plus de 65 ans consultant pour une dyspnée d’effort en médecine générale, 1 sujet sur 6 a une insuffisance cardiaque méconnue, principalement à fraction d’éjection du ventricule gauche (FEVG) préservée (voir plus loin). La prévalence de l’insuffisance cardiaque est en constante augmentation. Elle touche principalement les sujets âgés, est très invalidante et retentit de façon importante sur la qualité de vie des patients. La mortalité par insuffisance cardiaque est élevée, plus élevée que celle liée à certains cancers dans les mêmes tranches d’âge, et elle conduit à de nombreuses hospitalisations qui induisent des dépenses de santé très importantes. Au cours des trente dernières années, de nombreux progrès ont été réalisés dans le traitement médical, chirurgical, la prise en charge globale et le parcours de soins du patient insuffisant cardiaque. Un certain nombre d’études montrent que l’incidence des hospitalisations pour insuffisance cardiaque diminuerait, plus pour les insuffisances cardiaques à FEVG altérée que pour celles à FEVG préservée. Mais ces progrès s’avèrent encore insuffisants. Les données du registre européen publiées en 2013, montrent que la mortalité toutes causes à un an chez les patients hospitalisés était de 17 % et de 7 % respectivement chez les patients stables ou ambulatoires. Les causes de décès sont principalement cardiovasculaires (mort subite, aggravation de l’insuffisance cardiaque). Les hospitalisations sont principalement en lien avec des causes non cardiovasculaires particulièrement chez les patients avec une FEVG préservée alors que les hospitalisations pour cause cardiovasculaires n’ont pas augmenté entre 2000 et 2010.
Les deux causes principales de l’insuffisance cardiaque sont la maladie coronaire athéromateuse (voir chapitre 3) et l’hypertension artérielle systémique (voir chapitre 2–1). L’amélioration de la prise en charge de l’hypertension artérielle et des syndromes coronaires aigus, la diminution de la fréquence des valvulopathies rhumatismales et l’augmentation de la longévité, liés aux progrès médicaux en général, ont profondément modifié le profil des patients insuffisants cardiaques au cours des quarante dernières années.
Actuellement, on observe principalement deux présentations qui se distinguent par la valeur de la FEVG : l’insuffisance cardiaque à FEVG altérée (ou insuffisance cardiaque systolique) et l’insuffisance cardiaque à FEVG préservée.
________________________________________________________________________________
Le paramètre le plus simple pour évaluer la fonction cardiaque est la fraction d’éjection du ventricule gauche (FEVG), qui correspond au pourcentage du volume sanguin télédiastolique éjecté lors de chaque systole :
FEVG = (Volume télédiastolique-Volume télésystolique) / Volume télédiastolique
Elle témoigne de l’efficacité de la contraction cardiaque
________________________________________________________________________________
La FEVG varie en fonction de la méthode utilisée pour sa mesure, mais elle est normalement ≥ 50 % :
- dans l’insuffisance cardiaque systolique, ou insuffisance cardiaque à FEVG altérée, la contraction cardiaque est abaissée et un remodelage du ventricule gauche intervient sous la forme d’une dilatation (secondaires à différents mécanismes d’adaptation décrits dans la section Physiopathologie). Ces mécanismes permettent, dans un premier temps, de maintenir le volume d’éjection systolique (VES) : le ventricule éjecte une fraction plus basse d’un plus grand volume télédiastolique. Chez ces patients, les progrès techniques et pharmacologiques réalisés au cours des trente dernières années ont permis de réduire de façon importante la mortalité cardiovasculaire et totale, et d’améliorer la qualité de vie ;
- au cours des années quatre-vingt, la diffusion des échocardiographes a transformé la prise en charge clinique et a permis d’identifier progressivement l’insuffisance cardiaque à FEVG préservée, particulièrement fréquente chez les sujets âgés. La réalisation d’échocardiographies au moment d’un épisode aigu d’insuffisance cardiaque (par exemple lors d’un œdème aigu pulmonaire) a permis d’objectiver chez certains patients une FEVG normale. Le diagnostic de l’insuffisance cardiaque à FEVG préservée est donc plus difficile (voir encadré), car on n’observe pas de dilatation ventriculaire, mais il s’y associe souvent une hypertrophie des parois ventriculaires et une dilatation de l’atrium gauche. On objective aussi souvent chez ces patients une altération de la fonction diastolique qui participe à l’altération du remplissage du ventricule – et explique, en partie, l’hypertension veineuse en amont. La diminution fréquente de la taille de la cavité ventriculaire (liée à une hypertrophie pariétale dite concentrique, voir plus loin), une FEVG souvent limite, une altération du remplissage conduisent en général à une diminution du débit cardiaque au repos ou à l’effort. La physiopathologie de l’insuffisance cardiaque à FEVG préservée est encore mal connue, ses spécificités cliniques et son pronostic se précisent, mais son traitement reste très discuté car aucune étude n’a actuellement montré de réelle efficacité des traitements à réduire la morbimortalité.
Dans ce chapitre seront abordés successivement la physiopathologie, les aspects anatomiques, histologiques, cellulaires et moléculaires du remodelage cardiaque, la séméiologie et certains marqueurs biologiques de l’insuffisance cardiaque ainsi que les bases, en particulier pharmacologiques, de son traitement. Avant la lecture de la suite de ce chapitre, il est fortement recommandé de lire ou de relire la section dédiée à la physiologie cardiaque dans le chapitre 1, Physiologie, Coeur, Adaptation du débit cardiaque.
________________________________________________________________________________
Différentes présentations de l’insuffisance cardiaque (définies selon les recommandations de la Société européenne de cardiologie 2012)
Trois conditions doivent être satisfaites pour retenir le diagnostic d’insuffisance cardiaque à FEVG altérée :
- symptômes typiques d’insuffisance cardiaque ;
- signes cliniques typiques ;
- diminution de la fraction d’éjection ventriculaire gauche < 40 %.
Quatre conditions doivent être satisfaites pour retenir le diagnostic d’insuffisance cardiaque à FEVG préservée :
- symptômes typiques d’insuffisance cardiaque ;
- signes cliniques typiques ;
- fonction ventriculaire gauche préservée (≥ 50 %) avec un ventricule gauche non dilaté ;
- altérations structurelles cardiaques (hypertrophie ventriculaire gauche/dilatation de l’atrium gauche) et/ou signes de dysfonction diastolique (anomalies du remplissage ventriculaire gauche).
Les patients avec une FEVG entre 40 % et 49 % se situent dans une « zone grise » et en 2016 la Société européenne de cardiologie reconnaissait finalement un 3e groupe, correspondant à ces altérations « légères » de la FEVG entre 40 % et 49 % afin d’optimiser la recherche et mieux définir les stratégies thérapeutiques et l’évaluation du pronostic dans ce sous-groupe de patients.
________________________________________________________________________________
Glossaire
- Insuffisance cardiaque chronique : présence d’une insuffisance cardiaque depuis quelques semaines.
- Insuffisance cardiaque décompensée : quand un patient stable sous traitement médicamenteux s’aggrave, on parle de décompensation.
- Insuffisance cardiaque aiguë : si l’épisode de décompensation survient soudainement, on parle d’insuffisance cardiaque aiguë.
- Insuffisance cardiaque de novo : premier épisode d’insuffisance cardiaque, pouvant survenir de façon aiguë (lors d’un infarctus, par exemple) ou de façon progressive chez un patient qui avait une altération de la fonction ventriculaire gauche asymptomatique.
- Insuffisance cardiaque compensée : les symptômes et signes ont disparu mais l’atteinte ventriculaire persiste et les patients restent donc à risque de détérioration clinique. Dans certains cas, la guérison peut être complète spontanément (myocardite) ou avec le traitement médical (cardiomyopathie dilatée primitive).
- Insuffisance cardiaque congestive : terme utilisé pour les patients avec une insuffisance cardiaque aiguë ou chronique ayant des signes congestifs (c’est-à-dire de rétention hydrosodée).
- Insuffisance cardiaque avancée : elle concerne les stades évolués de l’insuffisance cardiaque. L’insuffisance devient réfractaire au traitement médical et les alternatives chirurgicales, transplantation cardiaque ou assistance circulatoire sont discutées.
Tous ces termes peuvent s’appliquer au même patient en fonction du moment du diagnostic, de l’évolution, de la réponse au traitement et des rechutes.
________________________________________________________________________________
Physiopathologie
Remodelage cardiaque physiologique et pathologique
L’insuffisance cardiaque dans sa forme chronique, qu’elle soit à fraction d’éjection altérée ou préservée, se développe à l’occasion d’un processus appelé remodelage du cœur, terme qui signifie que le cœur devient progressivement différent du cœur normal. Cette différence concerne aussi bien l’aspect extérieur, anatomique, du cœur, sa masse, la composition histologique du myocarde, la structure des myocytes et de la matrice extracellulaire, les protéines constitutives des myocytes par modification de l’expression de leurs gènes. Ce remodelage traduit la plasticité du cœur qui se remodèle tout au long de la vie, de l’embryogenèse au développement anténatal, à la croissance postnatale et au vieillissement. On distingue un remodelage bénéfique, adaptatif observé par exemple chez le sportif et la femme enceinte et un remodelage pathologique, délétère ( maladaptive remodelling des auteurs anglo-saxons) qui conduit progressivement à l’insuffisance cardiaque.
Différents niveaux du remodelage
Trois et même quatre niveaux sont à considérer pour décrire le remodelage cardiaque : (i) le niveau anatomique constitué par le ventricule, ses dimensions, sa masse ; (ii) le myocarde en tant que tissu avec ses cellules musculaires (cardiomyocytes), non musculaires, son tissu interstitiel, ses vaisseaux ; (iii) les cardiomyocytes avec leurs dimensions et leur micro-architecture ; (iv) enfin, les protéines constitutives des cardiomyocytes et des autres cellules du myocarde. Chaque niveau peut être concerné à des degrés divers au cours du remodelage, tant physiologique que pathologique.
Remodelage du ventricule
On considère classiquement que le ventricule gauche se remodèle en réponse à la modification chronique, c’est-à-dire durable, de ses conditions de charge (précharge et/ou postcharge, voir chapitre 1, Physiologie, Coeur, Adaptation du débit cardiaque) ayant pour conséquence d’augmenter son travail hémodynamique, afin de préserver son VES tout en maintenant les conditions de charge du myocarde et des cardiomyocytes aussi proches de la normale que possible, tant en systole qu’en diastole. Ce remodelage, dont l’aspect le plus emblématique est l’hypertrophie ventriculaire c’est-à-dire l’augmentation de la masse du/des ventricule(s) exposé(s) à la surcharge hémodynamique, revêt un aspect adaptatif, tant au niveau de la pompe qu’au niveau du fonctionnement du myocarde et des cardiomyocytes clairement mis en évidence par la loi de Laplace : σ = k.P.r/e (voir chapitre 1, Physiologie, Coeur, Adaptation du débit cardiaque).
Remodelage concentrique
Dans les augmentations chroniques de la postcharge du ventricule gauche, également appelées surcharges de pression (hypertension artérielle, rétrécissement aortique, etc.), il existe une élévation chronique de la pression intraventriculaire pendant la systole responsable d’une augmentation de la contrainte pariétale σ. Afin de maintenir cette contrainte aussi proche que possible de sa valeur normale, on observe une augmentation de l’épaisseur e de la paroi du VG, accompagnée souvent d’une diminution du rayon r, aboutissant à la classique hypertrophie concentrique du VG.
Remodelage excentrique
Dans les augmentations chroniques de la précharge du ventricule, appelées également surcharges de volume ou de débit (augmentation du retour veineux chez certains sportifs, fuites valvulaires, etc.), celui-ci va avoir tendance à se dilater ce qui augmente le rayon r et ainsi la contrainte σ, aussi bien en diastole qu’en systole. Là encore, l’adaptation du VG afin de préserver une contrainte normale se fait par une augmentation plus modérée de l’épaisseur de sa paroi aboutissant à l’hypertrophie excentrique du VG.
Remodelage du myocarde
Selon les deux modalités décrites ci-dessus, le myocarde voit sa masse augmenter, définissant ainsi l’hypertrophie ventriculaire. Cette hypertrophie résulte de modifications concernant les cardiomyocytes, les autres cellules du myocarde, dont les cellules interstitielles et vasculaires et la matrice extracellulaire. Les cardiomyocytes constituent 70 à 80 % du volume du myocarde mais ne représentent que 35 % du nombre total de cellules cardiaques chez l’adulte. En réponse à l’augmentation des contraintes pariétales, ces cardiomyocytes s’hypertrophient. Leur capacité de prolifération est très faible car ils sont dits « terminalement différenciés », mais il semblerait qu’un très faible pourcentage d’entre eux soit capable de se dédifférencier et de retourner ainsi dans le cycle de division cellulaire. Au contraire, les autres types cellulaires (cellules endothéliales, musculaires lisses, fibroblastes, etc.) se multiplient et permettent, le cas échéant, une adaptation vasculaire avec développement du réseau capillaire, et une augmentation de la matrice extracellulaire (MEC) plus ou moins proportionnelle à l’hypertrophie des cardiomyocytes. Cette adaptation vasculaire fait néanmoins défaut dans l’hypertrophie pathologique.
Remodelage des cardiomyocytes et de leurs protéines
Le remodelage des cardiomyocytes et de leurs protéines diffère selon le type de surcharge et le caractère physiologique ou pathologique du remodelage. Globalement, dans les augmentations chroniques de postcharge, les cardiomyocytes grossissent par augmentation de leur épaisseur du fait de l’adjonction de sarcomères « en parallèle ». Au contraire, dans les augmentations chroniques de précharge les myocytes s’épaississent peu mais s’allongent du fait d’une adjonction de sarcomères « en série ». Ces modifications concernent également les organites intracellulaires (réticulum sarcoplasmique, mitochondries, etc.) et sont le fait d’une augmentation de la synthèse protéique globale. Mais celle-ci n’est pas uniforme et certains gènes sont plus transcrits que d’autres.
Remodelage physiologique (adaptive remodelling)
Le remodelage est dit physiologique quand il participe à l’adaptation globale de l’organisme à des mod£ifications non pathologiques, c’est-à-dire observées dans des situations normales de la vie telles que la grossesse et les efforts physiques répétés, qu’ils soient professionnels ou réalisés dans un contexte sportif. Les efforts isométriques, statiques, en force, ont tendance à augmenter de façon importante la pression artérielle systolique et donc la postcharge (surcharge de pression) et favorisent l’hypertrophie de la paroi myocardique sans dilatation cavitaire, définissant l’hypertrophie concentrique, visant à normaliser la contrainte pariétale. À l’inverse, les efforts isotoniques, dynamiques, d’endurance entraînent une augmentation du débit cardiaque soutenu à l’effort et donc une surcharge volumétrique (surcharge de débit, surcharge de volume). Le cœur s’adapte à cette surcharge en se dilatant. L’hypertrophie de la paroi, plus modérée, est secondaire à l’augmentation du rayon (loi de Laplace), définissant l’hypertrophie excentrique. La grossesse normale comporte une hypertrophie cardiaque de l’ordre de 10 à 15 %. On observe au contraire chez les spationautes subissant une apesanteur prolongée une hypotrophie cardiaque du même ordre. La caractéristique de ces remodelages est qu’ils n’altèrent pas l’histologie du myocarde, notamment sa vascularisation et sa MEC, garantissant ainsi leur réversibilité complète quand la cause du remodelage disparaît. Contrairement aux remodelages pathologiques, ils ne s’accompagnent pas d’un pronostic péjoratif (pas d’augmentation de la morbimortalité).
Remodelage pathologique (maladaptive remodelling)
Le remodelage cardiaque peut également être pathologique ou délétère (qui est une traduction de l’anglais « maladaptive », préférable au barbarisme « maladaptatif »), lorsqu’il survient dans un contexte pathologique, en réponse à une large variété de stimulus hémodynamiques (surcharge barométrique, volumétrique, asynchronisme, etc.), neurohormonaux (activation des systèmes sympathique, rénine-angiotensine-aldostérone), ou de lésions myocardiques (myocardite, infarctus, par exemple).
Dans ces circonstances, l’hypertrophie concentrique ou excentrique revêt toujours la valeur de mécanisme d’adaptation de la pompe VG, qui vise à diminuer sa contrainte pariétale et à maintenir ainsi le débit cardiaque, mécanisme initialement bénéfique en termes d’économie musculaire (consommation d’énergie). Cependant, le remodelage hypertrophique est accompagné de modifications du myocarde et des cardiomyocytes qui conduisent progressivement à une détérioration de la fonction systolique et diastolique et à l’insuffisance cardiaque en cas de persistance du stimulus pathologique (hypertension, séquelles de l’infarctus, valvulopathies, etc.) ou de la lésion myocardique.
Signaux à l’origine du remodelage pathologique
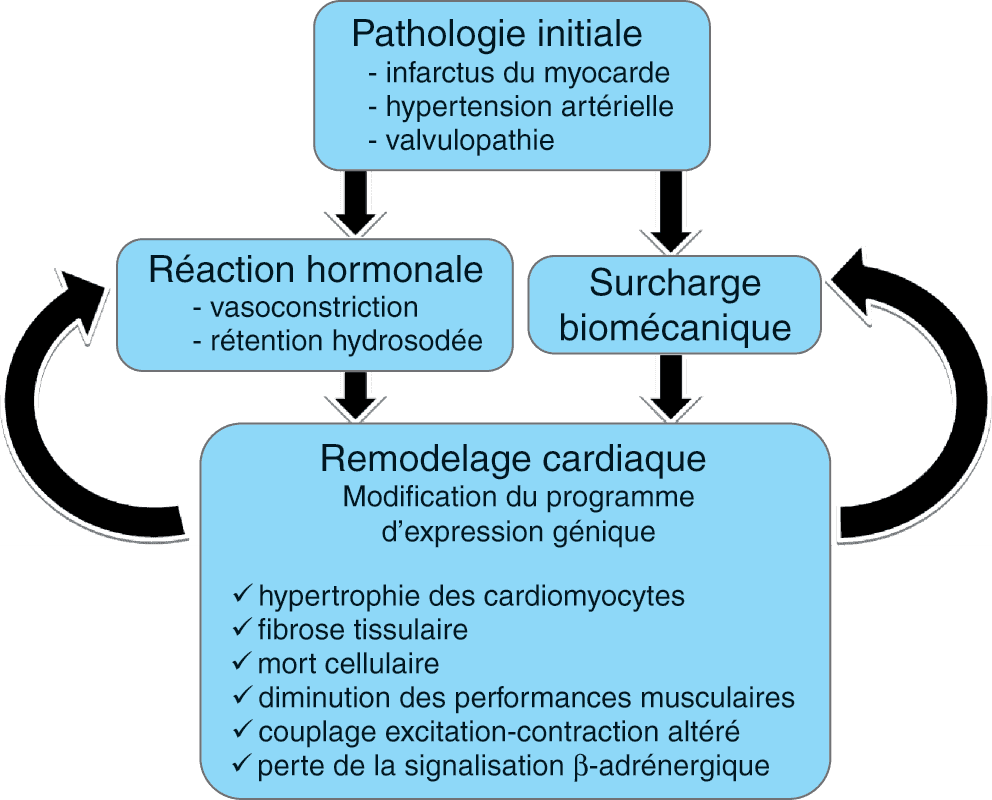
Dans les contextes pathologiques évoqués ci-dessus, deux grands types de signaux stimulent le remodelage conduisant à l’insuffisance cardiaque : la surcharge biomécanique et l’activation neurohormonale (fig. 5.1).
________________________________________________________________________________
Figure 5.1. Signaux à l’origine du remodelage pathologique.
________________________________________________________________________________
Surcharge biomécanique
La surcharge biomécanique imposée au muscle cardiaque entraîne une augmentation des contraintes systolique ou diastoliques, avec en diastole, une augmentation de l’étirement ( stretch) des cardiomyocytes et des cellules de la matrice. Ce signal est principalement intégré dans les cellules par trois mécanismes :
- les molécules d’intégrines qui sont des capteurs biomécaniques intégrés à la membrane cellulaire et qui lient des molécules de la matrice extracellulaire ;
- des canaux ioniques membranaires activés par l’étirement cellulaire ;
- des protéines ancrées dans la ligne Z des sarcomères telles que la titine qui agit comme un ressort moléculaire plus ou moins étiré pendant la diastole et participant ainsi à l’élasticité du myocarde (voir chapitre 1, figure 1.12).
Activation neurohormonale
La réaction neurohormonale est secondaire à la baisse de la pression artérielle induite par la baisse des performances contractiles cardiaques qui active le baroréflexe (voir chapitre 2.1, Régulation de la pression artérielle, Régulation à court terme : le baroréflexe artériel). Elle vise à maintenir la pression de perfusion des organes. Elle implique de nombreux systèmes hormonaux, regroupés en deux catégories suivant leur action vasoconstrictrice ou vasodilatatrice (leur activation dans l’insuffisance cardiaque est détaillée dans la section « Physiopathologie » intégrée ci-après) :
- le système sympathique, le système rénine-angiotensine-aldostérone (SRAA), l’arginine-vasopressine et l’endothéline sont les principaux systèmes/agents vasoconstricteurs impliqués ;
- les peptides natriurétiques, le monoxyde d’azote (NO), les prostaglandines et la bradykinine sont les principaux systèmes vasodilatateurs impliqués.
Ces systèmes contrôlent également la volémie et la natriurèse.
Globalement, la réaction hormonale survenant dans l’insuffisance cardiaque systolique induit une vasoconstriction et stimule la rétention hydrosodée.
De plus, certaines molécules ont des actions spécifiques directes sur le muscle cardiaque ou sur d’autres organes. L’aldostérone a une action pro-fibrosante cardiaque mais également rénale. Le tumor necrosis factor α (TNFα) n’a pas d’action hémodynamique significative mais c’est une molécule pro-inflammatoire qui induit une cachexie et une atrophie musculaire.
Les cellules cardiaques (en particulier les cardiomyocytes) possèdent des récepteurs capables d’intégrer les signaux de ces différents systèmes. Ce sont souvent des récepteurs à sept domaines transmembranaires couplés à des protéines G.
Il est important de noter que ces systèmes sont souvent aussi activés in situ dans le cœur, ce qui veut dire qu’ils fonctionnent également sur un mode paracrine voire autocrine. Le cœur est par exemple capable de produire de l’angiotensinogène et de le transformer localement en angiotensine II qui se fixe directement sur les récepteurs à l’angiotensine II des cellules cardiaques. Ainsi, le niveau sanguin de telle ou telle hormone n’est pas toujours un bon reflet de sa concentration dans le tissu cardiaque et de son impact sur le remodelage cardiaque.
Les voies de signalisation qui transduisent les différents signaux mécaniques et neurohormonaux aux noyaux des cardiomyocytes et autres cellules du myocarde pour entraîner une modification de l’expression de leurs gènes sont très nombreuses, complexes et intriquées, et ne seront pas détaillées ici.
Différentes composantes du remodelage pathologique
Les signaux biomécaniques et hormonaux modifient profondément le programme d’expression des gènes dans les cellules cardiaques et remodèlent ainsi le phénotype des cellules et de la matrice extracellulaire du myocarde. C’est le point central du remodelage cardiaque cellulaire. On parle souvent de réexpression du phénotype fœtal : on observe la réexpression de gènes spécifiquement exprimés lors de la vie fœtale, comme certaines isoformes de myosine et les peptides natriurétiques.
Ce remodelage est complexe, influencé par de nombreux facteurs propres à chaque individu. Néanmoins, cet ensemble de modifications peut être globalement regroupé autour de grandes fonctions cellulaires.
Hypertrophie des cardiomyocytes
Dans les cardiomyocytes, il existe une augmentation de la synthèse protéique et une diminution de l’activité des systèmes de contrôle-qualité et de recyclage des protéines. Ces modifications favorisent l’hypertrophie cellulaire qui participe, avec l’augmentation de la fibrose, à l’hypertrophie du myocarde. Il n’existe pas (ou très peu) de prolifération (hyperplasie) des cardiomyocytes dans l’insuffisance cardiaque, au contraire d’autres types cellulaires comme les fibroblastes, les cellules musculaires lisses vasculaires ou les cellules endothéliales.
Fibrose tissulaire
Le remodelage cardiaque pathologique est associé à une augmentation du volume et à une modification de la composition de la matrice extracellulaire, avec production accrue de collagène stimulée par la prolifération des fibroblastes. Cette fibrose conduit à une augmentation de la rigidité pariétale, une diminution du couplage mécanique entre cardiomyocytes et des anomalies de la conduction électrique cardiaque.
Mort cellulaire augmentée
L’insuffisance cardiaque est également associée à une diminution du nombre de cardiomyocytes dans le myocarde. Elle est liée, d’une part, à l’absence de prolifération et, d’autre part, à différents mécanismes de mort cellulaire dont l’activité est augmentée au cours du remodelage pathologique, comme l’apoptose et l’autophagie. Enfin, certaines pathologies causales comme l’ischémie myocardique induisent également les mécanismes de mort cellulaire d’origine hypoxique.
Diminution des performances du myocarde
Le remodelage modifie l’expression de protéines du sarcomère, en particulier celle des isoformes des chaînes lourdes de la myosine qui passent du type α au type β. Ces modifications permettent initialement une adaptation du muscle en diminuant sa vitesse de raccourcissement. Il s’agit d’une mesure d’économie musculaire qui permet de s’adapter à l’augmentation des contraintes mécaniques mais qui, sur le long terme, diminue la performance cardiaque. Ce phénomène mis en évidence chez les murins a peu d’importance chez l’homme dont la myosine ventriculaire est déjà essentiellement de type β. Au contraire, les altérations du couplage excitation-contraction et de la recapture diastolique du Ca2 + dans le réticulum sarcoplasmique (RS) par sa Ca2 + (SERCA2a) (voir chapitre 1, figure 1.11) jouent un rôle majeur dans l’altération des performances contractiles du myocarde chez l’homme. En effet, le remodelage moléculaire altère la libération du Ca2 + par le RS qui lie l’activation membranaire (le PA) et le déclenchement de la contraction au niveau du sarcomère. Il en résulte une diminution de la quantité de Ca2 + nécessaire pour activer la contraction en systole et ainsi une diminution des performances contractiles du myocarde. La diminution des capacités de recaptage du Ca2 + dans le RS en diastole conduit pour sa part à la persistance d’un taux diastolique important de Ca2 + dans le cytosol, ce qui altère la relaxation et favorise le déclenchement de troubles du rythme ventriculaire (voir chapitre 6).
Altération du métabolisme énergétique
Un autre aspect important du remodelage pathologique du cardiomyocyte concerne la production et l’utilisation de l’énergie qui aggrave la dysfonction contractile et celle du recyclage cellulaire du Ca2 +. Les phases précoces du remodelage comportent une transition de la consommation préférentielle des acides gras vers celle du glucose avec une redistribution des isoformes de la créatine kinase (CK), l’ensemble s’intégrant dans la réexpression du programme génique fœtal. Malheureusement, la progression vers l’IC ne s’accompagne pas d’une expression suffisante des enzymes glycolytiques et d’autres altérations s’y associent : altération de la production mitochondriale d’ATP, diminution du rapport PCr/ATP, augmentation de la concentration en ADP, défaut d’apport énergétique aux ATPases (myosine, SERCA, Na/K-ATPase, etc.), en particulier lors de l’effort.
Altération de la signalisation β1-adrénergique
En réponse à l’activation chronique du système sympathique, il existe une diminution du nombre de récepteurs β1-adrénergiques à la surface des cardiomyocytes. Il s’agit initialement d’une mesure de protection car la stimulation adrénergique chronique est délétère pour le cardiomyocyte, favorisant entre autres le remodelage délétère et la mort cellulaire. En revanche, la cellule est moins sensible aux catécholamines, dont le rôle est essentiel dans l’adaptation cardiaque à l’effort, ce qui est un signe important de l’insuffisance cardiaque.
________________________________________________________________________________
Remarques importantes
Le concept de remodelage a deux conséquences importantes pour la prise en charge de la maladie :
- le remodelage moléculaire est présent avant l’apparition des symptômes. Ceci veut dire que si on pouvait dépister les premiers signes du remodelage à partir de biomarqueurs facilement accessibles, comme un dosage sanguin, on pourrait prédire l’apparition de la maladie de manière beaucoup plus précoce qu’aujourd’hui et envisager des stratégies ciblées de prévention. De nombreuses recherches dans ce domaine sont en cours ;
- l’intensité du remodelage est positivement corrélée à la sévérité de la maladie. On dispose de marqueurs sanguins du remodelage cardiaque, dont le taux est corrélé à la sévérité de la maladie, qui permettent ainsi d’obtenir, en complément de l’évaluation clinique indispensable, une évaluation quantitative, non subjective et reproductible de la sévérité de la maladie. De nombreux marqueurs sont déjà identifiés. Certains, comme le peptide natriurétique de type B (BNP), sont déjà utilisés en routine chez l’insuffisant cardiaque.
À l’échelle moléculaire, comme à l’échelle de l’organe, ce remodelage n’est pas strictement identique pour tous les patients et est modulé par la pathologie causale, les facteurs de risque cardiovasculaire, l’existence de comorbidités et les traitements. Il s’agit d’un processus complexe qui affecte plusieurs types cellulaires distincts et touche de nombreuses fonctions cellulaires.
________________________________________________________________________________
Modifications des boucles pression-volume
Insuffisance cardiaque à FEVG altérée
Dans cette forme d’insuffisance cardiaque, c’est la dysfonction systolique qui prédomine. La pente de la relation PTS/VTS (élastance télésystolique ; voir chapitre 1, figure 1.16) est diminuée ce qui indique une diminution de la contractilité du VG (fig. 5.2A, flèche rouge) : pour maintenir son volume d’éjection et ainsi son débit et la pression artérielle, le ventricule doit se dilater. La fraction d’éjection (VES/VTD) diminue donc. Le ventricule défaillant est très sensible à une variation de la postcharge.
________________________________________________________________________________
Figure 5.2. Modification des boucles pression-volume dans les deux formes d’insuffisance cardiaque.
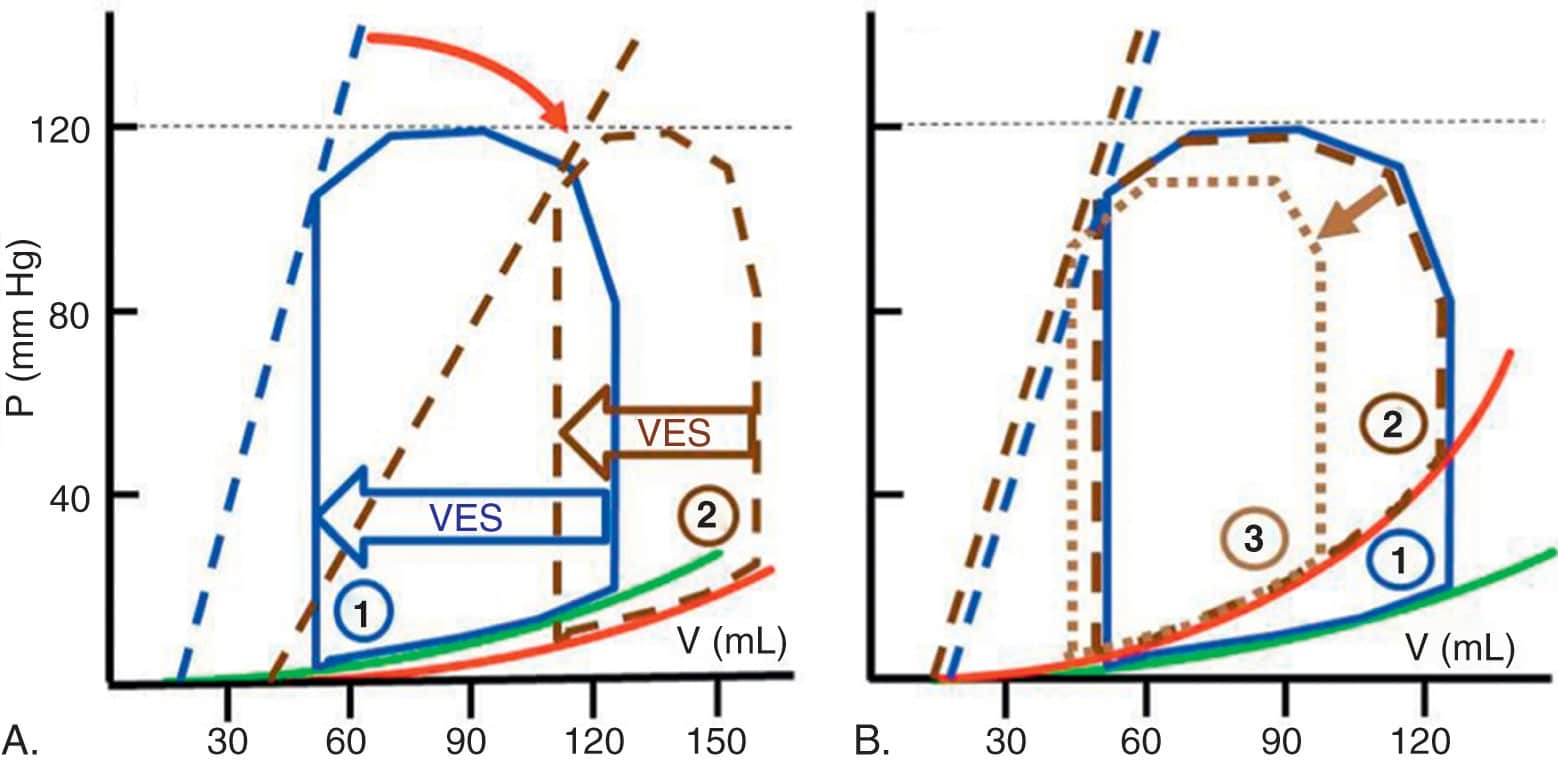
A. Insuffisance cardiaque à FEVG altérée. Par rapport à la boucle du VG normal (1, boucle bleue), la boucle du VG défaillant est décalée vers la droite car le VG doit se dilater pour tenter de maintenir son VES avec une FEVG abaissée (2, boucle marron foncé). La phase de remplissage s’inscrit sur une courbe (rouge) peu différente de celle du cœur normal (verte). La principale différence concerne la diminution de la contractilité du VG mise en évidence par la diminution de la pente de la relation PTS/VTS (flèche rouge) avec pour conséquence une diminution du VES ce qui diminue encore la FEVG.
B. Insuffisance cardiaque à FEVG préservée. La principale différence concerne la phase de remplissage du VG qui s’inscrit sur une courbe (rouge) déviée en haut et à gauche par rapport à celle du VG normal (verte). Pour un même volume de remplissage, la PTDVG est plus élevée traduisant une diminution de la compliance du VG. En revanche, la pente de la relation PTS/VTS n’est pas significativement diminuée, indiquant le maintien d’une fonction systolique satisfaisante. Pour des pressions atriales gauches normales ou basses, le remplissage ventriculaire et le VES sont diminués. C’est ce que l’on observe par exemple après un traitement diurétique (3, boucle et flèche marron clair).
________________________________________________________________________________
Insuffisance cardiaque à FEVG préservée
Dans cette forme d’insuffisance cardiaque, c’est la dysfonction diastolique qui prédomine. La courbe de remplissage du VG est déplacée en haut et à gauche traduisant une diminution de sa compliance (= augmentation de sa rigidité (fig. 5.2B ; voir aussi chapitre 1, figure 1.15). Le ventricule a des dimensions normales voire diminuées (hypertrophie concentrique). Le même volume télédiastolique n’est obtenu qu’au prix d’une élévation de la pression diastolique. Le ventricule n’étant pas dilaté et ses performances contractiles étant préservées, la fraction d’éjection est conservée. Le ventricule est très sensible à une variation (augmentation et baisse) de précharge.
Physiopathologie intégrée
L’insuffisance cardiaque à FEVG altérée était la forme la plus fréquente en France (60 %) jusqu’au début des années 2000. Mais depuis cette époque, la prévalence de l’insuffisance cardiaque à FEVG préservée augmente régulièrement en France, dans les pays du nord de l’Europe et aux États-Unis, dépassant celle de l’insuffisance cardiaque à FEVG altérée.
Mécanismes initiateurs
Insuffisances ventriculaires
Insuffisance cardiaque à FEVG altérée
Les grands mécanismes sont principalement :
- une surcharge mécanique chronique du ventricule par augmentation du volume à éjecter (fuites valvulaires) ou par une gêne à l’éjection (hypertension artérielle, rétrécissement valvulaire aortique), bien que celle-ci soit également pourvoyeuse d’insuffisance cardiaque à FEVG préservée ;
- une diminution de la contractilité du ventricule, qui peut être d’origine primaire, comme dans les cardiomyopathies dilatées primitives, ou secondaires, dues à un infarctus du myocarde ou une cause toxique (alcool), médicamenteuse (chimiothérapie anticancéreuse par anthracyclines), infectieuse, une myocardite, etc.
Schématiquement, plus l’altération de la fonction contractile est importante, plus le patient est symptomatique, plus les mécanismes compensateurs (remodelage cardiaque, activation neurohormonale) sont activés et plus le pronostic est altéré.
Insuffisance cardiaque à FEVG préservée
Les mécanismes en sont complexes et moins bien connus que ceux de l’insuffisance cardiaque à FEVG altérée. Plusieurs facteurs sont impliqués, à la fois myocardiques et vasculaires, avec des interactions fortes entre diminution de la compliance du ventricule (altération de la fonction diastolique) et augmentation de la rigidité artérielle : le ventricule se vide correctement mais a du mal à se remplir – notamment la fonction d’aspiration du sang par le ventricule en début de diastole est altérée – ou bien il se remplit au prix d’une augmentation des pressions de remplissage (élévation de la PTDVG) et d’amont, ce qui contribue à la congestion veineuse en amont des cavités cardiaques et à une augmentation insuffisante du débit cardiaque à l’effort. Elle touche particulièrement les sujets âgés, hypertendus.
On classe également dans ce groupe les cardiopathies qui s’accompagnent d’une augmentation de la rigidité du myocarde :
- les cardiopathies liées à l’infiltration du myocarde par une protéine anormale (amylose cardiaque) ;
- les cardiomyopathies hypertrophiques d’origine génétique.
Les deux mécanismes, altération de la fonction systolique et de la fonction diastolique, peuvent coexister et participer conjointement aux signes cliniques.
Insuffisance cardiaque sans insuffisance ventriculaire
Rétrécissement mitral
Il réalise un obstacle valvulaire à l’écoulement du sang entre l’atrium et le ventricule gauche. Il s’accompagne ainsi d’un remodelage de l’atrium gauche (dilatation et hypertrophie) et d’une augmentation des pressions veineuses pulmonaires.
Péricardite constrictive
La péricardite constrictive entraîne une gêne au remplissage des cavités cardiaques dans un sac péricardique inextensible et peut entraîner un tableau d’insuffisance cardiaque droite, gauche ou globale. Les fonctions myocardiques sont généralement préservées.
Mécanismes d’adaptation
L’essentiel des travaux de recherche physiopathologique a porté sur l’insuffisance cardiaque à FEVG altérée et dans la suite de cette section, les informations ne concerneront que ce type d’insuffisance cardiaque. On observe, actuellement, le développement important de travaux de recherche fondamentale et clinique sur l’insuffisance cardiaque à FEVG préservée mais ils restent limités par la rareté des modèles expérimentaux animaux.
En réponse à l’altération de la fonction contractile du VG et notamment à la baisse de la pression artérielle qui en résulte, sont mis en jeu des mécanismes compensateurs. Ils sont de trois ordres :
- cardiaques ;
- périphériques ;
- neurohormonaux.
Mécanismes d’adaptation cardiaques
Loi de Frank-Starling
Selon la loi de Frank-Starling, l’augmentation du remplissage ventriculaire accentue l’étirement des myocytes cardiaques et augmente la force de la contraction ventriculaire ; mais le rendement de la contraction est moindre que chez les sujets normaux car le mécanisme perd de son efficacité sur un VG dilaté au myocarde remodelé. Ainsi, l’augmentation du débit cardiaque est limitée (fig. 5.3). La dilatation du ventricule s’accompagne d’une augmentation progressive de ses pressions de remplissage qui favorise l’installation des signes congestifs.
________________________________________________________________________________
Figure 5.3. Loi de Frank-Starling en situation d’insuffisance cardiaque.
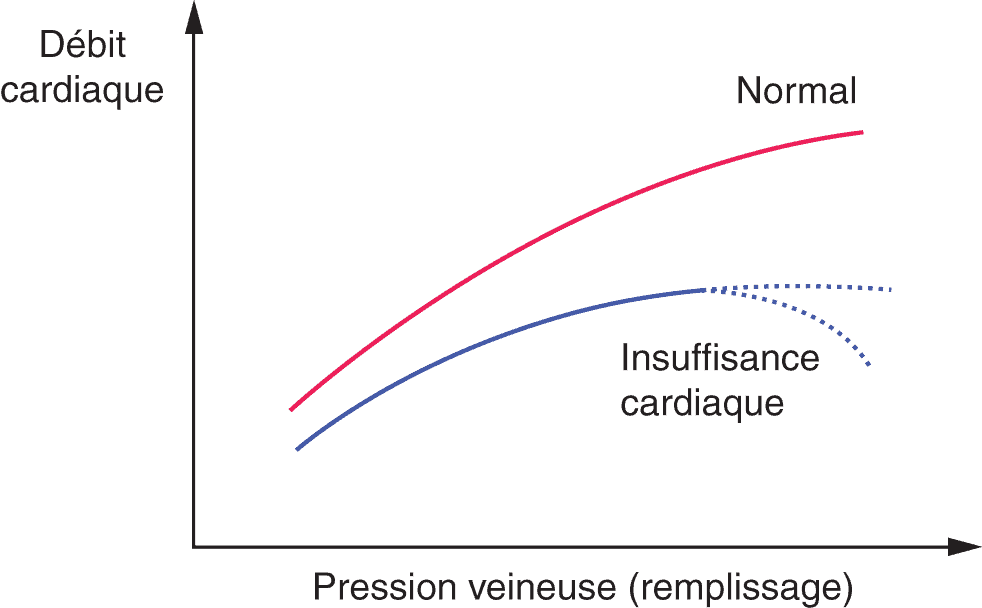
En cas d’insuffisance cardiaque associée à une dilatation du VG et à un remodelage du myocarde, l’augmentation du débit cardiaque secondaire à l’augmentation des pressions de remplissage ventriculaire, notamment lors de l’effort, reste limitée.
________________________________________________________________________________
Remodelage ventriculaire
Le remodelage ventriculaire (voir ci-dessus) permet de maintenir le VES, mais ce mécanisme est énergétiquement coûteux et délétère sur le long terme. On observe une modification de la géométrie du ventricule gauche qui perd sa forme ellipsoïde et tend à devenir sphérique.
Tachycardie sinusale
L’augmentation de la fréquence cardiaque, sous la dépendance de l’activation sympathique, permet une augmentation du débit cardiaque dans une certaine gamme de fréquence – au-delà de laquelle le raccourcissement du temps de remplissage devient délétère – là encore au prix d’un accroissement de la dépense énergétique cardiaque, donc délétère sur le long terme.
Mécanismes d’adaptation périphériques
Redistribution du débit sanguin
On observe une redistribution du débit sanguin vers les organes « nobles » : les circulations cérébrales et coronaires sont privilégiées aux dépens des circulations cutanée, rénale, splanchnique et musculaire squelettique, à l’origine de nombreux symptômes.
Libération facilitée de l’oxygène par l’hémoglobine
On observe une extraction accrue de l’oxygène par la périphérie qui se traduit par une augmentation de la différence artérioveineuse en oxygène. Cet accroissement est lié à une diminution de l’affinité de l’hémoglobine pour l’oxygène.
Mécanismes neuro-hormonaux
Systèmes vasoconstricteurs (fig. 5.4)
La baisse de pression artérielle enregistrée par les barorécepteurs localisés dans les sinus carotidiens et l’arche aortique d’une part, et les tensorécepteurs localisés au niveau de l’artériole afférente des glomérules rénaux d’autre part, entraîne la mise en jeu de mécanismes ayant pour objectif le maintien d’un niveau de pression nécessaire à la bonne perfusion des organes grâce à une vasoconstriction (à court terme) et une augmentation de la volémie (à plus long terme, voir chapitre 2.1, Régulation de la pression artérielle).
________________________________________________________________________________
Figure 5.4. Mécanisme d’activation des systèmes sympathique et rénine-angiotensine-aldostérone dans l’insuffisance cardiaque.
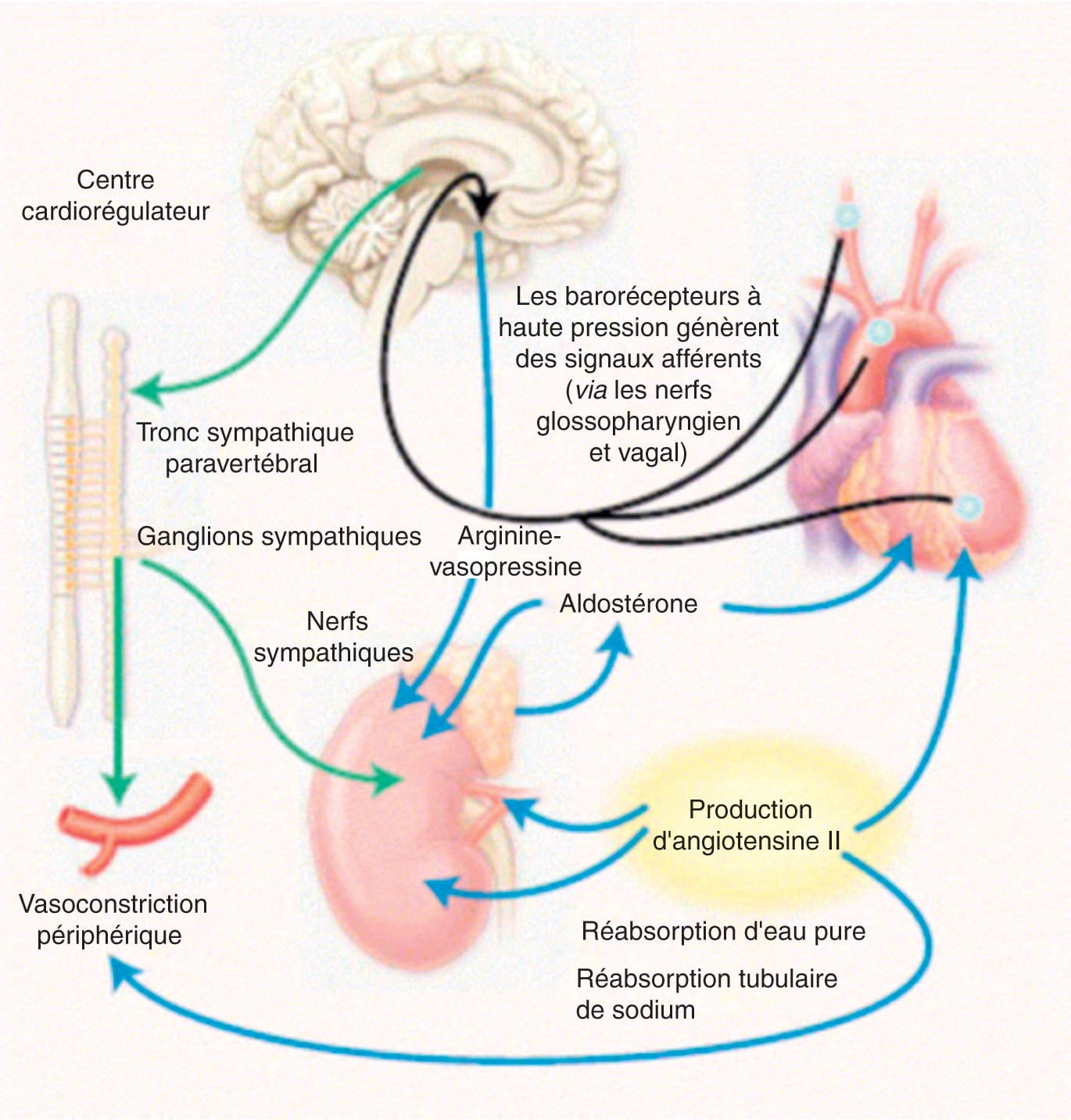
Source : d’après Chen HH, Schrier RW. Pathophysiology of volume overload in acute heart failure syndromes. Am J Med, 2006 ; 119 : S11–S16.
________________________________________________________________________________
Activation du système sympathique
Le système nerveux sympathique est le premier système neurohormonal mis en jeu dans la réponse vasoconstrictrice à la baisse de pression artérielle via la libération de noradrénaline par la terminaison des neurones postganglionnaires qui stimule les récepteurs α1-adrénergiques des cellules musculaires lisses vasculaires. Son activation persiste tout au long de l’évolution de la maladie non traitée. Les taux élevés de noradrénaline plasmatique sont associés à une mortalité accrue.
Au niveau cardiaque, la stimulation sympathique permet l’augmentation de la fréquence cardiaque – dont on a vu les limites – ainsi que l’augmentation de la contractilité du ventricule par stimulation des récepteurs β1-adrénergiques des myocytes cardiaques, mais au prix d’une augmentation des dépenses énergétiques qui s’avère délétère à long terme. L’efficacité de cette réponse, qui favorise les troubles du rythme cardiaque, diminue au cours du temps avec l’altération de la voie de signalisation β1-adrénergique (diminution de la densité et découplage des récepteurs, alias « down-regulation »). Au niveau rénal, l’activation des nerfs sympathiques rénaux stimule la sécrétion de rénine.
Les principaux effets délétères de l’activation sympathique chronique sont résumés dans la figure 5.5.
________________________________________________________________________________
Figure 5.5. Conséquences délétères de l’activation chronique du système sympathique.
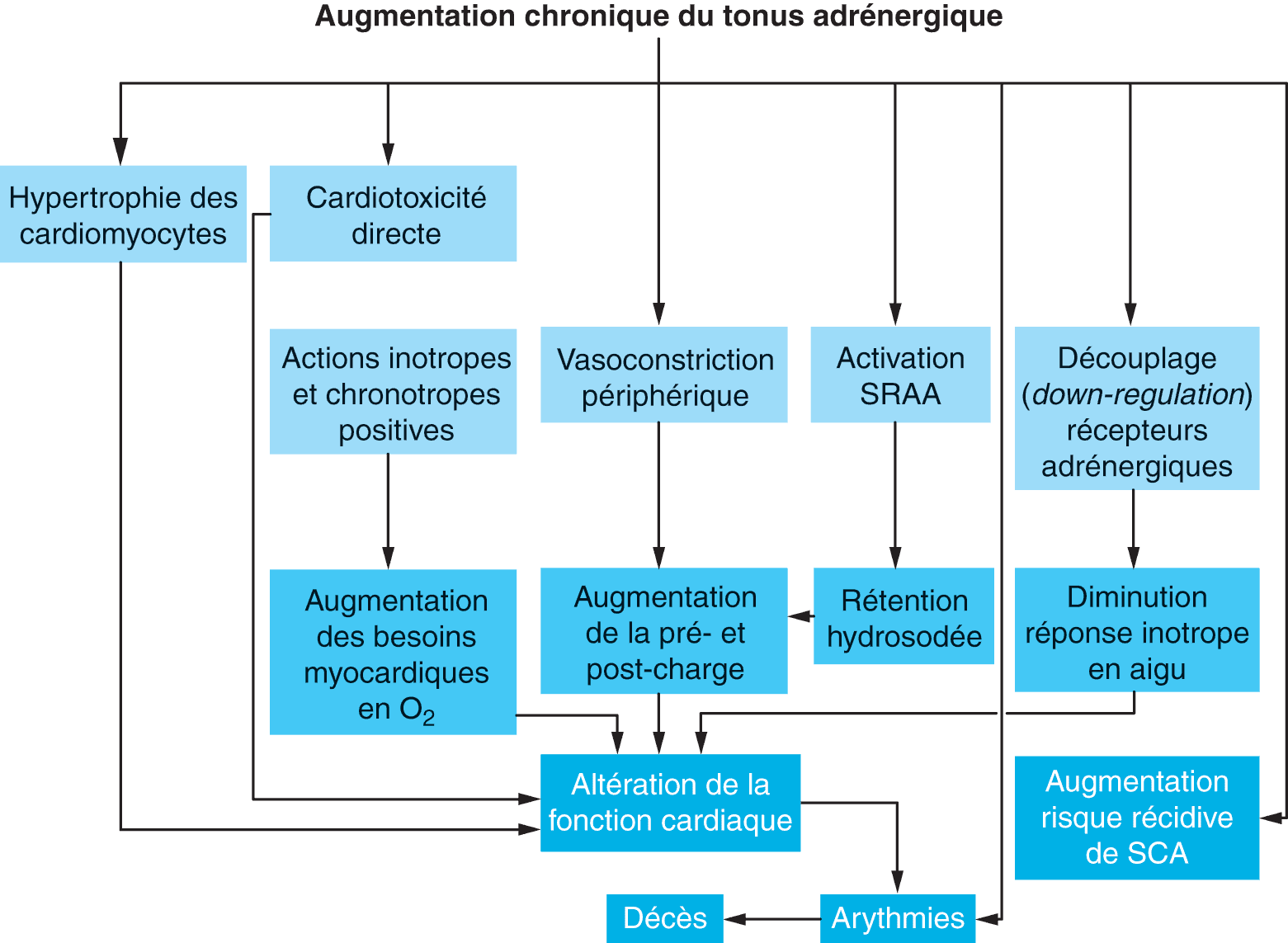
Source : d’après Bounhoure J-P. Actualités dans l’insuffisance cardiaque. Paris : John Libbey EUROTEXT ; 2001.
________________________________________________________________________________
Activation du système rénine-angiotensine-aldostérone (SRAA)
L’activation du SRAA aboutit à la production d’angiotensine II et d’aldostérone (voir chapitre 2.1, figure 2.2). Elle débute par la sécrétion plasmatique de rénine par les cellules de l’appareil juxta-glomérulaire en réponse à :
- la diminution de la pression de perfusion de l’artériole afférente de l’appareil juxtaglomérulaire, sensible à l’étirement ;
- une stimulation directe de l’appareil juxtaglomérulaire par le système sympathique et les catécholamines circulantes ;
- une diminution de la charge sodée au niveau de la macula densa.
La rénine transforme l’angiotensinogène d’origine hépatique en angiotensine I, molécule peu active, elle-même transformée en angiotensine II par l’enzyme de conversion de l’angiotensine (ECA), à la fois circulante et fixée à la surface des cellules endothéliales, surtout au niveau de la circulation pulmonaire.
L’angiotensine II :
- est un puissant agent vasoconstricteur ;
- stimule la sécrétion d’aldostérone par la corticosurrénale ;
- favorise la libération de catécholamines ;
- favorise la prolifération cellulaire.
La production d’angiotensine II augmente lors de chaque épisode de décompensation cardiaque.
L’aldostérone :
- favorise la réabsorption tubulaire de sodium ;
- favorise la perte de potassium (avec ses risques de troubles du rythme) ;
- participe au remodelage des cardiomyocytes ;
- est impliquée dans la fibrose interstitielle du myocarde.
Les systèmes sympathiques et le SRAA se coactivent, amplifiant ainsi les phénomènes délétères de l’activation neurohormonale prolongée sur le long terme (fig. 5.6).
________________________________________________________________________________
Figure 5.6. Boucles d’aggravation de l’insuffisance cardiaque systolique en l’absence de traitement.
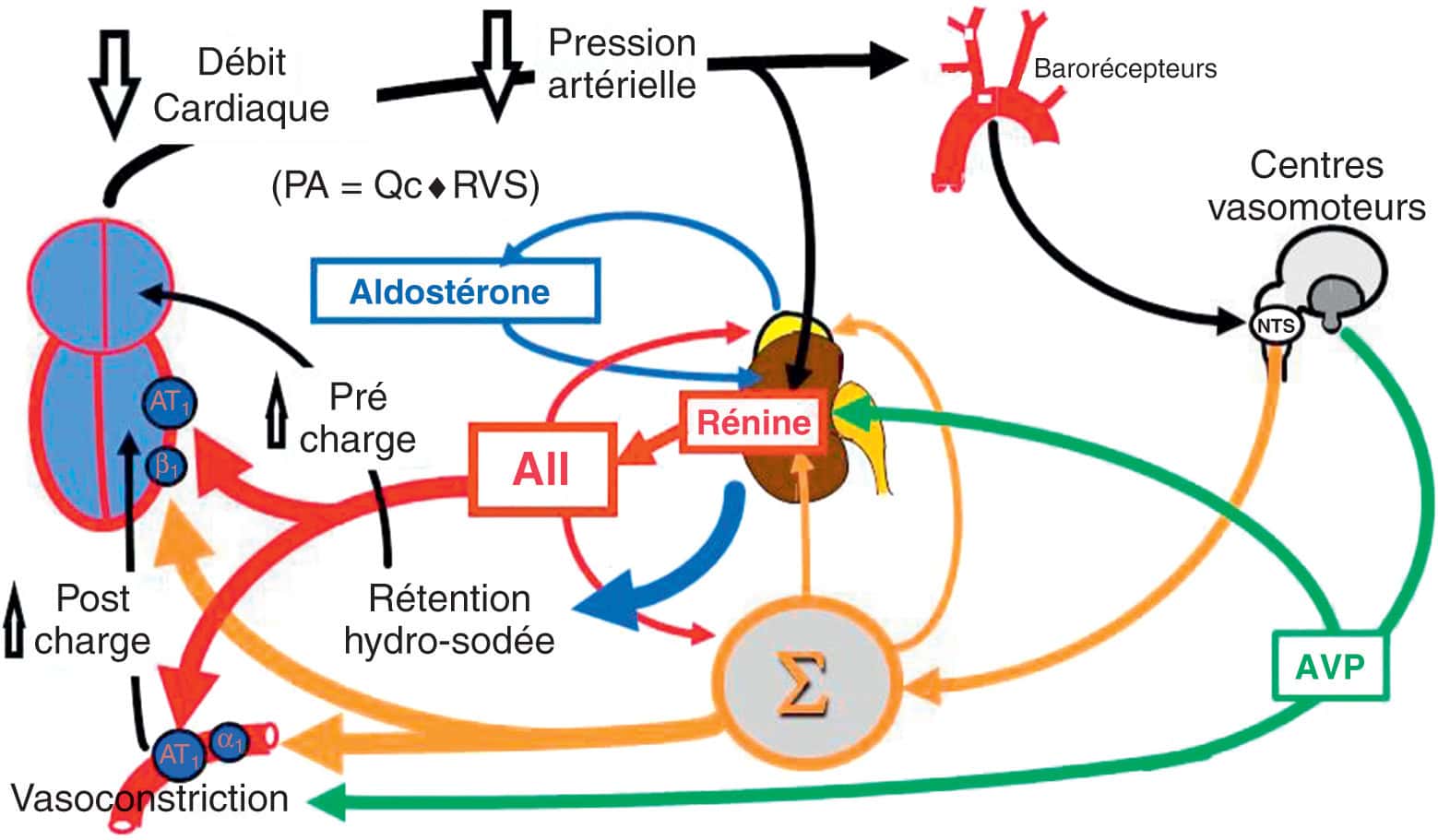
La baisse de la performance du ventricule gauche et du débit cardiaque entraînent une baisse de la PA perçue par les barorécepteurs aortiques et carotidiens. Ceci a pour effet de diminuer la stimulation qu’ils exercent sur le noyau du tractus solitaire (NTS) des centres vasomoteurs avec, pour conséquence, une diminution du tonus parasympathique et une augmentation du tonus sympathique (Σ), (voir chapitre 2.1). Cette augmentation exerce un effet inotrope positif sur le cœur (stimulation des récepteurs β1-adrénergiques des myocytes cardiaques par la noradrénaline), bénéfique à court terme mais délétère à long terme. Elle entraîne une vasoconstriction artériolaire (stimulation des récepteurs α1-adrénergiques des cellules musculaires lisses) délétère car augmentant la postcharge du VG. Au niveau rénal, l’augmentation du tonus sympathique joue de façon synergique avec la baisse de la PA pour activer la production de rénine qui aboutit, elle-même, à la production d’angiotensine II (AII). L’angiotensine II, en se fixant sur ses récepteurs AT1, favorise la vasoconstriction artériolaire et est synergique avec la stimulation sympathique pour stimuler la contractilité du VG. Elle stimule également les centres sympathiques au niveau du système nerveux central. Enfin, elle stimule la production d’aldostérone par les glandes surrénales, ce qui entraîne une réabsorption accrue de sel et d’eau au niveau rénal. Ceci a pour effet d’augmenter la volémie et la précharge. Enfin à un stade tardif, la stimulation de la production d’hormone antidiurétique (AVP) favorise la vasoconstriction artériolaire et entraîne la réabsorption d’eau libre au niveau rénal. Le cœur se trouve ainsi pris dans un cercle vicieux d’augmentation continue de la pré- et de la postcharge dans un contexte de stimulation cardiaque et vasculaire par la noradrénaline et l’angiotensine II qui favorisent leur remodelage délétère.
________________________________________________________________________________
Vasopressine
La sécrétion d’hormone antidiurétique est également stimulée par la baisse de la PA, ainsi que par l’augmentation de l’osmolarité plasmatique qui fait suite à l’augmentation de la réabsorption rénale du sodium sous l’effet de l’aldostérone. Elle survient plus tardivement et entraîne une réabsorption d’eau libre. Elle est la cause de l’hyponatrémie au stade d’insuffisance cardiaque terminale.
Endothéline
L’endothéline est un puissant vasoconstricteur qui a des actions vasculaires, rénales et cardiaques : elle favorise la synthèse de collagène et s’oppose localement aux effets du monoxyde d’azote (NO), en particulier au niveau de la microcirculation.
Systèmes vasodilatateurs
Les systèmes vasodilatateurs mis en jeu plus précocement ne peuvent cependant pas contrecarrer les systèmes vasoconstricteurs, dont l’effet prédomine puisque la pression artérielle étant la grandeur régulée du système cardiovasculaire, seule la vasoconstriction permet de pallier la défaillance de la pompe cardiaque.
Peptides natriurétiques
Le facteur atrial natriurétique (atrial natriuretic peptide, ANP) libéré lors de la distension atriale entraîne une vasodilatation artérielle et a un effet natriurétique comme le brain natriuretic peptide (BNP). La sécrétion de BNP est liée notamment à l’hypertrophie et l’étirement des cardiomyocytes ventriculaires et le taux circulant de BNP est corrélé à l’augmentation des pressions intraventriculaires (voir plus loin, « Marqueurs biochimiques de l’insuffisance cardiaque »). Le dosage du BNP ou du NT-proBNP est utile pour le diagnostic et la prise en charge des patients en insuffisance cardiaque. L’ANP et le BNP inhibent également la sécrétion de rénine et d’aldostérone.
Prostaglandines
Le système des prostaglandines s’oppose aussi aux effets vasoconstricteurs, en particulier au niveau des artérioles rénales glomérulaires afférentes.
Monoxyde d’azote (NO)
Dans l’insuffisance cardiaque, les propriétés de l’endothélium sont altérées et on observe, notamment en raison d’une diminution des forces de cisaillement (shear stress), une diminution de la production du monoxyde d’azote (NO) par les cellules endothéliales directement responsable d’une diminution du tonus vasodilatateur physiologique, mais également associée à la perturbation de nombreuses autres fonctions : génération d’un stress oxydant, altérations du métabolisme énergétique, de la contraction et de la relaxation, etc.
Autres mécanismes
D’autres mécanismes entrent en jeu dans la physiopathologie de l’insuffisance cardiaque mais leur rôle reste encore à préciser par des travaux de recherche fondamentale :
- l’inflammation et l’action des nombreuses cytokines pro- et anti-inflammatoires ;
- le stress oxydant ;
- la mort cellulaire programmée ;
- ainsi qu’un certain nombre de mécanismes réparateurs, tels que l’angiogenèse et la régénération cardiaque.
Désynchronisation électrique cardiaque
On observe chez 25 % des patients en insuffisance cardiaque des troubles de la conduction électrique atrioventriculaire (bloc atrioventriculaire) et intraventriculaire (bloc de branche gauche). Ces anomalies entraînent un défaut de synchronisation de la contraction entre atriums et ventricules et au sein même des ventricules avec, en particulier, un retard de contraction de la paroi latérale du VG. Ceci participe une altération supplémentaire de la contraction et du remplissage du VG, et peut aggraver une insuffisance mitrale.
Chez ces patients, les techniques de resynchronisation par stimulateur cardiaque permettent d’améliorer les symptômes et la survie en plus du traitement médicamenteux quand il s’avère insuffisant.
________________________________________________________________________________
Au total
L’hyperactivité du système sympathique et du SRAA permet de limiter la baisse de pression artérielle par une vasoconstriction qui l’emporte sur les mécanismes vasodilatateurs (fig. 5.7) et une augmentation de la volémie ; mais elle s’avère délétère à moyen et long terme car :
- l’augmentation de la postcharge ventriculaire gauche liée à l’augmentation des résistances vasculaires périphériques et à la dilatation du VG (loi de Laplace) altère la fonction VG et aggrave son remodelage délétère ;
- l’augmentation de la précharge aggrave également le remodelage délétère et entraîne l’apparition des signes congestifs ;
- ces adaptations sont obtenues au prix d’une augmentation de la dépense énergétique ;
- elles participent également, par leur action directe sur les myocytes et autres cellules du myocarde, à son remodelage délétère
L’insuffisance cardiaque est donc une « maladie de l’adaptation », associée à la mise en jeu de mécanismes compensateurs initialement bénéfiques mais finalement délétères. Ces mécanismes rendent compte des symptômes. L’inhibition du SRAA et du système sympathique, systèmes participant aux mécanismes initialement compensateurs mais dont l’activation est délétère à long terme, est à la base du traitement moderne de l’insuffisance cardiaque avec dysfonction systolique (voir plus loin).
________________________________________________________________________________
Figure 5.7. Activation neurohormonale dans l’insuffisance cardiaque.
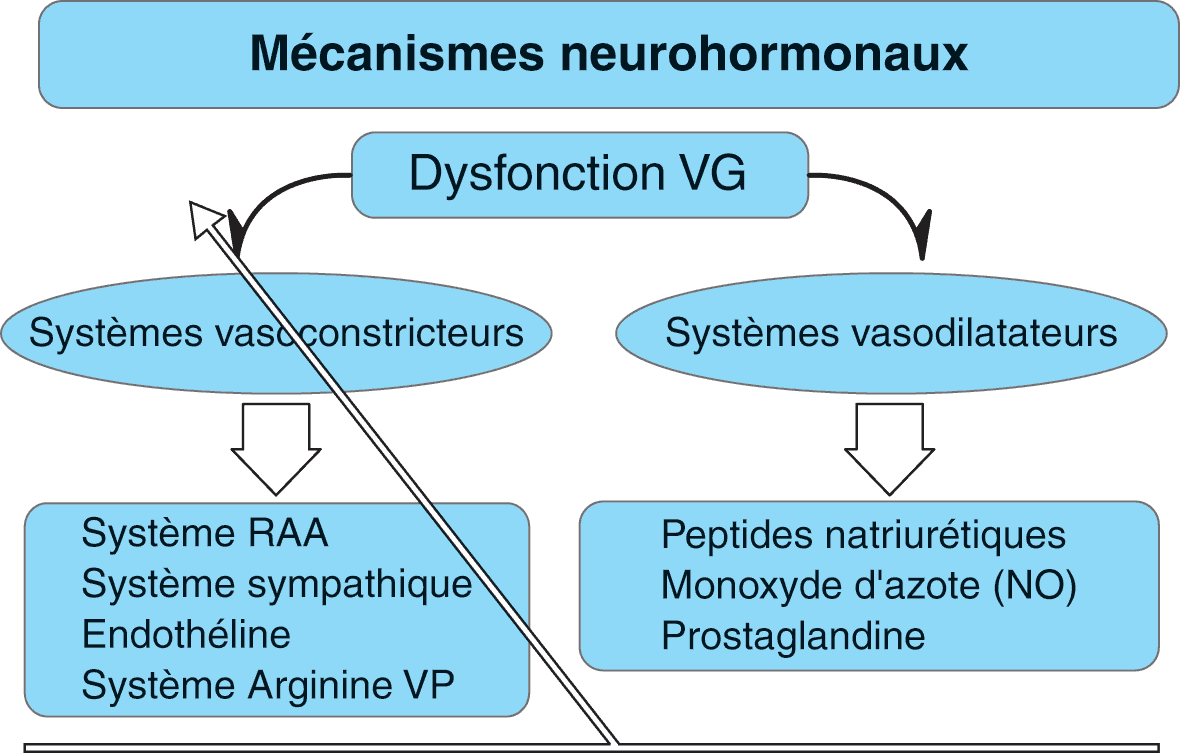
L’activation chronique des systèmes vasoconstricteurs domine les mécanismes d’adaptation neurohormonaux et est à long terme délétère.
________________________________________________________________________________
Sémiologie de l’insuffisance cardiaque
Dans cette section sont abordés les signes fonctionnels, les signes généraux et les signes physiques de l’insuffisance cardiaque gauche, de l’insuffisance cardiaque droite et de l’insuffisance cardiaque globale.
Insuffisance cardiaque gauche
Signes fonctionnels de l’insuffisance cardiaque gauche
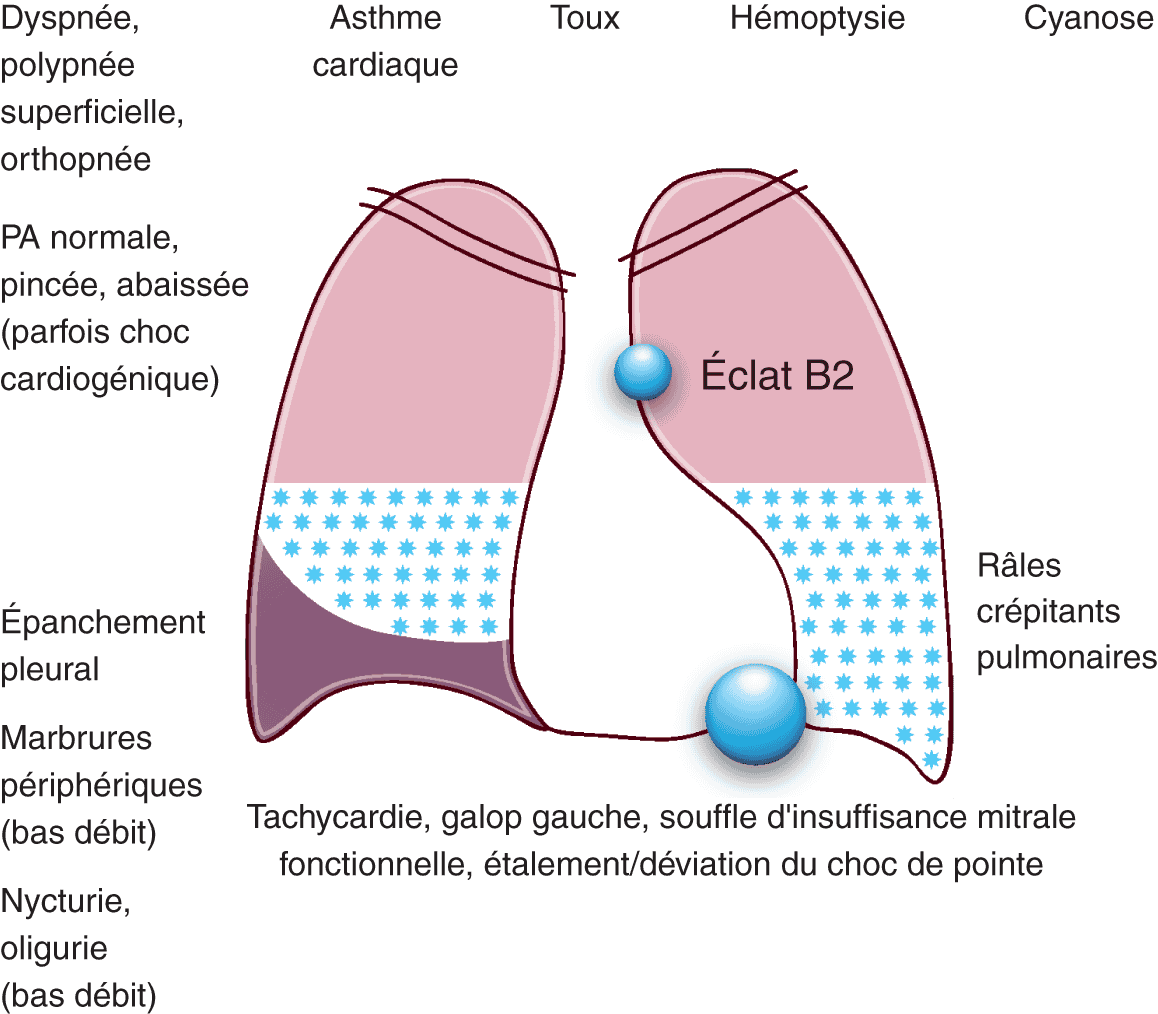
Les signes fonctionnels de l’insuffisance cardiaque gauche sont (fig. 5.8) :
- la dyspnée d’effort ;
- l’orthopnée (OAP, sub-œdème pulmonaire, asthme cardiaque) ;
- la toux ;
- les hémoptysies.
________________________________________________________________________________
Figure 5.8. Conséquences respiratoires de l’insuffisance cardiaque gauche.
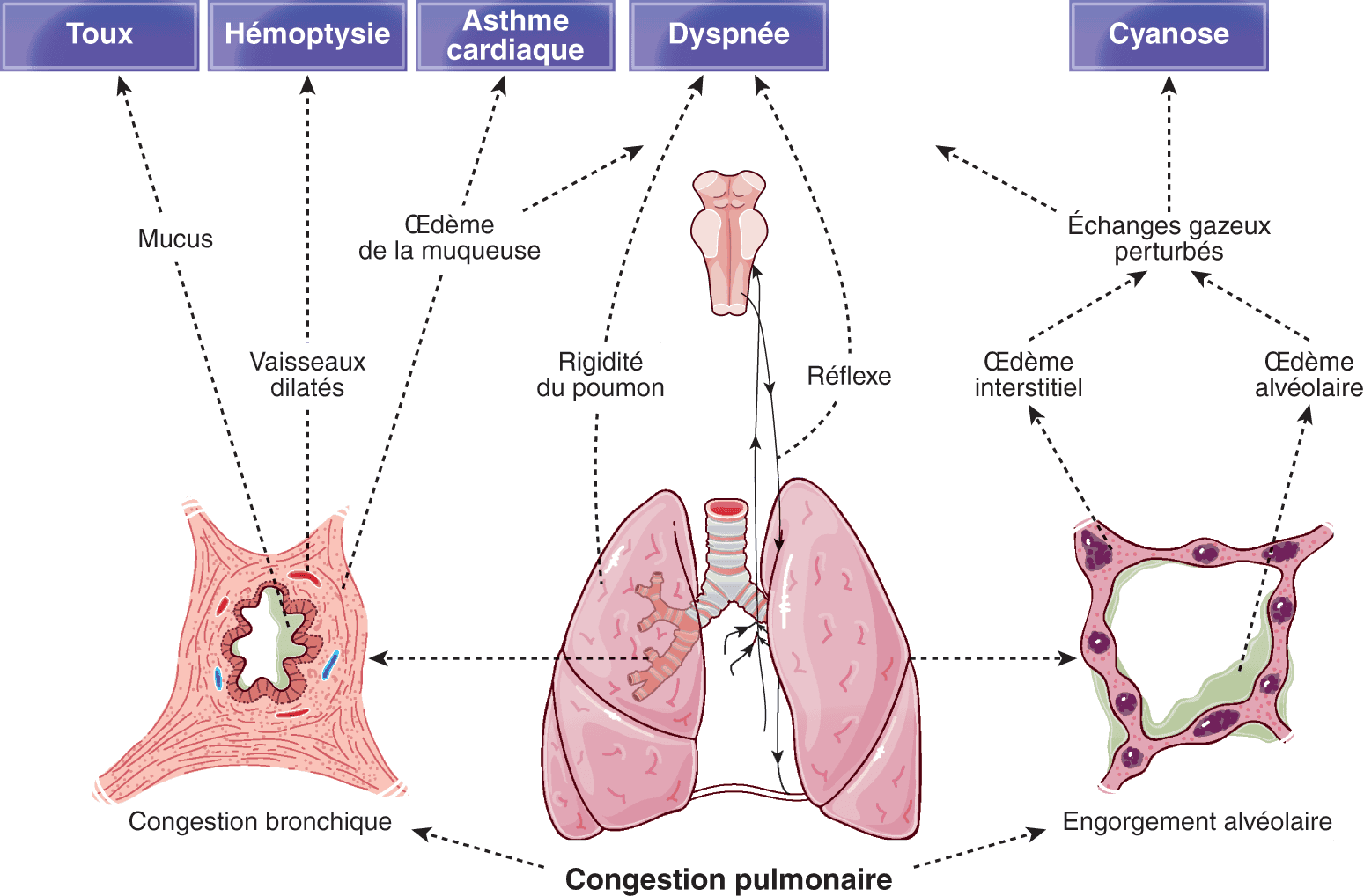
Source : d’après Rushmer RF. Structure and function of the cardiovascular system. Saunders ; 1972.
________________________________________________________________________________
Dyspnée de l’insuffisance cardiaque gauche
En l’absence d’affection pulmonaire, d’embolie pulmonaire récente, d’obésité, d’anémie sévère, de déformation thoracique (cyphose, scoliose, cypho-scoliose), la dyspnée est le signe le plus précoce de l’insuffisance cardiaque gauche.
Plus rarement, on évoquera une désadaptation cardiovasculaire à l’exercice par déconditionnement chez un sujet sédentaire ou une dyspnée psychogène (syndrome d’hyperventilation) caractérisée par de grands mouvements respiratoires. Ce phénomène de soupir, qui donne l’impression de libérer la respiration et inquiète souvent les sujets et parfois certains médecins, est physiologique mais n’a pas de caractère de gravité. Une dyspnée présente au repos mais qui ne s’accentue pas à l’effort n’est vraisemblablement pas d’origine organique.
La dyspnée du patient insuffisant cardiaque est principalement liée à la congestion pulmonaire et à la réduction du débit cardiaque. La congestion pulmonaire est secondaire à l’augmentation des pressions intraventriculaires et atriale gauches, altérant compliance et travail pulmonaire – phénomène qui s’accentue lors du passage en décubitus qui favorise le retour veineux. La baisse du débit cardiaque touche l’ensemble de la musculature périphérique et particulièrement diaphragme et muscles respiratoires, à l’origine d’une acidose d’effort à l’origine d’une hyperventilation et d’une dyspnée, aggravées par le déconditionnement à l’effort chez les patients en insuffisance cardiaque chronique.
Dyspnée d’effort
La dyspnée correspond à la prise de conscience par le patient d’une respiration difficile, exigeant un effort supplémentaire, avec une sensation de soif d’air. La dyspnée survient quand le patient prend conscience d’un décalage entre l’effort fourni pour respirer et le confort respiratoire obtenu.
Classiquement, la dyspnée de l’insuffisance cardiaque est une polypnée superficielle progressivement croissante – elle survient pour des efforts de moins en moins marqués avec l’évolution de la maladie – ou peut survenir de façon aiguë, d’emblée inaugurale de la maladie.
La dyspnée doit être quantifiée afin d’évaluer le retentissement fonctionnel de l’insuffisance cardiaque. Pour cela, il faut utiliser la classification de la New York Heart Association (NYHA, cf. encadré ci-après). La classification NYHA en quatre classes est importante car elle permet :
- une évaluation de la sévérité de l’insuffisance cardiaque fondée sur la gêne fonctionnelle qu’elle entraîne, en particulier sur les activités de la vie quotidienne ;
- de regrouper les patients en classes homogènes ;
- d’indiquer en fonction du stade fonctionnel les traitements recommandés par les sociétés savantes.
________________________________________________________________________________
En pratique – Savoir interroger un patient
Le temps de l’interrogatoire est essentiel car les patients ne précisent pas en général les conditions de survenue de la dyspnée. Il précise les efforts que le patient peut réaliser sans être essoufflé, les efforts ou les activités qu’il a dû limiter ou arrêter en raison des symptômes. L’analyse séméiologique doit prendre en compte l’état général du patient, son âge, son activité professionnelle pour orienter les questions et analyser ses réponses, mais la dyspnée reste un symptôme subjectif.
Dyspnée d’effort
Avez-vous parfois des difficultés à respirer ? Vous sentez-vous parfois essoufflé ? Cela vous arrive-t-il à l’effort ? Pour quel type d’effort ? Quel effort maximal pouvez-vous réaliser sans être essoufflé ? Quelle distance pouvez-vous effectuer en marchant sans être essoufflé ? L’essoufflement survient-il à la marche en côte ? À partir de quel étage faites-vous une pause lors de la montée des escaliers ? Ressentez-vous une gêne respiratoire en portant des charges modérées (sacs de courses, packs d’eau minérale, etc.) ? Ressentez-vous un essoufflement ou une fatigue lors des activités quotidiennes minimes (ménage, vaisselle, toilette, douche, habillage, discussions, répondre au téléphone, etc.) ?
Dyspnée de repos (orthopnée)
Vous arrive-t-il de vous réveiller essoufflé ? Êtes-vous obligé de vous asseoir ou de vous lever pour mieux respirer ? Dormez-vous en position assise ou semi-assise ? Combien d’oreillers utilisez-vous pour dormir ?
Classification de la NYHA
- Classe I : Dyspnée pour les efforts importants inhabituels : le patient n’a aucune gêne dans la vie courante.
- Classe II : Limitation modérée de la vie courante. Dyspnée pour les efforts modérés : marche rapide ou en côte, montée de plus de deux étages.
- Classe III : Dyspnée pour les efforts peu intenses de la vie courante : marche normale en terrain plat, montée de moins de deux étages.
- Classe IV : Dyspnée permanente de repos : impossibilité de mener des activités sans gêne, confinant le patient chez lui ou dans sa chambre.
________________________________________________________________________________
Orthopnée
Quand la dyspnée de repos apparaît, toute activité devient extrêmement pénible à réaliser et s’accompagne d’une fatigue intense. La dyspnée de repos se manifeste sous la forme d’une orthopnée : c’est une dyspnée qui oblige le patient à respirer en position assise. Les épisodes d’orthopnée peuvent survenir classiquement en milieu ou fin de nuit, plus rarement d’emblée (primo-décubitus) et obligent le patient à dormir en position assise ou semi-assise en relevant la tête du lit ou en empilant des oreillers, et parfois à s’asseoir au bord du lit pour reprendre son souffle.
L’orthopnée témoigne le plus probablement de l’origine cardiaque de la dyspnée, avec comme réserve qu’elle peut aussi se retrouver chez les patients ayant une bronchopneumopathie obstructive (BPCO) très évoluée avec emphysème, qui oblige ces patients à mettre en jeu les muscles respiratoires accessoires, ce qui est plus facile en position assise. Le contexte clinique et les antécédents permettent le plus souvent d’orienter le diagnostic (tableau 5.1).
Tableau 5.1. Orientations diagnostiques devant une dyspnée.
| OAP | Embolie pulmonaire | BPCO | Asthme | Pneumopathie | Pleurésie | Pneumothorax | |
| Dyspnée | Paroxystique
Souvent nocturne Orthopnée Brutale |
Polypnée
Brutale Douleur basithoracique |
Toux
Expectoration |
Bradypnée expiratoire | Parfois brutale
Accompagnée d’une douleur thoracique |
Souvent plus progressive
± Douleur thoracique (plus forte inspiration) |
Aiguë
Douleur thoracique (plus forte inspiration) |
| Antécédents, contexte | Maladie cardiovasculaire
Facteurs de risque cardiovasculaire |
Thrombose veineuse profonde Immobilisation postopératoire, du post-partum | Sujet tabagique ou exposé à des allergènes | Sujet jeune
Antécédents allergiques |
Syndrome infectieux fébrile | Fébrile | Sujet longiligne
Jeune |
| Examen physique | Expectoration mousseuse
Râles crépitants fins |
Recherche des signes d’insuffisance cardiaque droite
Souvent normal |
Râles sibilants à l’auscultation | Râles sibilants à l’auscultation
Baisse du peak-flow |
Râles crépitants unilatéraux (foyer) | Abolition du murmure vésiculaire unilatéral
Matité déclive |
Silence auscultatoire d’un hémichamp pulmonaire
Tympanisme |
| Radio de thorax | Cardiomégalie
Surcharge alvéolaire bilatérale |
Normale
Hypoventilation Surélévation d’une coupole |
Distension thoracique | Distension thoracique | Syndrome de condensation parenchymateuse pulmonaire | Épanchement (voir plus loin)
Ligne de Damoiseau |
Hyperclarté périphérique
Poumon rétracté sur le hile |
| ECG | Anormal : anomalie de le repolarisation, de la conduction, du rythme | Signes de cœur pulmonaire aigu : tachycardie, bloc de branche droit, ischémie sous-épicardique antérieure (V1–V3), S1Q3 | Normal
Ou signes de cœur pulmonaire aigu rares |
Normal
Ou signes de cœur pulmonaire aigu rares |
Normal
Ou signes de cœur pulmonaire aigu rares |
Normal
Ou signes de cœur pulmonaire aigu rares |
Normal
Ou signes de cœur pulmonaire aigu rares |
| Gazométrie artérielle | Effet shunt⁎ | Effet shunt | Hypoxémie, hypercapnie | Effet shunt | Effet shunt | Effet shunt | Effet shunt |
| Biologie | Troponine, BNP élevés | Troponine parfois un peu élevée
BNP élevé (si CPA⁎) |
BNP normal | BNP normal | BNP normal | BNP normal | BNP normal |
| ETT | Élévation des pressions de remplissage ventriculaire gauche
Anomalie de la cinétique, FEVG |
Recherche de signes de cœur pulmonaire aigu, HTAP | Recherche de signes de cœur pulmonaire aigu, HTAP | ||||
| ETO | Bilan étiologique (valvulopathie) | Non indiquée | Non indiquée | Non indiquée | Non indiquée | Non indiquée | Non indiquée |
| Angio-scanner pulmonaire | Non indiqué | Peut permettre le diagnostic positif | Permet de rechercher une étiologie | Permet de rechercher une étiologie | Permet de rechercher une étiologie | Permet de rechercher une étiologie | Permet de rechercher une étiologie |
| Coronaro-graphie | Recherche et traite une sténose coronaire responsable d’une ischémie | Non indiquée | Non indiquée | Non indiquée | Non indiquée | Non indiquée | Non indiquée |
CPA : cœur pulmonaire aigu.
⁎ Effet shunt : hypoxémie avec hypocapnie et alcalose ventilatoire à la gazométrie artérielle.
Dyspnée paroxystique nocturne
Ces épisodes sont attribués à un œdème pulmonaire lié à la résorption progressive des fluides intestinaux au cours de la nuit et à la dépression nocturne de la fonction respiratoire.
L’évolution peut être marquée par des accidents paroxystiques, qui peuvent être aussi inauguraux. Il s’agit de :
- l’œdème aigu pulmonaire (OAP) ;
- le sub-œdème pulmonaire qui est un accident de moindre intensité que l’OAP et qui régresse spontanément, mais qui a la même valeur sémiologique ;
- le (pseudo-)asthme cardiaque.
Œdème aigu pulmonaire
La présentation la plus sévère est l’OAP. C’est une urgence qui nécessite un traitement symptomatique fondé sur l’utilisation d’oxygène au masque, de diurétiques intraveineux et de vasodilatateurs, et qui requiert une hospitalisation. Le traitement de la cause (syndrome coronaire aigu, poussée hypertensive, décompensation cardiaque d’une insuffisance cardiaque déjà connue, maladie valvulaire, trouble du rythme cardiaque, etc.) est entrepris en parallèle.
L’OAP correspond à une inondation alvéolaire diffuse par un transsudat, secondaire à l’élévation de la pression capillaire pulmonaire au-dessus de 25 mmHg.
L’OAP se manifeste comme une détresse respiratoire de survenue brutale en pleine nuit, plus rarement à l’effort. Classiquement, le patient est retrouvé assis au bord du lit, jambes pendantes, couvert de sueurs, avec une tachypnée superficielle, très angoissante. Il est parfois agité et on observe un tirage sus-claviculaire et intercostal. Le patient décrit une sensation de « chape de plomb » sur les épaules. Souvent les symptômes ont débuté par la sensation d’un grésillement laryngé, associé à une toux ramenant une expectoration mousseuse, blanchâtre ou parfois « saumonée » car elle peut être teintée de sang. L’auscultation pulmonaire retrouve des râles crépitants bilatéraux remontant des bases vers les sommets au fur et à mesure que s’aggrave l’inondation alvéolaire. En l’absence de traitement, on observe une véritable « marée montante » des râles crépitants dans les deux champs pulmonaires.
La pression artérielle peut être élevée, normale ou abaissée. Quand elle est élevée, elle peut être cause ou conséquence de l’œdème pulmonaire.
Deux signes de gravité doivent être systématiquement recherchés :
- l’apparition d’une cyanose qui, associée à une expectoration mousseuse abondante et continue, évoque un œdème pulmonaire asphyxique ;
- une hypotension artérielle avec ou sans signes périphériques de choc.
L’examen et l’interrogatoire recherchent en parallèle la cause ou un facteur déclenchant qui eux-mêmes nécessiteront un traitement spécifique urgent (voir le paragraphe sur l’insuffisance cardiaque aiguë).
Les épisodes de sub-œdème pulmonaire sont plus fréquents que les formes aiguës ou suraiguës :
- ils surviennent chez un patient qui a une dyspnée d’effort ou de repos au stade III ou IV de la NYHA et se présentent comme une aggravation progressive de la gêne respiratoire qui évolue vers l’orthopnée, spontanément résolutive ;
- il peut aussi s’agir de poussées répétées de dyspnée nocturne aboutissant à des crachats, parfois hémoptoïques spontanément résolutifs. L’auscultation retrouve alors des râles crépitants et sous-crépitants aux deux bases parfois jusqu’à mi-champs pulmonaires, mais la présentation clinique est moins alarmante que celle de l’OAP.
Les épisodes de sub-œdème pulmonaire ont la même valeur sémiologique que l’OAP. Ils peuvent en effet évoluer vers une de détresse respiratoire et/ou l’apparition d’un collapsus. Il s’agit donc aussi d’urgences.
Asthme cardiaque
La congestion pulmonaire peut prendre l’aspect d’une « pseudo-crise d’asthme » : on observe lors de l’épisode d’œdème pulmonaire un freinage expiratoire, une toux peu productive et la présence à l’auscultation pulmonaire de râles sous-crépitants et sibilants (sifflements). L’origine cardiaque est d’autant plus difficile à affirmer qu’elle survient le plus souvent chez un sujet ayant un passé de bronchopneumopathie chronique obstructive (BPCO) voire d’asthme authentique. Cette présentation est souvent retrouvée chez le sujet âgé. Le risque évolutif de l’asthme cardiaque est identique à celui des autres présentations d’œdème pulmonaire. Cette présentation est expliquée par une stase veineuse interstitielle et péri-bronchiolaire qui provoque le spasme bronchique.
Bendopnée
Ce symptôme traduit une augmentation des pressions de remplissage cardiaque. Il s’agit d’une dyspnée en antéflexion, classiquement lorsque le patient met ses chaussures ou doit ramasser un objet à terre. Il peut, toutefois, être observé chez le patient obèse ou âgé sans insuffisance cardiaque.
Toux
La toux est un équivalent mineur du sub-œdème pulmonaire lorsqu’elle survient à l’effort ou la nuit. C’est un signe à rechercher systématiquement à l’interrogatoire.
Hémoptysies
Les hémoptysies peuvent être présentes sous forme d’expectoration saumonée lors de l’OAP, plus rarement sanglantes. Il peut aussi s’agir d’hémoptysies isolées sans crise de suffocation dans l’insuffisance cardiaque chronique (œdème péribronchique).
________________________________________________________________________________
Syndrome d’apnées du sommeil (SAS)
Les troubles respiratoires lors du sommeil sont fréquents au cours de l’insuffisance cardiaque : ils contribuent à l’altération de la fonction cardiaque et augmentent la morbimortalité. Le syndrome d’apnées du sommeil (SAS) est fréquent au cours de l’insuffisance cardiaque et, s’il n’est pas traité, va participer à l’aggravation de la maladie. Il doit être systématiquement évoqué. La présence de ronflements nocturnes ou de pauses respiratoires décrits par le conjoint et d’une somnolence diurne (rare chez l’insuffisant cardiaque) doit faire évoquer le diagnostic. L’apnée est définie par l’absence de flux inspiratoire pendant au moins 10 secondes. Elle peut être centrale (pas d’activation des muscles respiratoires dont le diaphragme), obstructive (muscles respiratoires actifs mais obstruction des voies aériennes supérieures) ou mixte (composante initiale centrale puis obstructive). L’apnée du sommeil entraîne trois conséquences : des anomalies des échanges gazeux, des micro-éveils, des variations importantes des pressions intrathoraciques qui engendrent une activation adrénergique excessive. L’apnée du sommeil est diagnostiquée par un enregistrement polysomnographique ou une polygraphie ambulatoire. Son traitement repose sur des mesures hygiénodiététiques (perte de poids, arrêt de l’alcool et des benzodiazépines) et une ventilation non invasive à pression positive au masque. Des prothèses d’avancée mandibulaire peuvent être également proposées. Une étude récente a démontré une surmortalité cardiovasculaire de la ventilation servo-assistée en cas d’apnée centrale et/ou dyspnée de Cheyne-Stokes chez le patient insuffisant cardiaque avec une fonction systolique altérée et ce traitement est donc contre-indiqué.
________________________________________________________________________________
Dyspnée de Cheyne-Stokes
L’insuffisance cardiaque gauche peut être associée à une dyspnée de Cheyne-Stokes, qui se traduit par une alternance régulière de période d’apnée (pendant laquelle le patient ne respire plus) et d’hyperpnée (période de respiration à amplitude croissante et exagérée). Elle s’améliore avec le traitement de l’insuffisance cardiaque. Elle est surtout observée en cas d’insuffisance cardiaque congestive, mais aussi en cas d’atteintes du système nerveux central, d’intoxication à l’oxyde de carbone ou d’intoxication médicamenteuse. Son mécanisme n’est pas bien connu ; y participent l’hyperventilation secondaire à la congestion pulmonaire et l’altération de la perfusion cérébrale.
________________________________________________________________________________
Signes physiques de l’insuffisance cardiaque gauche (fig. 5.9)
Tachycardie
La tachycardie sinusale est fréquente à la phase initiale ou lors d’une poussée aiguë. C’est un signe sensible mais non spécifique, car de nombreuses situations cliniques peuvent être associées à une tachycardie. La tachycardie est un mécanisme d’adaptation initial qui permet d’augmenter le débit cardiaque (Qc = VES × Fc), mais qui, au long cours, s’avère délétère.
________________________________________________________________________________
Figure 5.9. Schéma illustrant les principaux signes de l’insuffisance cardiaque gauche.
________________________________________________________________________________
Une fréquence cardiaque élevée régulière ou irrégulière peut aussi être due à un trouble du rythme supraventriculaire ou ventriculaire.
Bruit de galop
Le bruit de galop gauche est entendu lors de l’auscultation cardiaque, à la pointe :
- c’est un bruit sourd, surajouté, diastolique qui, en association avec le B1 et le B2, donne un rythme à trois temps, imitant celui du galop du cheval ;
- il signe l’insuffisance ventriculaire gauche ;
- il peut être protodiastolique (correspondant au remplissage ventriculaire rapide), télédiastolique (correspondant à la contraction atriale et disparaissant en cas de fibrillation atriale) ou mésodiastolique (galop de sommation correspondant à la sommation des deux bruits précédents en cas de tachycardie).
Le galop peut être aussi perçu à la palpation comme un double choc à la pointe du cœur lors de la palpation.
________________________________________________________________________________
Pour comprendre – Le bruit de galop (voir aussi chapitre 4, Sémiologie, et figure 4.9)
Le bruit de galop est un bruit diastolique surajouté entendu en cas d’insuffisance cardiaque et qui témoigne de l’élévation des pressions de remplissage ventriculaire. Dans ce cas, pendant la diastole, le passage du sang entraîne une mise en tension des parois ventriculaires qui génère un bruit sourd.
Pour comprendre les différents types de galop, il faut connaître les différents temps du remplissage ventriculaire (voir chapitre 1, Physiologie, Cœur). Pour cela, l’analyse Doppler du flux mitral (ou flux de remplissage ventriculaire gauche) mesuré à l’écho-Doppler cardiaque est particulièrement utile (fig. 5.10). Cette analyse permet de mesurer les vitesses d’écoulement du sang de l’atrium (en pratique la vitesse de déplacement des hématies) vers le ventricule gauche au niveau d’une zone d’échantillonnage placée au sommet des feuillets mitraux. La figure montre les trois temps du remplissage ventriculaire :
- le premier temps correspond au début de la diastole (appelé remplissage ventriculaire rapide), qui est essentiellement déterminée par la différence de pression entre atrium gauche et ventricule gauche, associé à un phénomène d’aspiration par le ventricule, qui se traduit en Doppler par une onde positive (le flux se dirige vers le capteur) ;
- puis les pressions entre les deux cavités s’équilibrent, le phénomène de succion du ventricule s’atténue : c’est la période de diastasis ;
- puis intervient la contraction de l’atrium, qui provoque une chasse sanguine en fin de diastole (télédiastole) vers le ventricule.
Les différents bruits de galop sont synchrones de ces différents flux :
- le galop protodiastolique (B3), indépendant de la contraction de l’atrium, est lié au remplissage rapide ; il est toujours présent en fibrillation atriale ;
- le galop télédiastolique (B4) n’est présent qu’en rythme sinusal car il est généré par la chasse sanguine dépendante de la contraction de l’atrium ;
- le galop de sommation correspond à la fusion des temps proto- et télédiastoliques et n’est retrouvé qu’en rythme sinusal.
________________________________________________________________________________
Figure 5.10. Tracé Doppler mitral.
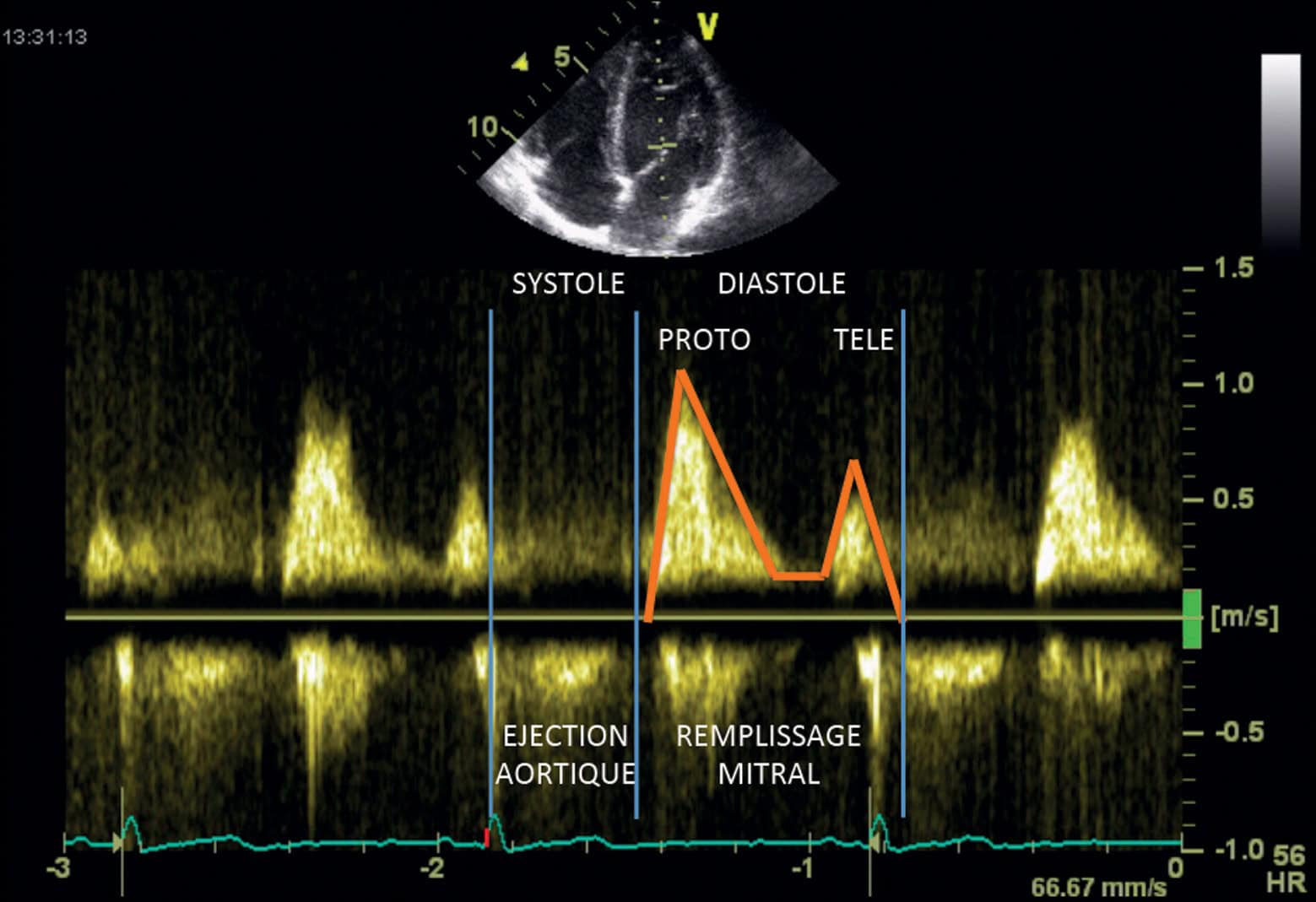
L’enregistrement du flux transmitral en Doppler pulsé renseigne sur la part respective du remplissage rapide (PROTO) et de la contraction atriale (TELE), ainsi que sur la qualité de la relaxation VG.
Déplacement et étalement du choc de pointe
L’étalement du choc de pointe traduit la dilation ventriculaire gauche ; il est souvent déplacé en bas à gauche.
Souffle valvulaire cardiaque (voir chapitre 4)
L’auscultation cardiaque peut parfois retrouver un souffle d’insuffisance mitrale dite fonctionnelle – car non liée à une atteinte organique de la valve mitrale – dans le cas de cardiopathies dilatées.
La présence d’un souffle valvulaire cardiaque peut aussi être due à une valvulopathie responsable de l’insuffisance cardiaque : rétrécissement aortique, insuffisance aortique, rétrécissement mitral, insuffisance mitrale organique (ou fonctionnelle, conséquence du remodelage cardiaque).
Éclat du deuxième bruit au foyer pulmonaire
Avec l’aggravation de l’insuffisance cardiaque, la pression artérielle pulmonaire augmente et l’intensité de B2 augmente. L’éclat du deuxième bruit traduit donc la présence d’une hypertension pulmonaire dite post-capillaire car sa genèse est liée à un mécanisme ayant pris place en aval des capillaires pulmonaires. L’intensité du deuxième bruit peut diminuer avec la baisse des pressions pulmonaires.
Râles crépitants pulmonaires
L’auscultation pulmonaire peut retrouver la présence de râles crépitants pulmonaires fins, secs, inspiratoires et bilatéraux en cas d’insuffisance cardiaque aiguë (cf. supra).
Épanchement pleural
Les veines pleurales se drainent à la fois dans le réseau veineux pulmonaire et le réseau veineux systémique : un hydrothorax (transsudat) peut donc être retrouvé en cas d’hypertension veineuse de l’un ou l’autre système, qui se complique d’un épanchement interstitiel (fig. 5.11). Dans l’insuffisance cardiaque gauche, l’épanchement pleural est la conséquence de l’hypertension veineuse pulmonaire. L’augmentation de la perméabilité capillaire participe également à la physiopathologie de l’épanchement.
________________________________________________________________________________
Figure 5.11. Physiopathologie de l’œdème pulmonaire interstitiel et alvéolaire.
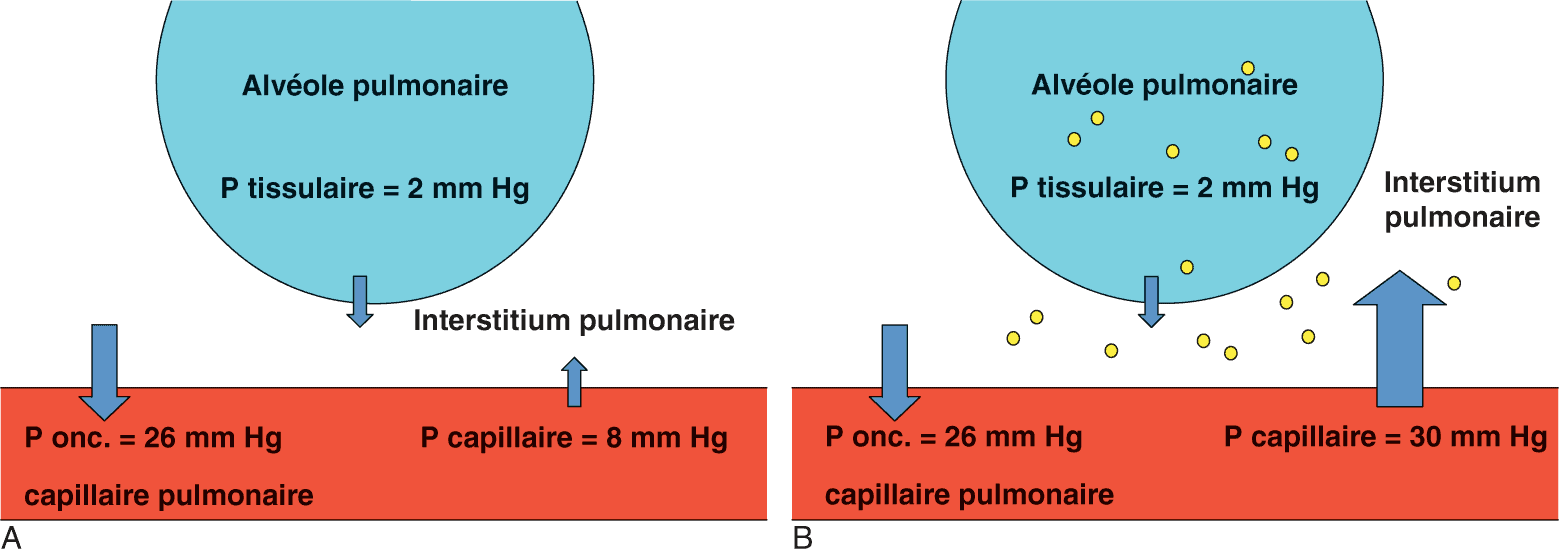
A. Situation physiologique. B. Œdème pulmonaire, insuffisance cardiaque gauche.
Source : d’après Maurice P, Fernandez F, Ourbak P. Cardiologie. Physiopathologie clinique. 2e édition. Paris : J-B Baillière ; 1979.
________________________________________________________________________________
La présence d’un épanchement bilatéral est fréquente, ou alors droit isolé, mais plus rarement gauche.
Il se traduit à l’examen clinique par la triade :
- diminution du murmure vésiculaire ;
- diminution des vibrations vocales ;
- matité à la percussion.
Il est objectivé à la radiographie thoracique (cf. infra). L’épanchement pleural participe à l’accroissement de la dyspnée en réduisant la capacité vitale. Il régresse avec le traitement de l’insuffisance cardiaque. Il doit parfois être ponctionné pour améliorer le patient plus rapidement. L’analyse biochimique permet alors de différencier un transsudat (concentration protéique < 30 g/L) d’un exsudat, faisant alors rechercher une pathologie associée (ainsi qu’en cas de doute étiologique).
Pression artérielle
En fonction de la cause de l’insuffisance cardiaque, la pression artérielle peut être normale, élevée, pincée, abaissée – le plus souvent abaissée. Les traitements de l’insuffisance cardiaque participent à la diminution de la pression artérielle. La pression artérielle est effondrée en cas de choc cardiogénique.
Cyanose
La cyanose correspond à une coloration bleu violacée des téguments. Elle traduit un bas débit et un défaut d’oxygénation du sang (hypoxémie). La cyanose est bien visible au niveau des ongles, des muqueuses, des lèvres. Dans le cas de l’insuffisance cardiaque, elle est tardive et se voit essentiellement lors d’un œdème aigu pulmonaire.
Nycturie
C’est un signe précoce de l’insuffisance cardiaque gauche. On observe une diminution de la quantité d’urine émise dans la journée et une diurèse plus importante la nuit. La nuit, la redistribution en position allongée vers le thorax des fluides interstitiels accumulés pendant la journée, le déficit moindre du débit cardiaque au regard des activités et la diminution de la vasoconstriction rénale favorisent l’émission d’urines.
Oligurie
L’oligurie est une diminution importante de la quantité totale d’urine émise par les reins en raison d’une baisse marquée du débit sanguin rénal, conséquence de la baisse du débit cardiaque. C’est un signe tardif.
Marbrures
Les marbrures périphériques (particulièrement visibles au niveau des genoux) témoignent de la baisse du débit sanguin périphérique en cas d’insuffisance cardiaque avancée. Elles sont associées à un refroidissement de la température des téguments (genoux) appréciée par le dos de la main.
Choc cardiogénique
Il correspond à une défaillance aiguë et sévère de la fonction cardiaque entraînant une altération profonde de la perfusion périphérique et une anoxie tissulaire. Cliniquement, il associe les signes suivants :
- pression artérielle systolique < 90 mmHg ou chute de la pression artérielle systolique de 30 mmHg par rapport à la valeur de base pendant au moins 30 minutes ;
- troubles de la perfusion périphérique (extrémités froides, cyanosées et marbrées) ;
- oligurie < 20 ml/h ;
- altération de la conscience (agitation, somnolence, confusion mentale) ;
- sueurs profuses.
Des signes d’insuffisance cardiaque gauche ou globale y sont le plus souvent associés.
Signes généraux de l’insuffisance cardiaque gauche
Asthénie
L’asthénie est un signe très fréquent en cas d’insuffisance cardiaque chronique mais il est peu spécifique. La fatigue et la faiblesse musculaire touchent particulièrement les membres inférieurs. Associées au déconditionnement musculaire et à la dyspnée, elles conduisent le patient à limiter ses activités et sont donc responsables d’une dégradation majeure de la qualité de vie des patients.
Anorexie et dénutrition
Anorexie et dénutrition sont des conséquences fréquentes de l’insuffisance cardiaque aux stades avancés.
Signes radiologiques pleuropulmonaires de l’insuffisance cardiaque gauche
La radiographie thoracique montre le plus souvent l’existence d’une cardiomégalie définie par un rapport cardiothoracique > 0,5. L’absence de cardiomégalie ne remet, cependant, pas en cause le diagnostic d’insuffisance cardiaque.
Les signes pleuropulmonaires doivent être systématiquement recherchés lorsqu’on examine une radiographie thoracique chez un patient qui se plaint d’une dyspnée. Ils sont corrélés à l’élévation des pressions dans le lit vasculaire pulmonaire veineux, capillaire, artériel et à l’extravasation de sérum dans le secteur interstitiel puis alvéolaire.
On distingue classiquement trois stades (fig. 5.12).
________________________________________________________________________________
Figure 5.12. Signes radiologiques pleuropulmonaires de l’insuffisance cardiaque gauche.
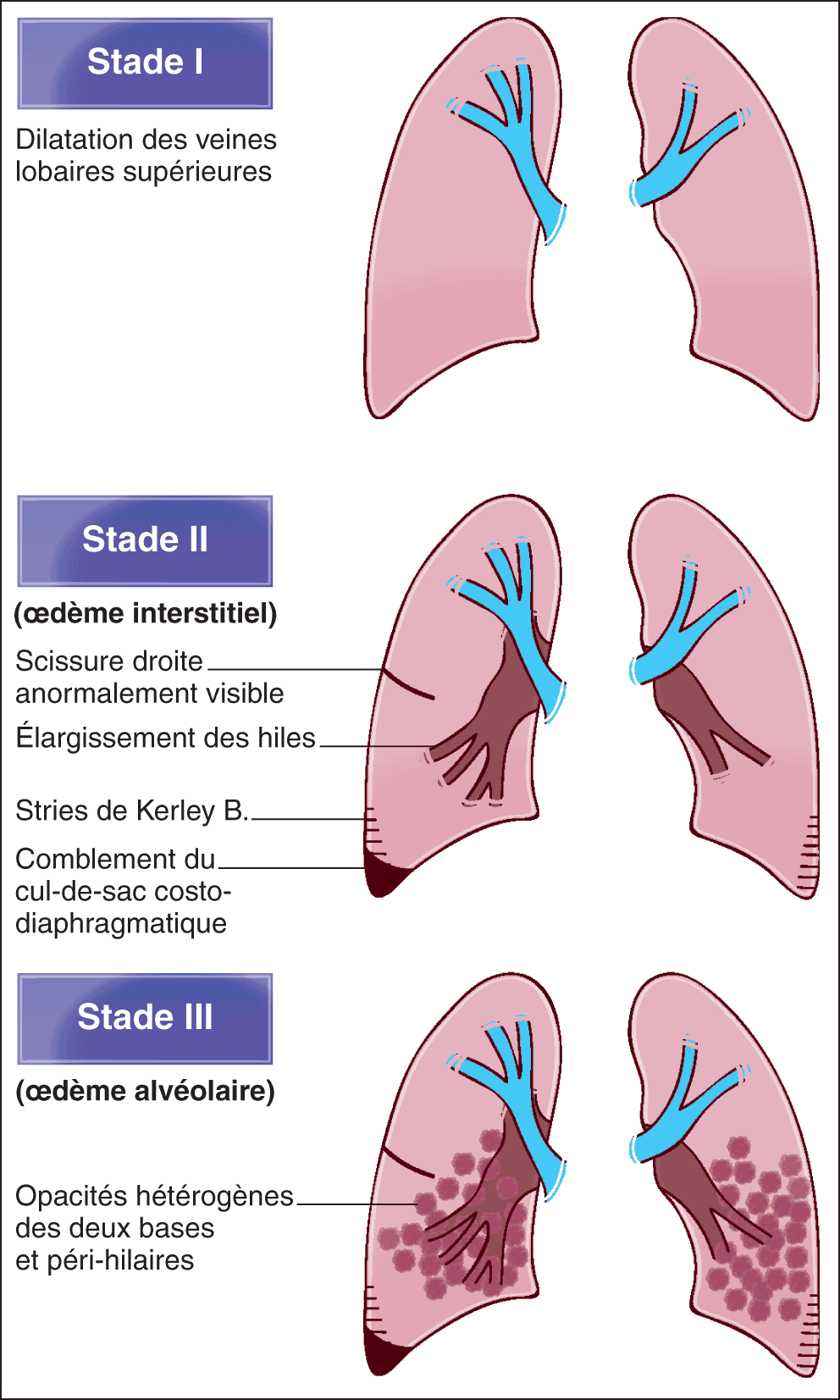
Source : d’après André-Fouët X (éd.) et le Collège des enseignants de cardiologie. Cardiologie. Lyon : université Claude-Bernard, Presses universitaires de Lyon ; 1999.
________________________________________________________________________________
Stade I
Le stade I correspond une redistribution vasculaire vers les sommets, qui deviennent aussi denses que les bases.
Stade II
Le stade II correspond à l’œdème interstitiel, avec plusieurs aspects :
- les stries de Kerley de type B correspondent à un œdème des cloisons septales et se présentent sous forme de petites lignes horizontales fines et courtes siégeant à la base des champs pulmonaire ;
- l’œdème péribronchique est visible sur les coupes des bronches péri-hilaires ;
- l’œdème sous-pleural se traduit par l’apparition des scissures interlobaires (en particulier à droite) et la présence d’épanchements pleuraux. Les épanchements pleuraux sont dus à la présence de sérum dans la cavité pleurale : lorsqu’ils sont minimes, ils prennent la forme d’un comblement des culs-de-sac costodiaphragmatiques ; s’ils sont plus importants, le liquide s’accumule latéralement entre le poumon et la paroi thoracique et remonte vers l’aisselle : on parle de la courbe de Damoiseau, qui est concave vers le haut. Les épanchements pleuraux de l’insuffisance cardiaque gauche sont uni- ou bilatéraux ;
- on observe une diminution de la transparence pulmonaire de façon bilatérale.
Ces anomalies sont souvent contemporaines d’un élargissement des hiles pulmonaires, correspondant à une dilatation des artères pulmonaires en cas d’hypertension artérielle pulmonaire.
Stade III
Le stade III correspond la présence d’un œdème alvéolaire. À ce stade, il existe une transsudation de plasma dans les alvéoles pulmonaires qui se traduit par l’apparition d’opacités bilatérales nodulaires et confluentes, prédominant dans les régions péri-hilaires, en « ailes de papillon ».
ECG de l’insuffisance cardiaque gauche
L’ECG est rarement normal. On peut observer une tachycardie sinusale, parfois une arythmie atriale (fibrillation atriale, flutter atrial), des troubles du rythme ventriculaire, un axe de QRS dévié à gauche, une hypertrophie atriale gauche, une hypertrophie ventriculaire gauche et un bloc de branche gauche complet, la présence d’onde Q (séquelle d’infarctus) ou des signes d’ischémie myocardique (voir chapitre 6 Électrocardiogramme normal et anormal).
Insuffisance cardiaque droite
Signes fonctionnels de l’insuffisance cardiaque droite
Les signes fonctionnels de l’insuffisance cardiaque droite sont limités à l’hépatalgie et, en cas d’insuffisance cardiaque droite avancée, à des signes digestifs non spécifiques. La dyspnée ne fait pas partie des signes classiques de l’insuffisance cardiaque droite, sauf au stade d’insuffisance cardiaque terminale compliquée d’une baisse majeure du débit cardiaque, d’une acidose, et au stade d’anasarque où les épanchements (hydrothorax, ascite) entravent la respiration.
Hépatalgie
Ce signe est caractéristique mais est souvent négligé par le patient. L’hépatalgie est une sensation de douleur de l’hypochondre droit à l’effort, perçue parfois comme une tension sous-costale ou une pesanteur, un inconfort épigastrique. Elle est due à la congestion hépatique lors de l’effort en raison de l’incapacité du ventricule droit à augmenter suffisamment son débit pour écluser l’augmentation du retour veineux associée à l’effort. La distension de la capsule de Glisson, par augmentation du volume hépatique, est responsable de douleurs spontanées au repos ou à l’effort ou lors de la palpation du foie. Ce signe peut apparaître lors des poussées aiguës, au repos ou à l’effort, s’atténuer ou disparaître en cas d’insuffisance chronique où la congestion hépatique se développe progressivement. Elle cède à l’arrêt de l’effort.
Signes digestifs
Des signes digestifs non spécifiques, souvent tardifs, liés à la congestion du système digestif peuvent être décrits par le patient : nausées, ballonnements, impression de plénitude gastrique même après des repas légers, troubles du transit.
Signes physiques de l’insuffisance cardiaque droite (fig. 5.13)
Les signes physiques de l’insuffisance cardiaque droite sont :
- hépatomégalie, reflux hépatojugulaire ;
- turgescence jugulaire ;
- ictère ;
- œdèmes déclives ;
- galop droit (voir encadré Pour comprendre Le bruit de galop) ;
- souffle d’insuffisance tricuspide ;
- signe de Harzer ;
- ascite.
________________________________________________________________________________
Figure 5.13. Signes physiques de l’insuffisance cardiaque droite.
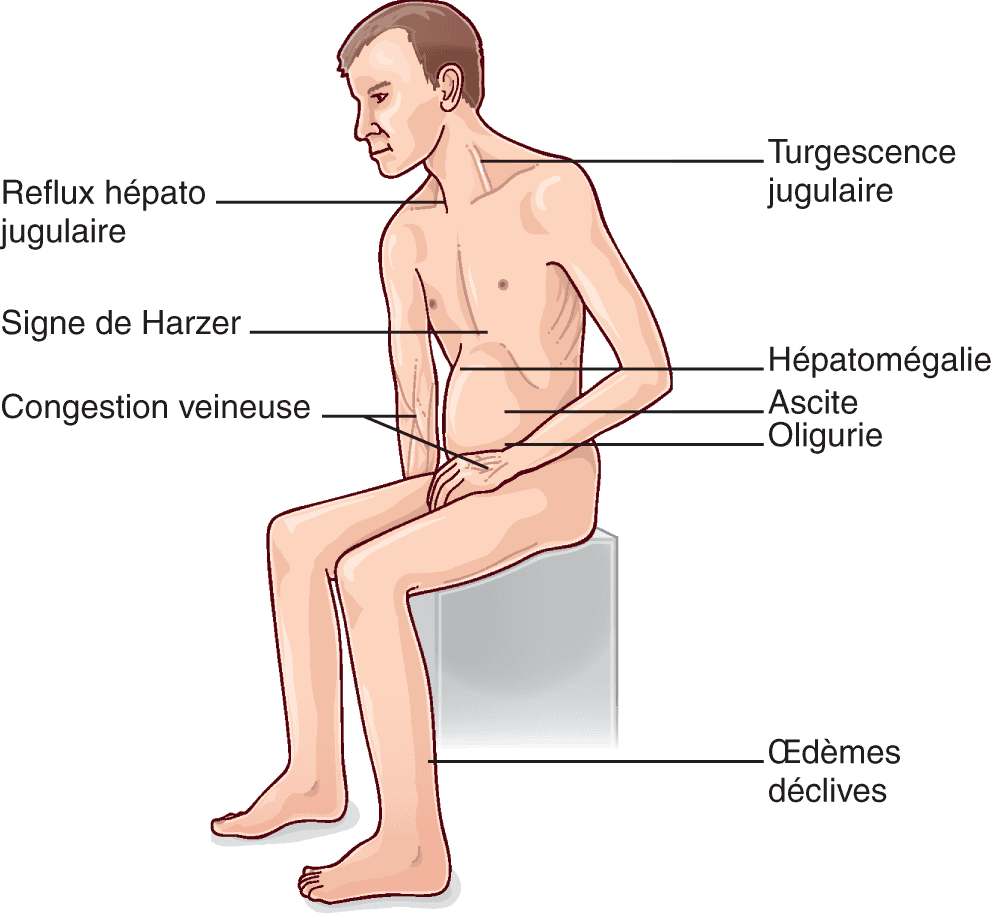
Source : d’ Rushmer RF. Structure and function of the cardiovascular system. Saunders ; 1972.
________________________________________________________________________________
Signes hépatiques de l’insuffisance cardiaque droite
L’insuffisance cardiaque droite se traduit par l’augmentation de la pression veineuse systémique et par une gêne au retour veineux dans les organes sous-diaphragmatiques situés en amont du cœur droit, une augmentation de pression des veines sus-hépatiques et des capillaires sinusoïdes, et donc une congestion passive du foie. L’hépatalgie en est la première manifestation clinique.
Hépatomégalie
Il s’agit d’une augmentation du volume du foie lié à la congestion sanguine, palpable sous le rebord costal : hauteur du foie aussi dénommée « flèche hépatique » > 12 cm sur la ligne médio-claviculaire (limite supérieure appréciée à la percussion du gril costal antérieur droit, limite inférieure à la palpation lors de l’inspiration).
Le patient doit respirer amplement bouche ouverte. Le médecin est à la droite du patient et palpe l’abdomen avec une ou deux mains, posée à plat et en exerçant une pression dosée pour ne pas entraîner une réaction de défense. La pulpe des doigts remonte progressivement vers le rebord costal et vient percevoir le rebord inférieur du foie lors de l’inspiration. La consistance du bord inférieur est appréciée lors de l’inspiration profonde : mousse, non tranchant et sans irrégularités ainsi que la face antérieure, lisse. La palpation peut être sensible ou douloureuse, alors qu’elle ne l’est pas dans la cirrhose. Le lobe gauche hypertrophique du foie congestif peut être parfois perçu vers le creux épigastrique.
La modification du volume du foie, liée à la baisse des pressions de remplissage du ventricule droit en réponse au traitement diurétique et vasodilatateur, est souvent observée à l’examen clinique par la diminution de l’hépatomégalie (appréciée par une diminution de la flèche hépatique, en particulier du débord sous-costal).
La palpation d’une expansion systolique du foie affirme la présence d’une insuffisance tricuspide importante par reflux sanguin systolique dans les veines sus-hépatiques.
Reflux hépatojugulaire persistant
Il se recherche chez un patient en décubitus dorsal, tête du lit inclinée à environ 45°. On demande au patient de regarder vers la gauche.
Normalement, la compression hépatique douce et prolongée chez le sujet normal entraîne une distension veineuse jugulaire transitoire qui disparaît en quelques secondes même si la pression manuelle est maintenue et en inspiration forcée.
En cas d’insuffisance ventriculaire droite, la pression douce et progressive de l’hypochondre droit entraîne une chasse sanguine hépatique et un retour de sang veineux accru au cœur droit incapable d’écluser ce volume sanguin supplémentaire. On observe la persistance de la distension jugulaire pendant la compression qui ne disparaît pas lors de l’inspiration forcée. C’est l’un des signes les plus caractéristiques de l’insuffisance cardiaque droite.
Turgescence des jugulaires
Chez un sujet normal allongé, tête de lit relevée à 45°, la hauteur du pouls jugulaire est autour de 4 cm au-dessus de l’angle sternal et la veine jugulaire disparaît en inspiration en quelques secondes. À un stade d’insuffisance cardiaque droite évolué, la dilatation des veines jugulaires, spontanément turgescentes, devient permanente ; en cas d’insuffisance tricuspide importante, on peut noter une expansion systolique jugulaire marquée.
Ictère
Un ictère cutané peut être observé en cas de poussée congestive.
Biologiquement, dans les formes sévères, on peut observer une augmentation des concentrations plasmatiques de bilirubine, une augmentation des γ-GT et des phosphatases alcalines (cholestase) qui traduit plutôt la congestion hépatique et des ASAT et ALAT (cytolyse) qui traduit plutôt la baisse du débit sanguin hépatique. Une baisse du facteur V de la coagulation (synthèse hépatique, vitamine K-indépendante) traduit une insuffisance hépatocellulaire, et c’est un marqueur de gravité. Ces altérations biologiques de la fonction hépatique s’améliorent avec le traitement de l’insuffisance cardiaque.
Plus rarement, dans le cas d’insuffisance cardiaque droite chronique prolongée, une cirrhose hépatique d’origine cardiaque peut apparaître.
Œdèmes déclives
Signes immédiatement visibles d’une insuffisance cardiaque droite (ou globale), ils sont en réalité d’abord infracliniques, ne se révélant qu’aux pesées successives.
Ils sont dus principalement à l’augmentation de pression dans l’anse veinulaire des capillaires périphériques qui empêche la réabsorption totale des fluides filtrés normalement dans la branche artériolaire de l’anse, mais également à la rétention hydrosodée et plus rarement à l’hypoprotidémie par dénutrition en cas d’insuffisance cardiaque avancée.
Ils deviennent progressivement manifestes, le soir, au niveau des jambes. Ils sont d’importance variable (gonflement des chevilles ou déformation des jambes avec perte du galbe de la cheville — jambes « en poteaux ») et suivent l’évolution de l’insuffisance cardiaque. On observe aux malléoles ou les faces antérieures des tibias, le signe du godet (empreinte du doigt qui appuie sur la zone d’œdème). En l’absence de traitement, ils s’amplifient et sont apparents dès la simple inspection.
Les œdèmes de l’insuffisance cardiaque droite siègent aux régions déclives (jambes en fin de journée, petit bassin avant le lever), sont bilatéraux et symétriques, longtemps blancs, mous, indolores. S’ils se prolongent, ils peuvent devenir rouges, durs, en particulier au dos du pied et aux régions prétibiales.
Ils répondent au traitement diurétique.
Ils doivent être accompagnés d’un foie cardiaque (et d’un reflux hépatojugulaire) pour confirmer leur origine cardiaque.
Très volumineux, ils peuvent être massifs et généralisés, touchant le petit bassin, l’abdomen et le thorax, et s’accompagnent d’épanchement des séreuses, plèvres (hydrothorax) et péritoine (ascite) : c’est l’état d’anasarque.
À noter que l’œdème du visage est très rarement observé chez le patient insuffisant cardiaque adulte mais peut être retrouvé chez l’enfant.
Signe de Harzer
C’est la palpation au creux épigastrique du battement du ventricule droit hypertrophié/dilaté. Il est recherché en plaçant le pouce de la main droite sous la xyphoïde au cours d’une inspiration profonde, on perçoit une onde de choc de haut en bas correspondant au battement du ventricule droit.
Ascite (et hydrothorax)
L’ascite est due à l’augmentation de la pression dans les veines hépatiques et les veines péritonéales. Elle est liée à une hypertension veineuse systémique prolongée, en particulier en cas de péricardite chronique constrictive, et elle est aggravée par la présence d’une hypoprotidémie (dénutrition, perte protidique digestive, etc.). Les épanchements pleuraux (plus souvent droits) sont tardifs dans l’insuffisance cardiaque droite et ses mécanismes sont identiques à ceux de l’insuffisance cardiaque gauche.
Signes généraux de l’insuffisance cardiaque droite
Cachexie
Une insuffisance cardiaque chronique au stade avancé peut se compliquer, en particulier en cas d’insuffisance cardiaque droite, d’une anorexie et d’une dénutrition en rapport avec les symptômes digestifs, un état inflammatoire chronique et d’hypermétabolisme. Les troubles de l’absorption intestinale et les pertes protidiques digestives sont rares. Ces phénomènes et l’inactivité favorisent la survenue d’une amyotrophie qui participe à l’asthénie et la fatigue musculaire.
ECG de l’insuffisance cardiaque droite
L’ECG est rarement normal. On peut observer une tachycardie sinusale, parfois une arythmie atriale (fibrillation atriale, flutter atrial), des troubles du rythme ventriculaire, un axe de QRS dévié à droite, une hypertrophie atriale droite, une hypertrophie ventriculaire droite, un bloc de branche droit incomplet ou complet (voir chapitre 6 Électrocardiogramme normal et anormal).
Insuffisance cardiaque globale
Les signes cliniques, fonctionnels et généraux associent ceux de l’insuffisance cardiaque gauche et de l’insuffisance cardiaque droite. L’insuffisance cardiaque droite est le plus souvent la conséquence d’une insuffisance cardiaque gauche. Quand les patients en insuffisance cardiaque gauche développent une insuffisance cardiaque droite, les manifestations respiratoires aiguës ont souvent tendance à diminuer (OAP, orthopnée) tant en fréquence qu’en sévérité.
Une autre façon de présenter les signes fonctionnels, physiques et généraux de l’insuffisance cardiaque globale est proposée ci-dessous (tableau 5.2), en regroupant les éléments syndromiques selon deux grands mécanismes : signes liés à la baisse du débit cardiaque et à l’augmentation des pressions de remplissage.
Tableau 5.2. Signes fonctionnels, physiques et généraux de l’insuffisance cardiaque globale.
| Amont
↑ Pression veineuse (pulmonaire/systémique) |
Aval
↓ Débit cardiaque |
||
| Poumons | Dyspnée d’effort, orthopnée, OAP, bendopnée | Muscles périphériques | Fatigue, faiblesse musculaire |
| Foie | Hépatalgie, hépatomégalie, cholestase | Rein | Nycturie, oligurie |
| Rein | Oligurie, rétention hydrosodée | Peau | Vasoconstriction, refroidissement, marbrures |
| Séreuses | Épanchements interstitiels (ascite, épanchement pleural) | Pression artérielle | Baisse |
| Tissus sous-cutanés | Œdèmes | ||
Enfin, la classification de Killip-Kimball est utilisée pour stratifier la gravité des infarctus du myocarde en se fondant sur les signes d’insuffisance cardiaque (tableau 5.3).
________________________________________________________________________________
Comorbidités et insuffisance cardiaque
Les comorbidités sont fréquentes et doivent toujours être recherchées car elles aggravent le pronostic et peuvent restreindre l’utilisation de traitements médicamenteux utiles pour traiter l’insuffisance cardiaque ; en outre, leur traitement peut avoir un effet aggravant sur l’insuffisance cardiaque. Il peut s’agir de : anémie, insuffisance rénale, diabète, bronchopneumopathie chronique obstructive, asthme, angor, cachexie, cancer, dépression, obésité, syndrome d’apnées du sommeil, goutte, hypertension artérielle, etc.
________________________________________________________________________________
Tableau 5.3. Classification de Killip-Kimball.
| Classe | Signes cliniques |
| I | Pas de signe d’insuffisance cardiaque |
| II | Crépitants, galop, signes droits : turgescence jugulaire |
| III | Œdème pulmonaire franc |
| IV | Choc cardiogénique ou hypotension (PAS < 90 mmHg) + signes de vasoconstriction périphérique (oligurie, cyanose, sueurs) |
Insuffisance cardiaque décompensée (= insuffisance cardiaque aiguë)
L’insuffisance cardiaque est une maladie chronique caractérisée par un risque important d’hospitalisations. Ces hospitalisations sont dans la majorité des cas des réhospitalisations pour décompensation cardiaque d’une insuffisance cardiaque chronique, avec dans la majorité des cas des signes congestifs (cf. encadré).
Les facteurs favorisant – ou précipitant – les décompensations, retrouvés dans 75 % des cas, sont principalement : les infections (pulmonaires), l’ischémie myocardique (syndrome coronaire aigu), les arythmies supraventriculaires (fibrillation atriale, flutter atrial), la mauvaise observance du traitement et des consignes diététiques, l’hypertension artérielle mal contrôlée, l’anémie, une dysthyroïdie, l’aggravation de l’insuffisance rénale et, plus rarement, une embolie pulmonaire.
La grande majorité de ces facteurs précipitant les décompensations peut être prévenue et leur contrôle permettrait de limiter les réhospitalisations.
________________________________________________________________________________
En pratique – Reconnaître les quatre profils hémodynamiques de l’insuffisance cardiaque décompensée
La plupart des patients hospitalisés pour une décompensation cardiaque peuvent être classés selon l’un des quatre profils cliniques ci-dessous en fonction de la présence de signes congestifs et de signes d’hypoperfusion (tableau 5.4) :
- signes congestifs :
- orthopnée ;
- turgescence jugulaire ;
- râles crépitants ;
- hépatomégalie ;
- ascite ;
- œdème ;
- signes d’hypoperfusion :
- pression artérielle pincée ;
- extrémités froides, marbrures des genoux ;
- obnubilation ;
- intolérance aux IEC ou ARA II (hypotension artérielle) ;
- oligurie progressive.
Cette classification permet d’orienter très rapidement la prise en charge thérapeutique.
________________________________________________________________________________
Tableau 5.4. Profils cliniques de l’insuffisance cardiaque décompensée.
| Congestion au repos ? | |||
| Non | Oui | ||
| Hypoperfusion au repos ? | Non | « Chaud et sec » | « Chaud et humide » |
| Oui | « Froid et sec » | « Froid et humide » | |
Causes de l’insuffisance cardiaque
Principales causes
L’insuffisance cardiaque peut être considérée comme la manifestation évolutive de l’ensemble des maladies acquises ou congénitales du myocarde, péricarde ou endocarde, des coronaires, de l’aorte et de l’artère pulmonaire.
________________________________________________________________________________
Les deux principales causes, représentant environ 90 % des cas d’insuffisance cardiaque dans les pays industrialisés, sont :
- l’athérosclérose coronaire (insuffisance cardiaque post-SCA, insuffisance cardiaque au cours de l’ischémie myocardique, voir chapitre 3) ;
- l’hypertension artérielle (voir chapitre 2.1).
________________________________________________________________________________
Autres causes
Les autres causes les plus fréquentes sont ensuite :
- les pathologies valvulaires (voir chapitre 4) ;
- les cardiomyopathies primitives (hypertrophique, dilatée, restrictive, dysplasie arythmogène) (voir encadré).
Les autres causes sont plus rares, représentées par :
- les causes infectieuses : myocardites virales ;
- les cardiopathies congénitales ;
- les cardiomyopathies spécifiques, secondaires à des maladies générales (amylose, sarcoïdose, hémochromatose, etc.) ;
- autres causes : cardiomyopathies toxiques (chimiothérapies aux anthracyclines) et métaboliques, cardiomyopathie du peri partum, cardiomyopathie rythmique, insuffisance cardiaque à débit élevé, etc.
Les causes de l’insuffisance cardiaque droite :
- principalement l’insuffisance ventriculaire gauche compliquée d’hypertension pulmonaire ;
- le rétrécissement mitral (sans insuffisance ventriculaire gauche) ;
- les pathologies pulmonaires chroniques compliquées d’hypertension artérielle pulmonaire ;
- les embolies pulmonaires massives responsables d’insuffisance cardiaque droite aiguë ou les embolies pulmonaires répétées (cœur pulmonaire chronique postembolique) ;
- les cardiopathies congénitales ;
- les cardiomyopathies du cœur droit (cardiomyopathies arythmogènes) ;
- les valvulopathies du cœur droit.
Facteurs de risque d’insuffisance cardiaque
Au-delà des causes listées ci-dessus, le meilleur moyen de prévenir la survenue d’une insuffisance cardiaque est de contrôler les facteurs de risque cardiovasculaires et les conditions responsables d’insuffisance cardiaque :
- les facteurs de risque modifiables de l’athérosclérose coronaire (voir chapitres 2.1 et 2.2) ;
- l’hypertension artérielle ;
- le diabète ;
- l’obésité ;
- l’alcoolisme.
________________________________________________________________________________
Pour comprendre – Nosologie et aspects anatomiques des cardiomyopathies
Concernant les cardiomyopathies (fig. 5.14 et 5.15), la Société européenne de cardiologie en 2007 a proposé de les identifier selon la morphologie et la fonction ventriculaire gauche et leur origine génétique/familiale ou non.
________________________________________________________________________________
Figure 5.14. Classification des cardiomyopathies (European Society of Cardiology, 2008).
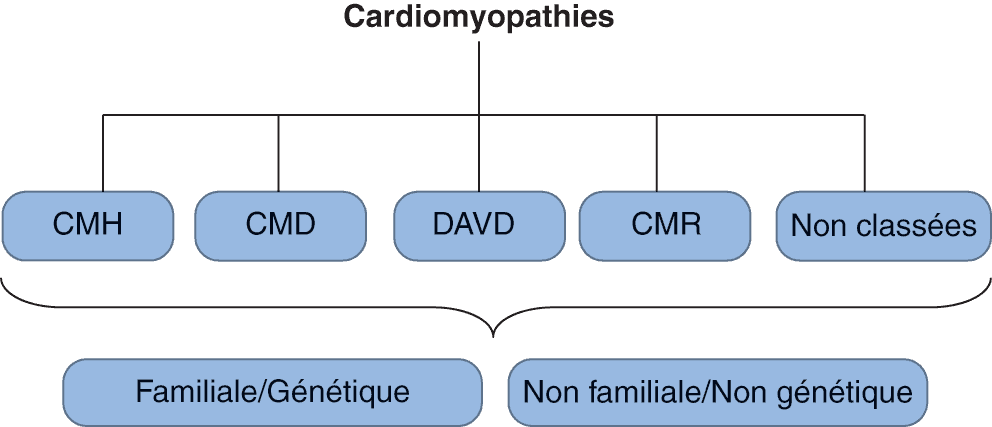
CMH, cardiomyopathie hypertrophique ; CMD, cardiomyopathie dilatée ; DAVD, dysplasie arythmogène du ventricule droit ; CMR, cardiomyopathie restrictive.
Source : d’après Elliott P. Classification of the cardiomyopathies: a position statement from the european society of cardiology working group on myocardial and pericardial diseases. Eur Heart J, 2008 ;29:270–6.
________________________________________________________________________________
Figure 5.15. Cardiomyopathies : aspects macroscopique et histologique.
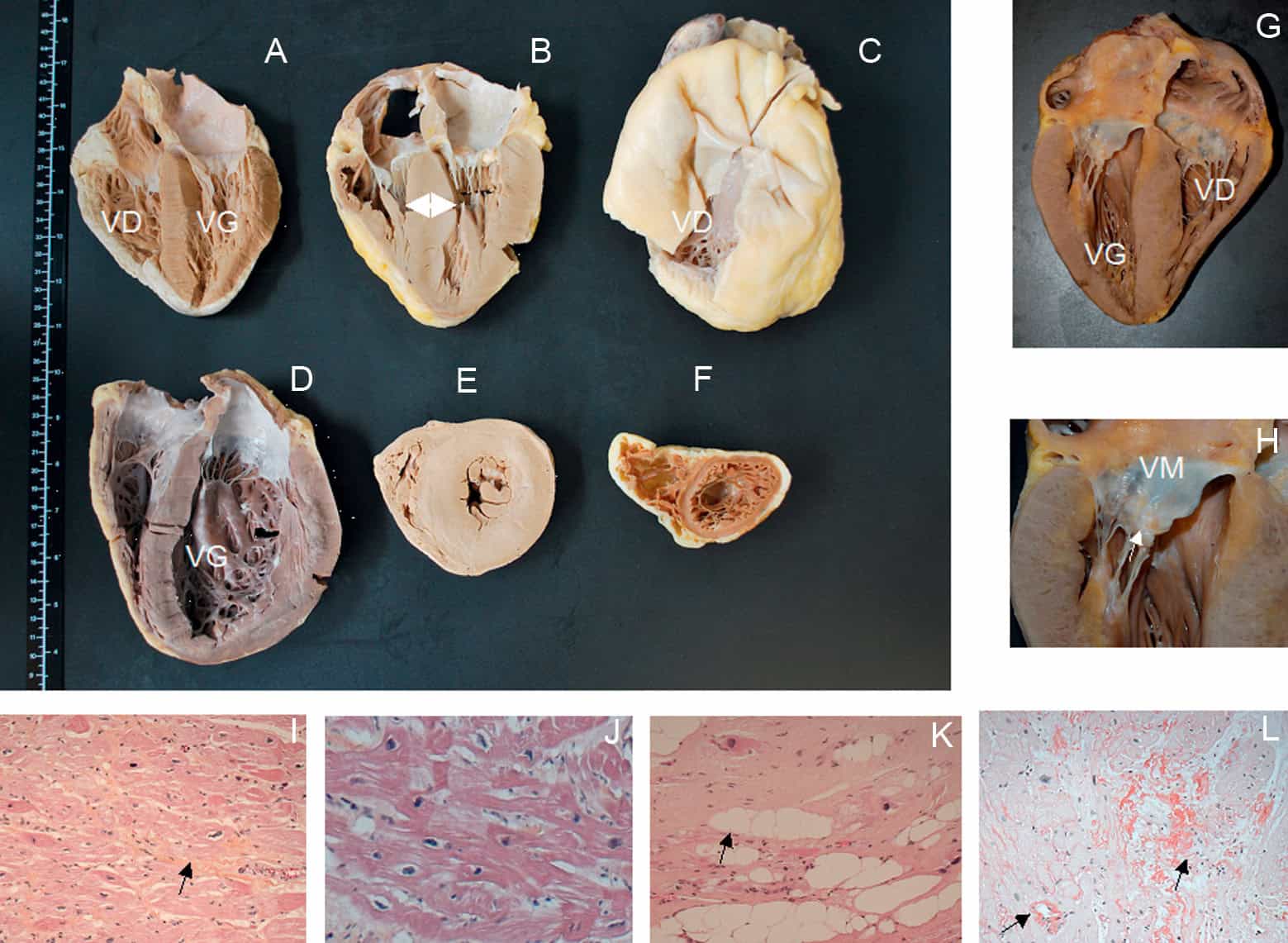
A. Cœur normal. B, E, J. Cardiomyopathie hypertrophique primitive (CMH). B, E. Hypertrophie septale prédominante (↔). J. Fibres myocardiques hypertrophiques et désorganisées (coloration hématoxyline éosine safran, HES, × 200). C, F, K. Dysplasie arythmogène du ventricule droit (DAVD). C, F. Dilatation majeure du ventricule droit avec aspect adipeux de la paroi. F. Régression fibro-adipeuse du myocarde avec nombreux adipocytes (→) (coloration HES, × 200). D, I. Cardiomyopathie dilatée (CMD). D. Dilatation majeure du ventricule gauche. I. Fibres myocardiques dystrophiques et fibrose interstitielle (→) (coloration HES, × 200). G, H, L. Cardiopathie restrictive (amylose cardiaque) (CMR). G. Hypertrophie diffuse des parois atriales et ventriculaires. H. Dépôts amyloïdes au niveau des valves (→). L. Dépôts amyloïdes fibrillaires intramyocardiques, colorés par le rouge Congo, de topographie interstitielle et vasculaire (→) (coloration au rouge Congo, × 200).
VG, ventricule gauche ; VD, ventricule droit ; VM, valve mitrale.
________________________________________________________________________________
Cardiomyopathie dilatée
Le cœur apparaît souvent dilaté, flasque à pointe arrondie. À l’ouverture, il existe une dilatation prédominante des cavités ventriculaires. La paroi ventriculaire est d’épaisseur normale, amincie ou discrètement augmentée, contrastant avec l’importance de la dilatation des cavités. La masse myocardique est généralement augmentée. Les valves et les coronaires sont normales.
L’histologie standard est souvent peu spécifique, avec des lésions plus ou moins étendues, caractérisées par des fibres myocardiques dystrophiques de calibre variable avec des noyaux bien visibles et une fibrose interstitielle non systématisée. Néanmoins, certains aspects histologiques peuvent permettre une orientation diagnostique. Par exemple, la clarification cytoplasmique des fibres myocardiques peut faire suspecter une cause toxique ou une pathologie mitochondriale.
Cardiomyopathie hypertrophique
Elle est définie par une augmentation de la masse myocardique du cœur. Cet épaississement prédomine au niveau des parois du ventricule gauche (le plus souvent sur le septum intraventriculaire) et est souvent associé à une diminution de la taille de la cavité ventriculaire. Dans cette forme prédominant sur le septum intraventriculaire, on parle d’hypertrophie asymétrique.
Sur le plan histologique, on observe une désorganisation plus ou moins diffuse de l’architecture des fibres myocardiques qui prennent une orientation anarchique. Ces fibres ont une augmentation de leur calibre (elles sont dites hypertrophiques) avec un noyau volumineux, charbonneux. Il existe également une fibrose interstitielle et on peut observer des vaisseaux aux parois épaissies, dystrophiques.
Ces aspects macroscopique (hypertrophie asymétrique) et microscopique font évoquer en premier le diagnostic de cardiomyopathie hypertrophique sarcomérique.
L’analyse histologique permet d’éliminer d’autres causes d’hypertrophie : les hypertrophies métaboliques par surcharge (l’amylose, les glycogénoses, par exemple), où l’hypertrophie myocardique ventriculaire est plus souvent symétrique.
Cardiomyopathie restrictive (CMR)
Dans la forme classique, le ventricule gauche conserve ses dimensions tandis que l’atrium gauche présente un épaississement de sa paroi puis se dilate au cours de l’évolution de la maladie. L’examen macroscopique recherche un épaississement endocardique ou myocardique pouvant réduire les cavités ventriculaires. Au cours de l’évolution et en fonction de la cause une hypertrophie ventriculaire peut s’installer en pratique dans les causes infiltratives ou de surcharge.
L’histologie peut confirmer le diagnostic d’amylose, étiologie la plus fréquente de ce type de cardiopathie. Il s’agit d’un dépôt finement fibrillaire interstitiel et vasculaire, coloré en rouge par le rouge Congo et prenant un aspect biréfringent en lumière polarisée. Sa caractérisation précise (amylose à chaînes légères, à transthyrétine, etc.) nécessite une étude immunohistochimique complémentaire sur prélèvement congelé. Dans d’autres cas, il peut s’agir d’une fibrose endocardique associée ou non à une hyperéosinophilie. Dans certains cas, l’histologie est non spécifique.
Dysplasie arythmogène
Dans sa forme typique de dysplasie arythmogène du ventricule droit (DAVD), on observe une dilatation du ventricule droit avec un amincissement de sa paroi qui peut devenir translucide.
Histologiquement, il existe une régression fibro-adipeuse du myocarde, c’est-à-dire un remplacement des fibres myocardiques par un tissu fibreux et adipeux. Ces anomalies prédominent au niveau du ventricule droit mais peuvent s’étendre au ventricule gauche.
Génétique des cardiomyopathies
Jusqu’à un passé récent, l’origine familiale et la possibilité d’une transmission héréditaire des cardiomyopathies était rarement évoquée avec les patients. Mais le dépistage familial, qui doit être systématiquement conduit, et les progrès scientifiques et techniques permettent, maintenant, de retrouver fréquemment une origine génétique, variable avec le type de cardiomyopathie – plus fréquent avec les CMH que les CMD, la dysplasie arythmogène et les CMR – le plus souvent avec une transmission autosomique dominante. De nombreuses mutations pathogènes sont identifiées le plus souvent dans des gènes qui codent pour des protéines du sarcomère (en premier lieu MYH7 codant pour la chaîne lourde β de la myosine et MYBPC3 codant pour la protéine C liant la myosine). Une atteinte musculaire périphérique associée est possible (mutations de la dystrophine, par exemple, dans la maladie de Duchenne). Certaines mutations peuvent également altérer le codage de protéines en dehors du sarcomère conduisant à des anomalies multi-systémique avec atteinte cardiaque (maladie de Fabry liée à un déficit de l’alpha galactosidase entraînant l’accumulation de sphingolipides dans les organes, se traduisant par une hypertrophie cardiaque) ou à des dépôts intracardiaques (amylose à transthyrétine mutée à l’origine d’une hypertrophie cardiaque). Le screening familial conseillé par le groupe d’expert européen chez les apparentés au premier degré en cas cardiomyopathie nécessite un ECG, une échocardiographie (et un Holter-ECG des 24 heures si un trouble de la conduction est observé chez le propositus) à partir de 10–12 ans, tous les 3–5 ans si réalisé avant 10 ans, tous les 1–2 ans entre 10 and 20 ans, tous les 2–5 ans après 20 ans et arrêté vers 50–60 ans.
________________________________________________________________________________
Marqueurs biochimiques en pratique clinique
De nombreux marqueurs biochimiques ont été décrits pour le diagnostic et la prise en charge des insuffisants cardiaques. Ne sont détaillés ici que les marqueurs les plus utilisés.
Fonction rénale (urémie, créatininémie, formules estimant la clairance)
Près d’un insuffisant cardiaque sur deux a une atteinte de la fonction rénale. Les mécanismes de cette dysfonction associent l’hypoperfusion rénale induite par la vasoconstriction, la réaction hormonale et, chez un patient sur trois, une insuffisance rénale liée à un facteur de risque cardiovasculaire comme le diabète ou la maladie athéromateuse. Mais, dans cette population âgée, d’autres causes que cardiovasculaires peuvent coexister, en particulier l’hypertrophie prostatique chez l’homme.
Il existe aussi fréquemment une part fonctionnelle réversible dans l’insuffisance rénale de l’insuffisance cardiaque qui peut être évaluée par le dosage combiné de l’urémie et de la créatinémie.
Le diagnostic de syndrome cardiorénal s’évoque surtout en présence d’une insuffisance rénale aiguë apparaissant dans un contexte d’insuffisance cardiaque ne répondant pas au traitement initial, ou présente à l’entrée et s’améliorant après traitement de l’insuffisance cardiaque. La priorité en cas de syndrome cardiorénal est de diminuer la congestion veineuse et/ou de rétablir un débit cardiaque.
La surveillance de la fonction rénale est indispensable dans le suivi des patients insuffisants cardiaques, car de nombreux médicaments de l’insuffisance cardiaque ont une élimination rénale et leur posologie doit être adaptée à la fonction rénale pour éviter un surdosage. Une fonction rénale altérée est un facteur pronostique péjoratif.
La fonction rénale est, au mieux, estimée par une formule car les taux sériques de créatinine et son élimination sont dépendants de l’âge, du sexe et de la masse musculaire en particulier.
L’adaptation des posologies des médicaments se fait actuellement en fonction de la clairance de la créatinine estimée par la formule de Cockcroft et Gault :
Clairance de la créatinine = (140-âge)×P / Créatininémie [μmol/l] × K
avec K = 1,23 pour les hommes, K = 1,03 pour les femmes et P le poids en kg.
La formule MDRD, qui ne tient pas compte du poids, semble plus pertinente pour estimer la fonction rénale chez les sujets maigres, âgés de plus de 65 ans, les obèses, les femmes enceintes et les sujets noirs.
La Haute Autorité de santé retient la formule CKD-EPI comme équation la plus fiable pour estimer la fonction rénale en cas d’insuffisance rénale chronique. Elle suggère d’utiliser le site de la Société́ française de néphrologie et précise que le résultat, déjà indexé à la surface corporelle, ne doit pas être réadapté à la surface corporelle du patient et que l’équation CKD-EPI n’est pas complètement validée chez le sujet non caucasien, les sujets de plus de 75 ans, les patients de poids extrême, dénutris ou ayant une alimentation pauvre en protéines animales.
Définition de l’insuffisance rénale aiguë
Le diagnostic de syndrome cardio-rénal s’évoque surtout en présence d’une insuffisance rénale aigüe (IRA) apparaissant dans un contexte d’insuffisance cardiaque ne répondant pas au traitement initial ou présente à l’entrée et s’améliorant après traitement de l’insuffisance cardiaque. La priorité en cas de syndrome cardio-rénal est de diminuer la congestion veineuse et/ou de rétablir un débit cardiaque. En cas de congestion veineuse et de baisse du débit cardiaque, des mécanismes d’adaptation de l’hémodynamique rénale se mettent en place, notamment une activation du SRAA). Si ceux-ci sont dépassés, du fait d’une insuffisance cardiaque sévère, le débit de filtration glomérulaire (DFG) diminue : on parle de syndrome cardio-rénal de type 1. Il peut s’associer une baisse de la pression de perfusion rénale due en partie à une diminution du débit cardiaque. Dans ces cas, (a fortiori en cas de choc cardiogénique), si l’insuffisance cardiaque se prolonge, une atteinte organique rénale d’origine principalement ischémique peut apparaître, on parle alors de nécrose tubulaire aiguë. Voir tableaux 5.5 5.6 et 5.7.
________________________________________________________________________________
Tableau 5.5. Définition de l’insuffisance rénale aiguë Kidney Disease Improving Global Outcome (KDIGO).
| KDIGO 1 | KDIGO 2 | KDIGO 3 | |
| Variation de la créatinine sur prélèvements successifs | Augmentation > 26,5 μmol/l | N’importe quelle valeur > 353,6 μmol/l | |
| Variation de la créatinine par rapport à la base | 1,5 à 1,9 fois la base | 2 à 2,9 fois la base | ≥ 3 fois la base |
| Diurèse | < 0,5 ml/kg/h sur > 6 heures | < 0,5 ml/kg/h sur > 12 heures | < 0,3 ml/kg/h sur > 24 heures
Anurie sur > 12 heures |
Tableau 5.6. Principaux marqueurs biologiques permettant de différencier IRA fonctionnelle et nécrose tubulaire aiguë.
| IRA fonctionnelle | Nécrose tubulaire aiguë | |
| [Na] u | < 20 mmol/l | > 40 mmol/l |
| [Na] u / [K] u | < 1 | > 1 |
| Fraction d’excrétion du sodium | < 1 % | > 1 % |
| Fraction d’excrétion de l’urée | < 35 % | > 35 % |
| [urée] u / [urée] p | > 10 | < 10 |
| [creatinine] u / [creatinine] p | > 30 | < 30 |
| [urée] p / [creatinine] p | > 100 | < 50 |
Tableau 5.7. Classification du syndrome cardio-rénal en fonction de l’atteinte initiale.
________________________________________________________________________________
Natrémie
L’hyponatrémie est fréquemment observée, souvent associée à une inflation hydrosodée avec hémodilution. Elle est le signe d’une réaction hormonale excessive ou non contrôlée par le traitement, en particulier une activation du système rénine-angiotensine-aldostérone. Le traitement par IEC réduit efficacement le risque d’hyponatrémie. Il s’agit d’un paramètre de mauvais pronostic à court terme. L’hyponatrémie doit être corrigée rapidement, car elle expose à un risque de troubles neurologiques (confusion mentale, convulsion, coma). L’hyponatrémie peut être aussi favorisée par un excès de traitement diurétique, avec une perte excessive de sodium.
Kaliémie
Les troubles de la kaliémie (hypokaliémie ou hyperkaliémie) sont fréquents chez les insuffisants cardiaques. Ils favorisent les troubles du rythme et de la conduction. De nombreux facteurs influent sur la kaliémie. Les diurétiques de l’anse le plus souvent utilisés sont hypokalémiants (diurétique de l’anse, thiazidiques) mais d’autres molécules diurétiques sont hyperkaliémiantes (antagonistes des récepteurs minéralo-corticoïdes. L’insuffisance rénale et les médicaments ciblés contre le système rénine-angiotensine-aldostérone sont hyperkaliémiants.
Peptides natriurétiques de type B
Ces marqueurs biochimiques sont issus de l’étude du remodelage moléculaire et cellulaire cardiaque observé dans les cardiopathies et sont utilisés en routine dans le suivi clinique des patients.
Il s’agit d’une famille de protéines fortement sécrétées par les cardiomyocytes dans l’insuffisance cardiaque. En pratique, après sécrétion par le cardiomyocyte, le proBNP est clivé enzymatiquement en peptide natriurétique de type B (BNP) et NT-proBNP (extrémité N-terminale du pro-BNP). Seul le BNP a une activité biologique mais les deux molécules sont des marqueurs fiables utilisés en routine. Leur niveau de sécrétion et, donc, leur taux sanguin sont directement influencés par le niveau d’étirement cellulaire des cardiomyocytes. Ils sont des marqueurs du niveau de pression de remplissage cardiaque qui détermine la surcharge de la paroi des ventricules et donc l’étirement cellulaire mais également des marqueurs de l’intensité du remodelage cardiaque et/ou de l’hypertrophie ventriculaire. Les pathologies associées à une augmentation de la contrainte mécanique des parois ventriculaires gauches ou droites (comme une embolie pulmonaire compliquée de surcharge ventriculaire droite), augmentent le taux sanguin de peptides natriurétiques. À l’inverse, chez un patient insuffisant cardiaque bien traité, on observera une diminution du taux sanguin de peptides natriurétiques s’il est euvolémique. Parfois, chez certains patients chez qui il est possible d’obtenir un remodelage inverse et une normalisation des fonctions ventriculaires grâce au traitement de la cause ou grâce aux traitements cardioprotecteurs, on pourra observer une normalisation des taux sanguins de peptides natriurétiques. L’âge, le poids et la fonction rénale doivent être pris en compte dans l’interprétation, car ils modifient le taux sanguin de ces marqueurs. Enfin, le taux sanguin de BNP et de NT-proBNP a une valeur pronostique.
Le dosage des peptides natriurétiques est utilisé dans deux situations :
- pour faire le diagnostic d’une insuffisance cardiaque dans un bilan de dyspnée aiguë en complément du bilan clinique et paraclinique (fig. 5.16). Chez les patients pour lesquels un doute diagnostique persiste après le bilan initial, un taux sanguin de BNP < 100 pg/ml exclut à 95 % le diagnostic d’insuffisance cardiaque, alors qu’un taux > 400 pg/ml confirme à 95 % le diagnostic. Le dosage de BNP ou NT-proBNP n’a aucun intérêt si le diagnostic clinique de l’insuffisance cardiaque est certain ;
________________________________________________________________________________
Figure 5.16. Algorithme pour le diagnostic étiologique d’une dyspnée aiguë.
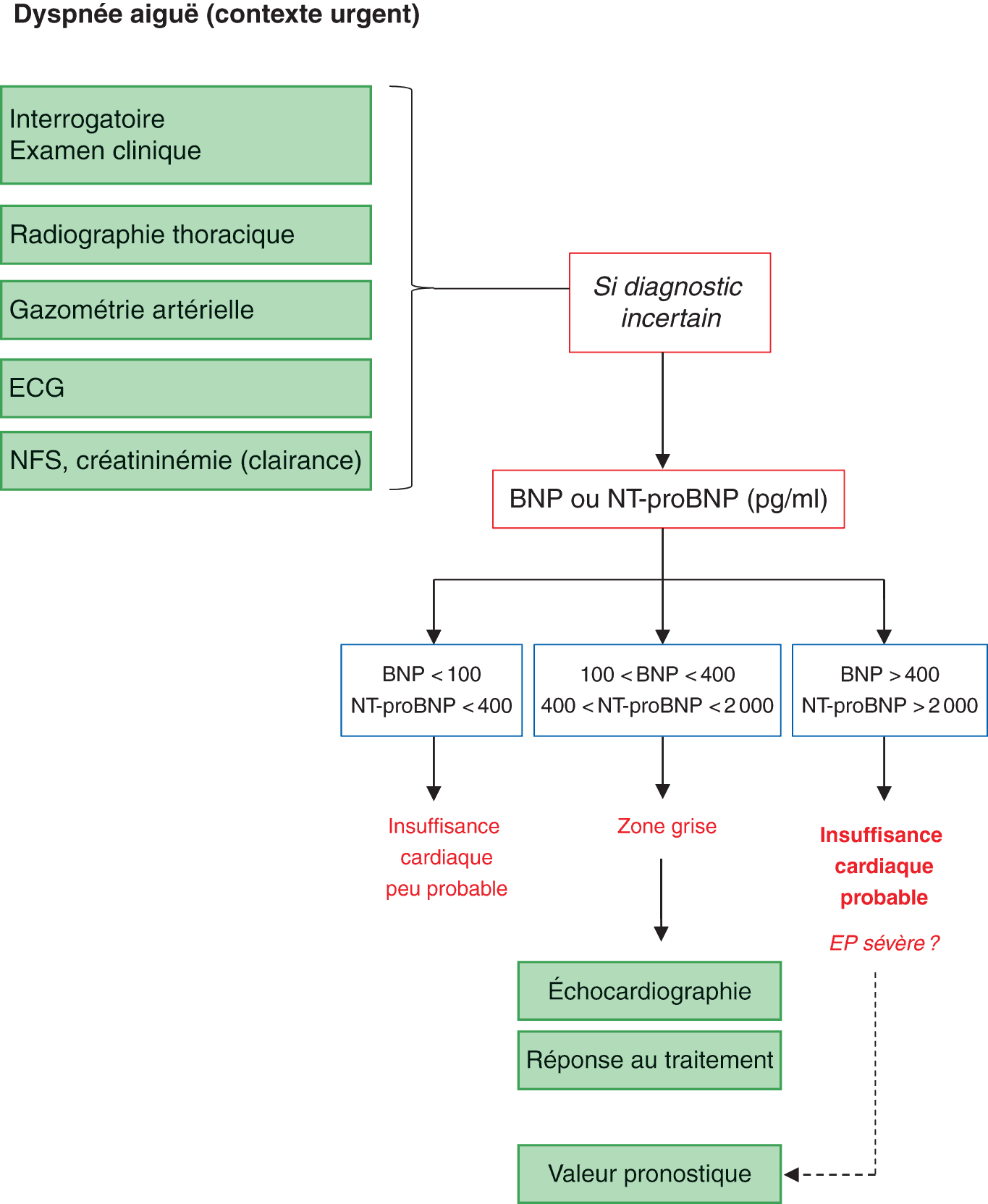
Source : d’après Cohen A, Berthelot-Garcias E, Douna F. Urgences cardiovasculaires et situations critiques en cardiologie. Paris : Elsevier-Masson ; 2010.
________________________________________________________________________________
- pour le suivi de l’insuffisant cardiaque chronique ou après une décompensation : l’évolution du taux sanguin dans le temps permet de juger de l’efficacité du traitement mis en place ; une augmentation des taux de BNP ou NT-proBNP doit inciter à majorer le traitement (majoration des posologies et/ou thérapeutique supplémentaire).
Hémoglobine
L’anémie est fréquemment associée à l’insuffisance cardiaque. Il s’agit d’un facteur péjoratif important de la maladie car le taux sanguin d’hémoglobine conditionne les apports en oxygène au tissu cardiaque. Une anémie favorisera donc une hypoxie cardiaque chronique, favorisant entre autres la mort cellulaire. L’anémie est liée à une combinaison de mécanismes. L’hémodilution, liée à la rétention hydrosodée induite par la réaction hormonale, est la première cause d’anémie. Il existe, également, une diminution de la production des globules rouges favorisée par une carence martiale fréquente chez les insuffisants cardiaques, une diminution de la production d’érythropoïétine par le rein, en particulier en cas d’insuffisance rénale associée, et la diminution de l’érythropoïèse au niveau de la moelle osseuse favorisée par certains médicaments de l’insuffisance cardiaque inhibant le système rénine-angiotensine comme les inhibiteurs de l’enzyme de conversion (IEC) ou les antagonistes du récepteur de l’angiotensine II (ARA II).
Bases du traitement, pharmacologie
Cette section décrit les grands principes du traitement de l’insuffisance cardiaque à fonction systolique altérée, en se fondant sur les connaissances physiopathologiques.
Le traitement est tout d’abord étiologique. Le bilan clinique et paraclinique recherchera systématiquement l’étiologie de l’insuffisance cardiaque, qui sera traitée afin de corriger la cause de la dysfonction ventriculaire (valvulopathie, maladie coronaire, etc.).
Les progrès réalisés au cours des trente dernières années dans l’étude des mécanismes physiopathologiques de l’insuffisance cardiaque chronique ont permis de trouver des traitements efficaces sur les symptômes, la survie et la qualité de vie. Ces traitements sont systématiquement administrés aux patients ayant une dysfonction ventriculaire gauche systolique selon des modalités précisées par les recommandations de la Société européenne de cardiologie, en fonction du stade de la maladie et des comorbidités.
Traitement de l’insuffisance cardiaque aiguë
Le traitement repose essentiellement sur les diurétiques de l’anse et les dérivés nitrés intraveineux en cas de décompensation cardiaque.
Diurétiques de l’anse
Les deux molécules principalement utilisées sont le furosémide et le bumétanide.
Ils peuvent s’utiliser au long cours per os, afin de limiter les signes congestifs. Ils s’utilisent par voie intraveineuse lors d’œdème aigu pulmonaire (OAP) ou de décompensation cardiaque.
Les diurétiques de l’anse inhibent le cotransport du NaCl dans la branche ascendante de l’anse de Henlé, ce qui provoque un effet natriurétique. Ils augmentent l’excrétion du potassium, du calcium et du magnésium. Ils sont parfois associés aux diurétiques thiazidiques (hydrochlorothiazide) en cas de résistance aux diurétiques.
Leurs effets secondaires principaux sont l’hypokaliémie, la déshydratation, la majoration d’une insuffisance rénale préexistante, l’ototoxicité.
Dérivés nitrés
Les dérivés nitrés tels que le dinitrate d’isosorbide sont utilisés en cas d’insuffisance cardiaque décompensée, particulièrement lors de l’OAP hypertensif par voie intraveineuse. Ils ont une action vasodilatatrice en agissant sur les cellules musculaires lisses via le monoxyde d’azote (NO) qui en résulte après avoir été dénitratés. L’action du NO, vasorelaxante, s’effectue au niveau artériel, artériolaire et surtout veineux avec pour conséquence une réduction de la précharge des ventricules.
Les effets secondaires sont l’hypotension artérielle et les céphalées.
Autres
L’administration d’oxygène par voie nasale ou masque est systématique en cas d’hypoxémie. Le recours à la morphine peut soulager un patient très anxieux ou en grande détresse.
Choc cardiogénique
Cette situation grave nécessite l’usage d’agonistes β1-adrénergiques, tels que la dobutamine, et/ou les inhibiteurs des phosphodiestérases de type 3.
La dobutamine est une amine proche de la noradrénaline, inotrope positive, administrée par voie veineuse.
Ses autres actions sont :
- une action chronotrope positive ;
- une vasodilatation modérée ;
- une augmentation de la consommation en oxygène.
Elle permet, ainsi, de maintenir un niveau de pression artérielle correct en augmentant le débit cardiaque et en abaissant modérément la postcharge.
Les inhibiteurs des phosphodiestérases de type 3 sont inotropes positifs également et sont utilisés par voie intraveineuse surtout en deuxième intention ou en association à la dobutamine. Ils sont également vasodilatateurs.
Les inotropes positifs sont utilisés pour une durée limitée par voie intraveineuse dans les situations d’insuffisance cardiaque décompensée avec baisse du débit cardiaque. Leur administration au long cours per os ou répétée par voie intraveineuse n’a jamais montré d’effet bénéfique sur la survie et est au contraire potentiellement délétère.
Traitement de fond de l’insuffisance cardiaque à FEVG abaissée
Traiter l’insuffisance cardiaque à FEVG abaissée, c’est :
- contrôler la congestion (diurétiques, régime pauvre en sel) ;
- prescrire les traitements qui diminuent la mortalité, préviennent les aggravations et améliorent la qualité de vie : inhibiteurs de l’enzyme de conversion (IEC), antagonistes des récepteurs de l’angiotensine II (ARA II), INRAN (antagoniste combiné de l’angiotensine II – valsartan et de la néprilysine – sacubitril), anti-aldostérone, bêtabloquants, ivabradine, resynchronisateur-défibrillateur cardiaque ;
- en association avec des traitements adjuvants pour améliorer les symptômes (dérivés nitrés, réadaptation cardiovasculaire).
La prescription de ces traitements se fait selon des modalités précises d’administration et de surveillance clinique et biologique détaillées en deuxième cycle des études de médecine.
Ce traitement per os doit être mis en place dès le stade II de la NYHA et en dehors de toute poussée d’insuffisance cardiaque.
Les traitements étudiés ont prouvé leur efficacité en cas d’insuffisance cardiaque avec FEVG altérée en diminuant la morbimortalité.
________________________________________________________________________________
L’ordonnance d’un patient traité pour insuffisance cardiaque à FEVG altérée comprend :
- un IEC ou un ARA II / ou INRAN si reste symptomatique
- un bêtabloquant ;
- de la spironolactone ou une molécule apparentée (éplérénone) ;
- un diurétique de l’anse si présence de signes congestifs.
________________________________________________________________________________
Diurétiques
Les diurétiques favorisent l’excrétion de sodium et d’eau ; ils permettent de traiter et contrôler la rétention hydrosodée (diurétiques thiazidiques, diurétiques de l’anse) et d’obtenir un état d’euvolémie. Après la phase de décompensation, ils doivent être utilisés aux doses minimales efficaces, adaptés à chacun pour limiter l’activation du système rénine-angiotensine-aldostérone.
Les diurétiques thiazidiques ont une action moins diurétique que les diurétiques de l’anse de Henlé.
Les effets des diurétiques de l’anse et thiazidiques sur la survie n’ont jamais été étudiés.
Inhibiteurs de l’enzyme de conversion et antagonistes des récepteurs de l’angiotensine II
Les inhibiteurs de l’enzyme de conversion (IEC) et les antagonistes des récepteurs de l’angiotensine II (ARA II) s’opposent aux effets négatifs de l’activation chronique du système rénine-angiotensine-aldostérone. Pour rappel, l’angiotensine II, résultant de la dégradation de l’angiotensine par la rénine, a des effets vasoconstricteurs. Les IEC agissent non seulement comme des vasodilatateurs mais aussi contre le remodelage délétère du ventricule gauche induit par l’angiotensine II. En diminuant les résistances artérielles périphériques, ils améliorent le travail cardiaque.
De nombreux essais cliniques dans l’insuffisance cardiaque chronique et après infarctus du myocarde ont montré qu’ils réduisaient la mortalité, les réhospitalisations, et amélioraient les capacités d’effort et la qualité de vie.
IEC
Les IEC utilisés dans l’insuffisance cardiaque sont le ramipril, le captopril, l’énalapril, le lisinopril et le trandolapril.
Leurs effets indésirables sont l’hyperkaliémie, l’insuffisance rénale aiguë, la toux, l’hypotension artérielle et l’allergie (œdème de Quincke) – cette dernière contre-indique toute nouvelle introduction d’un IEC.
ARA II
Les ARA II sont indiqués en cas d’intolérance aux IEC : ils peuvent être utilisés à la place des IEC en cas d’allergie ou de toux sous IEC. Leurs effets indésirables sont l’hyperkaliémie, l’insuffisance rénale aiguë, l’hypotension artérielle et l’allergie.
Les ARA II utilisés sont le candesartan, le losartan et le valsartan.
Antagonistes des récepteurs de l’angiotensine II et inhibiteurs de la néprilysine (INRAN)
La néprilysine, une endopeptidase neutre, enzyme impliquée dans la dégradation de nombreux peptides et en particulier les peptides natriurétiques : ANP, BNP, CNP (également l’angiotensine II, angiotensine I, l’adrénomédulline, la substance P, la bradykinine, l’endothéline-1). L’inhibition de la néprilysine par le sacubitril entraîne une augmentation des taux circulants d’ANP, de BNP et de leurs effets physiologiques via l’augmentation du GMPc, améliorant diurèse, natriurèse, relaxation myocardique et vasculaire avec un effet anti-remodelage délétère. L’association du sacubitril avec un antagoniste des récepteurs AT1 de l’angiotensine 2 permet de combiner les effets potentiellement favorables et a prouvé sa supériorité par rapport au seul blocage du SRAA dans un essai clinique dans l’insuffisance cardiaque à FEVG abaissée. En revanche, cette association n’a pas prouvé son efficacité dans l’insuffisance cardiaque à FEVG préservée.
L’Entresto® est le premier représentant de cette nouvelle classe thérapeutique combinant le valsartan, antagoniste de l’angiotensine II et le sacubitril, inhibiteur de la néprilysine. Il a démontré une réduction significative de la mortalité cardiovasculaire, mortalité totale, réhospitalisations pour insuffisance cardiaque chez des patients insuffisants cardiaques chroniques à fraction d’éjection altérée en comparaison aux IEC. Ses effets indésirables sont l’hypotension artérielle – l’effet vasodilatateur est plus marqué que celui d’un ARAII ou d’un IEC – l’hyperkaliémie, l’insuffisance rénale et l’allergie.
Bêtabloquants
Les bêtabloquants s’opposent aux effets négatifs de l’activation chronique du système sympathique. Les bêtabloquants baissent la fréquence cardiaque (effet chronotrope négatif), la contractilité myocardique (effet inotrope négatif), le débit cardiaque, la pression artérielle systolique et diastolique et ont une action anti-ischémique.
Les bêtabloquants inhibent les effets de la stimulation sympathique au niveau cardiaque, ce qui permet la réduction de l’augmentation de la fréquence cardiaque et de pression artérielle au cours de l’effort physique secondaire à la stimulation sympathique physiologique. Ils diminuent la production de rénine par l’appareil juxtaglomérulaire.
Ils diminuent la mortalité globale, subite et par insuffisance cardiaque dans l’insuffisance cardiaque chronique systolique. Ils améliorent la capacité d’effort, les symptômes et la fonction systolique, s’opposent au remodelage ventriculaire quelle que soit la cause de l’insuffisance cardiaque. Les mécanismes d’action sont multiples, en partie liés au ralentissement de la fréquence cardiaque.
Ceux utilisés dans l’insuffisance cardiaque à FEVG altérée sont : le nébivolol, le bisoprolol, le carvédilol, le métoprolol.
Les bêtabloquants sont utilisés per os et introduits en dehors de tout épisode de décompensation cardiaque, à petites doses qui sont augmentées ensuite par paliers progressifs et successifs sur quelques semaines.
Les contre-indications aux bêtabloquants se sont réduites et comprennent l’asthme, le syndrome de Raynaud et les troubles de la conduction atrioventriculaire de haut grade non appareillés. La BPCO et l’artériopathie oblitérante des membres inférieurs bien contrôlées ne sont plus considérées comme des contre-indications.
Les effets indésirables sont l’asthénie, la dysfonction érectile, l’hypotension artérielle.
Diurétiques épargneurs de potassium
Les diurétiques épargneurs de potassium de la classe des anti-aldostérone sont maintenant appelés antagonistes des récepteurs aux minéralocorticoïdes.
Ils s’opposent aux effets délétères de l’aldostérone et diminuent la mortalité en cas d’insuffisance cardiaque chronique et d’insuffisance cardiaque associée à l’infarctus du myocarde. Ils s’opposent, aussi, au remodelage ventriculaire.
Les diurétiques épargneurs de potassium agissent au niveau du tube contourné distal. Ils diminuent la réabsorption du sodium et inhibent la sécrétion de potassium.
Dans l’insuffisance cardiaque, ils ont prouvé leur efficacité en diminuant la mortalité cardiovasculaire.
Les effets secondaires sont l’hyperkaliémie, l’insuffisance rénale aiguë, la gynécomastie.
Ivabradine
L’ivabradine est un composé pharmacologique bradycardisant agissant uniquement sur le nœud sinusal (inhibiteur du courant If), sans action directe sur le système adrénergique. Par cet effet bradycardisant exclusif, l’ivabradine a montré une réduction de la morbimortalité en cas d’insuffisance cardiaque systolique chronique chez le patient en rythme sinusal.
L’ivabradine est utilisée soit en association avec les bêtabloquants, soit seule lorsque ces derniers sont contre-indiqués ou ne sont pas tolérés, à la condition d’avoir éliminé une cardiopathie ischémique sous-jacente.
Resynchronisateur et défibrillateur
Un resynchronisateur cardiaque (pacemaker biventriculaire) doit être proposé aux patients qui restent symptomatiques et qui ont une altération sévère de la fraction d’éjection et un bloc de branche gauche. Les resynchronisateurs améliorent les symptômes, améliorent la capacité d’effort, diminuent la mortalité et réduisent les réhospitalisations.
Un défibrillateur doit être implanté chez les patients considérés comme à risque de mort subite d’origine rythmique en prévention secondaire – quelle que soit la fonction ventriculaire – ou primaire quand la fonction systolique est sévèrement altérée. La fonction « défibrillateur » peut être associée au resynchronisateur cardiaque.
Autres traitements
Si le patient reste symptomatique, d’autres traitements peuvent être ajoutés.
La digoxine est proposée en particulier chez le patient ayant une fibrillation atriale. La digoxine améliore les symptômes et la qualité de vie mais n’a pas d’effet sur la survie. La digoxine exerce un effet inotrope positif modéré et améliore le baroréflexe.
Les dérivés nitrés peuvent améliorer les symptômes. Aux États-Unis, l’association dérivés nitrés-dihydralazine a démontré un effet bénéfique sur la survie des patients insuffisants cardiaques afro-américains, chez qui existe une certaine résistance aux effets des inhibiteurs de l’enzyme de conversion. Cette association n’est pas commercialisée en France à l’heure actuelle.
La réadaptation est importante et permet d’améliorer la qualité de vie et elle a un impact favorable sur la survie quand elle est régulièrement poursuivie.
Les comorbidités (diabète, carence martiale, BPCO, insuffisance rénale, troubles de l’humeur, etc.), la dénutrition seront prises en charge. Un régime pauvre en sel (< 6 g par jour) est conseillé systématiquement.
Les facteurs déclenchant des poussées congestives seront identifiés et traités pour prévenir les récidives (traitements des arythmies, vaccinations, régime, observance, etc.).
Insuffisance cardiaque à FEVG préservée
À l’heure actuelle, il n’existe pas de traitement spécifique de l’insuffisance cardiaque à fraction d’éjection préservée en dehors du traitement des facteurs de risque, des facteurs aggravants (fibrillation atriale, mauvais contrôle de tensionnel, ischémie myocardique, par exemple) et de la prise en charge des symptômes et de la congestion (diurétiques). En effet, aucun traitement, notamment ceux de l’insuffisance cardiaque à fraction d’éjection réduite, n’a prouvé son efficacité dans la baisse de la morbimortalité.
Néanmoins, on utilise classiquement les mêmes traitements que ceux de l’insuffisance cardiaque à FEVG altérée (sauf Entresto®) pour traiter les facteurs de risque et les facteurs aggravants. Les diurétiques sont administrés afin de lutter contre les signes congestifs.
Insuffisance cardiaque avancée
Il est nécessaire d’adresser les patients à des centres de référence d’insuffisance cardiaque pour discuter l’indication de la greffe cardiaque ou d’une assistance circulatoire monoventriculaire gauche, en attente de greffe ou définitive, ou pour proposer une prise en charge palliative quand ces traitements ne sont pas envisageables. La transplantation cardiaque reste le traitement de référence lorsque toutes les possibilités thérapeutiques ont été épuisées chez les patients les plus jeunes (limite autour de 65 ans – en fonction des pathologies associées) symptomatiques en classe 3 ou 4 de la NYHA avec un pronostic menacé à court terme. En France, environ 900 patients sont inscrits sur la liste d’attente nationale mais seulement 450 greffes cardiaques environ sont réalisées. Les progrès techniques réalisés avec les petites pompes axiales et centrifuges permettent d’indiquer ces traitements comme une alternative à la greffe cardiaque. On dispose également de cœurs artificiels totaux indiqués uniquement en attente de transplantation cardiaque et les recherches sur les nouveaux cœurs artificiels totaux en alternative à la greffe sont en cours (programme CARMAT).
Les procédés de thérapie cellulaire et génique en sont encore au stade expérimental et ne sont pas utilisés dans la pratique quotidienne.
De nombreux travaux de recherche clinique et physiopathologique sont en cours pour explorer de nouvelles voies thérapeutiques en particulier en cas d’insuffisance cardiaque à fraction d’éjection ventriculaire gauche préservée.
Organisation du suivi, éducation thérapeutique
L’organisation du suivi ambulatoire des patients ainsi que l’éducation du patient, de sa famille ou de ses aidants sont très importantes. Le traitement est complexe et souvent responsable d’effets secondaires qui gênent l’observance médicale, d’autant plus que le patient est âgé avec des comorbidités. L’éducation thérapeutique permet au patient de composer avec les contraintes de la maladie et de poursuivre une vie sociale, professionnelle et familiale la plus proche de la normale. Elle permet au patient d’acquérir des compétences pour son autoprise en charge, de comprendre et d’appliquer un régime pauvre en sel, de maintenir des activités physiques régulières, d’identifier des signes d’alerte qui l’amèneront à consulter plus tôt et prévenir ainsi des réhospitalisations. Elle peut être réalisée grâce à une approche pluridisciplinaire médicale et paramédicale en réseau de collaborations. La coordination des soins et l’organisation d’un plan personnalisé de soins sont indispensables pour améliorer la prise en charge.
Les programmes de télésuivi du patient insuffisant cardiaque (balance, fréquence cardiaque, saturation, outils d’auto-évaluation de la dyspnée, etc.) en lien avec un accompagnement éducatif sont en cours de développement.
________________________________________________________________________________
Points importants
- L’insuffisance cardiaque est une anomalie de la structure ou de la fonction cardiaque, responsable de l’impossibilité pour le cœur de délivrer l’oxygène et les nutriments de façon adaptée aux besoins métaboliques des tissus à un niveau de pression de remplissage normal.
- L’insuffisance cardiaque est donc l’incapacité du cœur à générer un débit cardiaque suffisant au repos ou à l’effort, pour assurer le transport de la quantité d’oxygène et de nutriments nécessaire au fonctionnement normal de l’organisme.
- La prévalence de l’insuffisance cardiaque est de 1 à 2 % de la population adulte et elle passe à 10 % chez les sujets âgés de plus de 70 ans.
- L’insuffisance cardiaque systolique ou insuffisance cardiaque à fraction d’éjection ventriculaire gauche (FEVG) altérée est liée à une altération de la fonction contractile avec remodelage ventriculaire gauche, dilatation cavitaire et réduction de la fraction d’éjection ventriculaire gauche (< 40 %).
- Elle s’oppose à l’insuffisance cardiaque à FEVG préservée, (> 50 %) de diagnostic plus difficile.
- L’absence de dilatation du VG, la recherche d’une hypertrophie pariétale, d’une dilatation de l’atrium gauche et d’argument pour une altération de remplissage du ventricule gauche participent à ce diagnostic.
- Le remodelage cardiaque concerne quatre niveaux : le ventricule dont les dimensions et le poids sont augmentés ; le myocarde dont les cellules sont altérées ; les cardiomyocytes dont les dimensions et la microstructure architecturale sont altérées et enfin les protéines constitutives des cardiomyocytes.
- Le remodelage physiologique participe à l’adaptation globale de l’organisme et des modifications observées dans des conditions normales (exercice physique, grossesse).
- Lors d’un remodelage physiologique, l’hypertrophie ventriculaire gauche peut être concentrique ou excentrique, mais sans altération de la fonction cardiaque, et sans retentissement sur le pronostic.
- Le remodelage pathologique ou délétère répond à des stimulus hémodynamiques neurohormonaux ou des lésions myocardiques, à l’origine d’une dysfonction cardiaque avec altération de l’hémodynamique intracardiaque.
- Deux grands types de signaux stimulent le remodelage pathologique : la surcharge biomécanique et l’activation neurohormonale, cette dernière visant à maintenir la pression de perfusion des organes et impliquant le système sympathique, le système rénine- angiotensine-aldostérone.
- Le remodelage pathologique cellulaire est complexe, faisant intervenir une hypertrophie des cardiomyocytes, une fibrose tissulaire par prolifération des fibroblastes, une mort cellulaire augmentée (apoptose ou autophagie), aboutissant à une diminution des performances du myocarde, à l’altération du métabolisme énergétique et de la signalisation bêta adrénergique.
- La loi de Frank-Starling indique que l’augmentation du remplissage ventriculaire accentue l’étirement des myocytes cardiaques et augmente la force de la contraction ventriculaire.
- L’activation du système rénine-angiotensine aboutit à la production d’angiotensine 2 et d’aldostérone, en réponse à la sécrétion plasmatique de rénine par les cellules de l’appareil juxtaglomérulaire
- L’angiotensine 2 est un puissant agent vasoconstricteur, stimulant la sécrétion d’aldostérone par la corticosurrénale, favorisant la libération de catécholamines et la prolifération cellulaire.
- L’aldostérone favorise la réabsorption tubulaire de sodium, la perte de potassium, participe au remodelage des cardiomyocytes et est impliquée dans la fibrose interstitielle myocardique.
- Outre l’activation du système sympathique et du système rénine-angiotensine-aldostérone, d’autres facteurs vasoconstricteurs peuvent intervenir : la vasopressine ou hormone antidiurétique et l’endothéline.
- Le système vasodilatateur, qui s’oppose au système vasoconstricteur, comprend les peptides natriurétiques, les prostaglandines et le monoxyde d’azote ou NO.
- La dyspnée d’effort est le principal signe fonctionnel de l’insuffisance cardiaque gauche. Elle doit être quantifiée en utilisant la classification NYHA en quatre classes.
- L’œdème aigu du poumon ou OAP se manifeste comme une détresse respiratoire de survenue brutale et d’évolution spontanée grave surtout en présence d’une cyanose ou d’une hypotension artérielle.
- Les signes radiologiques pleuropulmonaires de l’insuffisance cardiaque comprennent trois stades : le stade 1 correspond à une redistribution vasculaire vers les sommets ; le stade 2 à un œdème interstitiel ; et le stade 3 à un œdème alvéolaire.
- Les signes physiques fréquents de l’insuffisance cardiaque droite sont l’hépatomégalie, le reflux hépatojugulaire, la turgescence jugulaire et surtout les œdèmes déclives.
- Les autres signes de l’insuffisance cardiaque droite, galop droit et souffle d’insuffisance tricuspide sont inconstants.
- L’insuffisance cardiaque droite est le plus souvent la conséquence d’une insuffisance cardiaque gauche.
- L’insuffisance cardiaque globale associe des signes d’insuffisance cardiaque droite et gauche.
- Les deux principales causes d’insuffisance cardiaque sont la maladie coronaire et l’hypertension artérielle.
- Les cardiomyopathies peuvent être classées en dilatée, hypertrophique, restrictive et arythmogène.
- L’origine familiale et la possibilité d’une transmission héréditaire des cardiomyopathies sont à connaître. Parmi les nombreuses mutations pathogènes décrites, les plus fréquentes concernent les gènes qui codent pour des protéines du sarcomère.
- D’autres mutations à l’origine des cardiomyopathies concernent l’altération du codage des protéines qui peuvent conduire à des anomalies multisystémiques avec atteinte cardiaque (par exemple, maladie de Fabry liée à un déficit de l’alpha galactosidase).
- Parmi les marqueurs biologiques classiques, la caractérisation de la fonction rénale, avec le débit de filtration glomérulaire, la natrémie, la kaliémie et le taux d’hémoglobine sont indispensables à l’évaluation de tout patient en insuffisance cardiaque.
- Le dosage des peptides natriurétiques de type B participe de façon déterminante au diagnostic d’insuffisance cardiaque. Devant toute dyspnée, surtout si la cause est indéterminée, un taux sanguin de BNP inférieur à 100 pg/ml exclut à 95 % le diagnostic d’insuffisance cardiaque.
- Le traitement de l’insuffisance cardiaque aiguë repose sur les diurétiques de l’anse et les dérivés nitrés.
- En cas de choc cardiogénique, l’utilisation de molécules bêta 1-adrénergiques (dobutamine) et/ou les inhibiteurs des phosphodiestérases de type 3 (milrinone) sont indiqués.
- L’ordonnance d’un patient traité pour insuffisance cardiaque à FEVG altérée associe un IEC ou un antagoniste des récepteurs de l’angiotensine ou l’association sacubitril-valsartan, un bêtabloquant (bisoprolol, carvédilol), la spironolactone ou un autre inhibiteur des récepteurs minéralocorticoïdes (éplérénone). Les diurétiques de l’anse sont indiqués lors de chaque poussée congestive.
- En cas de persistance de symptôme malgré un traitement médical optimal, à la dose maximale tolérée, une resynchronisation cardiaque par pacemaker biventriculaire doit être discutée, en présence d’un trouble conductif intraventriculaire (QRS > 150 ms).
- La mise en place d’un défibrillateur automatique implantable doit être discutée afin de prévenir le risque de mort subite d’origine rythmique, lorsque la FEVG est altérée, à distance d’un épisode d’ischémie myocardique.
- Il n’y a pas de traitement spécifique à proposer dans l’insuffisance cardiaque à FEVG préservée ; les principes thérapeutiques sont les mêmes que ceux de l’insuffisance cardiaque à FEVG altérée.
- Une approche multidisciplinaire médicale et paramédicale est indispensable dans la prise en charge de l’insuffisance cardiaque, avec une coordination des soins entre les médecines ambulatoire et hospitalière. Des programmes de télésuivi apparaissent de plus en plus utiles.
________________________________________________________________________________
Exercices en ligne
Les exercices relatifs à ce chapitre sont disponibles en ligne à l’adresse suivante : http://www.em-consulte.com/e-complement/475848
Partagez cette publication
Written by : SFC
Plus de publications de la SFC

CARDIOLOGIE PÉDIATRIQUE Pediatric reflex syncope: updated insights and future directions | Lire l'article European Journal of [...]

CARDIOLOGIE PÉDIATRIQUE 📌 À LA UNE : Pediatric reflex syncope: updated insights and future directions | Lire l'article [...]


