Suivez-nous sur les réseaux sociaux !
Publications
Chapitre 22 – Item 330 : Prescription et surveillance des classes de médicaments les plus courantes chez l’adulte et chez l’enfant, hors anti-infectieux. Connaître les grands principes thérapeutiques
I. Antiagrégants plaquettaires
II. Héparines et héparinoïdes
III. Antivitamines K
IV. Anticoagulants oraux directs
V. Thrombolytiques
VI. Accidents des anticoagulants
Situations de départ
10 Méléna/rectorragies.
59 Tendance aux saignements.
60 Hémorragie aiguë.
89 Purpura/ecchymose/hématome.
102 Hématurie.
147 Épistaxis.
199 Créatinine augmentée.
213 Allongement du temps de céphaline activée (TCA).
215 Anomalies des plaquettes.
217 Baisse de l’hémoglobine.
218 Diminution du taux de prothrombine (TP).
248 Prescription et suivi d’un traitement par anticoagulant et/ou antiagrégant.
264 Adaptation des traitements sur un terrain particulier (insuffisant rénal, insuffisant hépatique, grossesse, personne âgée).
272 Prescrire et réaliser une transfusion sanguine.
275 Prise en charge d’une suspicion de thrombophilie.
285 Consultation de suivi et éducation thérapeutique d’un patient avec un antécédent cardiovasculaire.
331 Découverte d’un aléa thérapeutique ou d’une erreur médicale.
352 Expliquer un traitement au patient (adulte/enfant/adolescent).
354 Évaluation de l’observance thérapeutique.
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé |
|---|---|---|
| Prise en charge | Antiagrégants plaquettaires : connaître les mécanismes d’action, indications, effets secondaires, interactions médicamenteuses, modalités de surveillance et principales causes d’échec | |
| Prise en charge | Héparines : connaître les mécanismes d’action, indications, effets secondaires, interactions médicamenteuses, modalités de surveillance et principales causes d’échec | |
| Prise en charge | Anticoagulants oraux (antivitamines K et anticoagulants directs) : connaître les mécanismes d’action, indications, effets secondaires, interactions médicamenteuses, modalités de surveillance et principales causes d’échec |
![]() Le traitement antithrombotique est un atout majeur dans la prise en charge de la maladie athérothrombotique et dans la maladie thromboembolique veineuse. Il a considérablement évolué en quelques années et de nombreuses données scientifiques valident son utilisation dans de nombreuses circonstances.
Le traitement antithrombotique est un atout majeur dans la prise en charge de la maladie athérothrombotique et dans la maladie thromboembolique veineuse. Il a considérablement évolué en quelques années et de nombreuses données scientifiques valident son utilisation dans de nombreuses circonstances.
De façon un peu schématique, on distingue :
• les agents antiplaquettaires qui agissent sur l’hémostase primaire ;
• les anticoagulants qui agissent sur la phase de la coagulation ;
• les fibrinolytiques qui agissent en activant la fibrinolyse, donc la destruction du caillot une fois que celui-ci a été formé.
I Antiagrégants plaquettaires
Les antiagrégants plaquettaires (AAP) sont très utilisés en cardiologie.
Ces médicaments ont pour cible les plaquettes, effecteurs essentiels de la phase d’agrégation plaquettaire qui est une étape clé de la formation d’un caillot artériel.
A Aspirine
L’aspirine est le plus ancien des AAP.
Les médicaments disponibles sont : Aspirine Protect® (cp), Kardégic® (poudre), Aspégic® (poudre), aspirine UPSA® (cp effervescents), etc.
1 Mode d’action
L’aspirine agit en inhibant la cyclo-oxygénase (la Cox 1 et, à un moindre niveau, la Cox 2) (cf. fig. 22.1).
![]() Elle diminue le taux de thromboxane A2 qui est proagrégant.
Elle diminue le taux de thromboxane A2 qui est proagrégant.
Son effet sur la plaquette est irréversible et va durer toute la vie de la plaquette (7–10 jours).
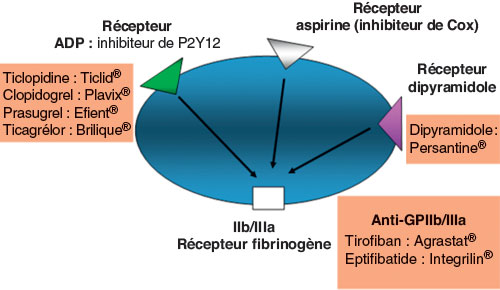
ADP : adénosine diphosphate.
L’aspirine possède de nombreuses autres propriétés :
• des effets antalgique, antipyrétique et anti-inflammatoire à des doses > 1 g/j (chez l’adulte), largement utilisés ;
• un possible effet anticancéreux (essentiellement sur les adénocarcinomes), qui reste débattu.
2 Posologie
![]() Les doses nécessaires pour obtenir l’effet AAP sont bien moindres que celles nécessaires pour obtenir un effet anti-inflammatoire ou antipyrétique.
Les doses nécessaires pour obtenir l’effet AAP sont bien moindres que celles nécessaires pour obtenir un effet anti-inflammatoire ou antipyrétique.
Très récemment 2 doses d’aspirine, 75 et 325 mg, ont été comparées sans que l’une ne l’emporte. En France et en Europe, la dose de 75 mg est la plus utilisée. Une dose de 300 mg est le plus souvent nécessaire en dose d’attaque (cf. tableau 22.1). La dose la plus souvent utilisée pour la prise en charge de la maladie coronarienne et de l’artériopathie des membres inférieurs est de 75–100 mg/j alors que les neurologues utilisent le plus souvent après un AVC 160 mg/j.
L’aspirine est rapidement active per os (quelques dizaines de minutes) mais peut s’administrer par voie IV ou à mâcher.
L’aspirine peut être associée dans le même comprimé avec un autre antiplaquettaire, le clopidogrel (Duoplavin®) lors des premiers mois après un stenting coronarien ou au long cours chez des patients à haut risque thrombotique.
Tableau 22.1 ![]() Posologies de l’aspirine.
Posologies de l’aspirine.
| Dose de charge pour les SCA | Dose d’entretien pour la coronaropathie ou l’AVC | Dose anti-inflammatoire ou antipyrétique |
|---|---|---|
| 250–300 mg | 75–160 mg/j | 500 mg à 2 g/j |
AVC : accident vasculaire cérébral ; SCA : syndrome coronarien aigu.
3 Indications
L’aspirine est indiquée :
• en prévention secondaire de la coronaropathie, de l’artériopathie des membres inférieurs, des AVC. C’est un traitement à vie, en l’absence d’effets indésirables ou de complications ;
• en prévention primaire de la coronaropathie et des AVC chez les sujets à haut risque vasculaire. Cette indication est de plus en plus discutée car le bénéfice ischémique est contrebalancé par un risque hémorragique, non négligeable.
4 Surveillance
Il n’existe pas de test biologique fiable et utilisable en routine pour surveiller l’efficacité de l’aspirine. La bonne tolérance clinique est évaluée par la recherche d’hémorragie extériorisée et une numération formule au moins annuelle.
5 Effets indésirables essentiels
Ils sont représentés par les saignements et les intolérances gastriques, raison pour laquelle on associe de plus en plus fréquemment une protection gastrique (inhibiteur de la pompe à protons) dans les situations à risque.
De très rares « allergies » peuvent exister. Leur suspicion est beaucoup plus fréquente que les formes avérées. Le syndrome de Widal associe asthme, polypose nasale et allergie à l’aspirine.
6 Situations à risque hémorragique et aspirine
En cas d’arrêt de l’aspirine justifié par la crainte d’une hémorragie, il existe un risque d’évènement athérothrombotique.
| Grandes règles de la bonne gestion du traitement antiplaquettaire • Après implantation d’un stent coronarien, il faut retarder au minimum de 6 semaines (en cas de stent nu) et de 3–6 mois (en cas de stent actif) tout acte invasif non urgent à risque hémorragique. • Pour de très nombreux actes à risque hémorragique modéré (chirurgie/fibroscopie/biopsie, etc.), il est préférable de ne pas arrêter l’aspirine. De nombreuses conférences de consensus existent dans chaque spécialité concernée (chirurgiens-dentistes/rhumatologues/gastro-entérologues, etc.) qui acceptent cette règle. • Quand le risque hémorragique est très important (chirurgie ORL, urologique, neurologique), l’aspirine ne doit être arrêtée que sur une courte durée : 5 jours et reprise le plus tôt possible après l’acte. |
B Thiénopyridines et ticagrélor
Les médicaments disponibles sont les suivants : ticlopidine (Ticlid®), clopidogrel (Plavix®), prasugrel (Efient®) et ticagrélor (Brilique®).
1 Mode d’action
Il s’agit d’une classe d’AAP qui agit en bloquant la voie de l’ADP (cf. fig. 22.1) par blocage d’un récepteur plaquettaire appelé P2Y12, donc par un mode d’action différent de celui de l’aspirine.
Les effets des médicaments de cette classe sont additifs à ceux de l’aspirine.
![]() Ils ont permis d’incontestables progrès dans les situations à haut risque de thrombose, en particulier coronarienne.
Ils ont permis d’incontestables progrès dans les situations à haut risque de thrombose, en particulier coronarienne.
• La ticlopidine, molécule la plus ancienne, n’est pratiquement plus utilisée du fait d’effets indésirables hématologiques graves (agranulocytose) qui nécessitaient la surveillance de la NFS.
• Le clopidogrel a été longtemps le chef de file de cette classe. Il s’agit d’une prodrogue. C’est son métabolite qui est actif. Son métabolisme passe par la voie du cytochrome P450 et en particulier par le CYP2C19. Chez 15 à 25 % des patients, le métabolisme du clopidogrel se fait mal et le médicament n’est pas ou est trop peu actif. Par ailleurs, certains médicaments qui interfèrent avec le CYP peuvent limiter son effet.
• Le prasugrel est aussi un inhibiteur du récepteur P2Y12.
• Le ticagrélor fait partie d’une famille voisine (cyclo-pentyl-triazolo-pyrimidines) mais agit aussi comme un antagoniste sélectif du récepteur P2Y12 de l’ADP. Il ne nécessite pas de métabolisation pour être actif. Son effet serait réversible.
![]() Prasugrel et ticagrélor ont un effet antiplaquettaire plus puissant et plus rapide que le clopidogrel : en moyenne 70 à 80 % d’inhibition plaquettaire contre 40 à 50 % pour le clopidogrel.
Prasugrel et ticagrélor ont un effet antiplaquettaire plus puissant et plus rapide que le clopidogrel : en moyenne 70 à 80 % d’inhibition plaquettaire contre 40 à 50 % pour le clopidogrel.
2 Posologies (cf. tableau 22.2)
• ![]() Le clopidogrel est donné à une dose de charge de 300 à 600 mg (cp à 300 mg) puis, le plus souvent, à des posologies quotidiennes de 75 mg en 1 prise/j (cp à 75 mg).
Le clopidogrel est donné à une dose de charge de 300 à 600 mg (cp à 300 mg) puis, le plus souvent, à des posologies quotidiennes de 75 mg en 1 prise/j (cp à 75 mg).
• Le prasugrel est donné à une dose de charge de 60 mg/j puis à 10 mg/j en 1 prise/j (cp à 10 mg ; des cp à 5 mg existent dans de nombreux pays mais pas en France).
• Le ticagrélor est prescrit à 180 mg en dose de charge puis en 2 prises/j à 90 mg matin et soir.
La durée de traitement est précisée dans le tableau 22.3.
Tableau 22.2 ![]() Posologies des thiénopyridines et du ticagrélor.
Posologies des thiénopyridines et du ticagrélor.
| Molécule | Dose de charge | Dose d’entretien | Nombre de prises/jour |
|---|---|---|---|
| Clopidogrel | 300–600 mg | 75 mg | 1 |
| Prasugrel | 60 mg | 10 mg | 1 |
| Ticagrélor | 180 mg | 90 mg × 2 | 2 |
Tableau 22.3 ![]() Durée du traitement antiplaquettaire chez le patient coronarien.
Durée du traitement antiplaquettaire chez le patient coronarien.
| Aspirine | Le plus souvent à vie |
| Clopidogrel, ticagrélor | Le plus souvent en association avec l’aspirine pour une période 1 à 12 mois (classiquement 12 mois) mais certains patients peuvent en bénéficier au-delà des 12 mois |
| Prasugrel | Le plus souvent en association avec l’aspirine pour une période de 1 à 12 mois |
3 Indications
![]() Les indications de chacun de ces AAP sont inhérentes aux études cliniques qui ont été conduites et qui ont pu démontrer un intérêt. Toutes ses molécules ne sont pas « interchangeables ». Ces indications sont évolutives.
Les indications de chacun de ces AAP sont inhérentes aux études cliniques qui ont été conduites et qui ont pu démontrer un intérêt. Toutes ses molécules ne sont pas « interchangeables ». Ces indications sont évolutives.
• Le clopidogrel est indiqué dans les SCA (quand le prasugrel et le ticagrélor ne sont pas indiqués ou après une fibrinolyse) et après angioplastie coronarienne, chez les patients présentant un syndrome coronarien chronique (angor stable) en association avec l’aspirine, pour une durée de 3 à 12 mois, selon l’indication.
![]() Mais quelques patients (haut risque de récidive/faible risque hémorragique) peuvent en bénéficier sur du plus long terme. Il peut remplacer l’aspirine lorsque cette dernière est mal tolérée mais des indications de remplacement abusives trop nombreuses sont à l’origine d’une surveillance particulière par les caisses d’assurance maladie (prix de l’aspirine : 0,10 €/j, prix du clopidogrel 0,80 €/j).
Mais quelques patients (haut risque de récidive/faible risque hémorragique) peuvent en bénéficier sur du plus long terme. Il peut remplacer l’aspirine lorsque cette dernière est mal tolérée mais des indications de remplacement abusives trop nombreuses sont à l’origine d’une surveillance particulière par les caisses d’assurance maladie (prix de l’aspirine : 0,10 €/j, prix du clopidogrel 0,80 €/j).
• ![]() Le prasugrel est indiqué dans les SCA, en association à l’aspirine, chez les patients qui ont été traités par angioplastie.
Le prasugrel est indiqué dans les SCA, en association à l’aspirine, chez les patients qui ont été traités par angioplastie.
• Le ticagrélor est indiqué dans les SCA, en association à l’aspirine.
![]() Il l’est également chez certains coronariens stables au-delà d’un an.
Il l’est également chez certains coronariens stables au-delà d’un an.
![]() Dans le SCA, clopidogrel, prasugrel ou ticagrélor sont associés à l’aspirine pendant une durée classiquement de 12 mois mais qui dépend aussi du risque hémorragique (de 1 à 12 mois). Plus le risque hémorragique est élevé, plus la durée de la double antiagrégation est réduite (exemple du SCANST, cf. fig. 22.2).
Dans le SCA, clopidogrel, prasugrel ou ticagrélor sont associés à l’aspirine pendant une durée classiquement de 12 mois mais qui dépend aussi du risque hémorragique (de 1 à 12 mois). Plus le risque hémorragique est élevé, plus la durée de la double antiagrégation est réduite (exemple du SCANST, cf. fig. 22.2).
Les combinaisons des traitements antithrombotiques dans le post-SCA sont définies par des recommandations européennes.
4 Surveillance
![]() Il n’existe pas de test biologique fiable utilisable en routine pour surveiller l’efficacité des thiénopyridines ou du ticagrélor.
Il n’existe pas de test biologique fiable utilisable en routine pour surveiller l’efficacité des thiénopyridines ou du ticagrélor.
5 Précautions et effets indésirables
Contre-indication absolue
Le prasugrel expose à un risque hémorragique cérébral qui le contre-indique chez les sujets ayant des ATCD d’accident cérébral (hémorragique ou ischémique).
Contre-indications relatives
Les sujets de moins de 60 kg et ceux de plus de 75 ans étant les plus susceptibles de saigner, ils représentent une contre-indication relative au prasugrel.
L’effet adénosine du ticagrélor par lequel le médicament est actif peut être responsable de dyspnée gênante (jusqu’à 18 % des patients) et de bradycardie, réversible à son arrêt.
Fig. 22.2 ![]() Stratégie antithrombotique dans le syndrome coronarien aigu sans sus-décalage du segment ST (SCANST) sans nécessité de traitement anticoagulant.
Stratégie antithrombotique dans le syndrome coronarien aigu sans sus-décalage du segment ST (SCANST) sans nécessité de traitement anticoagulant.
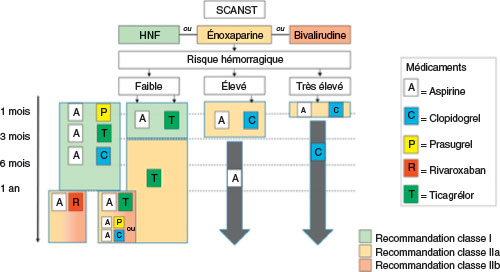
HNF : héparine non fractionnée.
© Collet JP, Thiele H, Barbato E, Barthélémy O, Bauersachs J, Bhatt DL, et al. ; ESC Scientific Document Group. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J. 2021 ; 42 (14) : 1289–367.
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
C Anti-GPIIb/IIIa
![]() Ce sont les médicaments suivants : eptifibatide (Integrilin®), tirofiban (Agrastat®).
Ce sont les médicaments suivants : eptifibatide (Integrilin®), tirofiban (Agrastat®).
La glycoprotéine IIb/IIIa est un récepteur de la plaquette qui permet son adhésion au fibrinogène (constituant une des phases essentielles d’élaboration du thrombus) (cf. fig. 22.1). Les anti-GPIIb/IIIa bloquent ce récepteur.
Ces traitements efficaces ne sont utilisés que par voie veineuse sur de très courtes périodes.
Ils sont réservés à des conditions très spécifiques, en particulier en salle d’angioplastie lors des dilatations coronariennes à haut risque de thrombose, et sont de moins en moins utilisés depuis l’avènement des nouveaux AAP.
Le risque hémorragique est important.
L’abciximab est responsable de thrombopénies (4 %).
Leur coût est élevé.
II Héparines et héparinoïdes
A Médicaments
![]() On distingue :
On distingue :
• l’héparine standard non fractionnée (HNF) : héparine IV et héparine calcique (Calciparine®, voie SC – sous-cutanée) ;
• les héparines de bas poids moléculaire (HBPM) : énoxaparine (Lovenox®), tinzaparine (Innohep®), nadroparine (Fraxiparine®), daltéparine (Fragmine®) qui correspondent à une fraction plus réduite de la chaîne d’héparine ;
• des « apparentés » comme le fondaparinux (Arixtra®), le danaparoïde (Orgaran®) ou la bivalirudine.
B Mode d’action – Pharmacologie (cf. tableau 22.4)
![]() L’HNF et les HBPM agissent en activant un anticoagulant physiologique présent dans le sang qui est l’antithrombine.
L’HNF et les HBPM agissent en activant un anticoagulant physiologique présent dans le sang qui est l’antithrombine.
Le fondaparinux est un anti-Xa.
Après injection IV, l’effet anticoagulant de l’HNF est immédiat. La demi-vie de l’HNF est de l’ordre de 1 h 30 (cette notion permet de gérer les doses sur 24 heures). Le maintien de l’activité anticoagulante désirée est donc obtenu soit en perfusant l’HNF en continu (seringue autopousseuse), soit en pratiquant plusieurs injections dans le nycthémère (× 2 ou × 3 pour l’héparine calcique).
Les HBPM, qui ont une demi-vie plus longue, s’administrent en SC en 1 ou 2 fois/j en fonction de leur demi-vie. Un bolus pour obtention d’un effet anticoagulant immédiat peut se faire par voie IV.
Le fondaparinux, qui a une demi-vie longue, s’administre en IV ou en SC 1 seule fois/j.
L’HNF est éliminée, en grande partie, par une fixation sur les protéines, les cellules endothéliales et les macrophages et pour une petite partie par le rein alors que les HBPM et le fondaparinux sont essentiellement éliminés par le rein.
L’HNF est le seul anticoagulant utilisable dans les insuffisances rénales sévères (clairance de la créatinine = ClCr < 20–30 mL/min).
Tableau 22.4 ![]() Pharmacologie des héparines et héparinoïdes.
Pharmacologie des héparines et héparinoïdes.
| Action par antithrombine | Élimination par le rein | Demi-vie | Antidote | |
|---|---|---|---|---|
| HNF | Oui | + | 1 h 30 | Sulfate de protamine |
| HBPM | Oui | +++ (CI si ClCr < 30 mL/min) |
8 à 24 heures | En cours de développement |
| Fondaparinux | Non | +++ (CI si ClCr < 30 mL/min) |
17–21 heures | En cours de développement |
HBPM : héparine de bas poids moléculaire ; HNF : héparine non fractionnée ; CI : contre-indication ; ClCr : clairance de la créatinine.
Les HBPM ainsi que le fondaparinux sont plutôt contre-indiqués lorsque la ClCr est inférieure à 30 mL/min. Des règles d’utilisation récentes autorisent l’énoxaparine lorsque la ClCr est inférieure à 30 mL/min.
Pour l’héparine standard, il existe un antidote, le sulfate de protamine, qui doit être administré par voie intraveineuse. Il neutralise instantanément l’action de l’héparine non fractionnée.
C Posologie
Les posologies curatives de l’héparine standard pour obtenir un effet anticoagulant rapide (bolus) sont de 80 UI/kg (environ 5 000 UI en bolus pour un poids de 70 kg), puis de 18 UI/kg/h (environ 500 UI/kg/j, soit 30 000 UI/24 h à la seringue autopousseuse).
Les posologies curatives des HBPM sont fonction du poids du sujet (100 U anti-Xa/kg), par exemple 0,8 mL × 2 pour l’énoxaparine pour un poids de 80 kg, ce qui implique de connaître le poids du malade avec la plus grande précision.
D Surveillance
L’effet thérapeutique de l’HNF se mesure par le temps de céphaline activée (TCA) qui doit être prolongé de 2 à 3 fois par rapport à celui du témoin et/ou par l’activité anti-Xa (entre 0,5 et 0,8/mL).
Le premier TCA doit être fait vers la 5e heure après l’instauration du traitement.
Les doses d’héparine sont adaptées par rapport à ce TCA qui doit être surveillé au moins une fois par jour. Puis les doses sont adaptées selon le schéma du tableau 22.5.
Sauf exception, l’activité thérapeutique des HBPM n’a pas besoin d’être mesurée si elle est prescrite de façon correcte en fonction du poids et en l’absence d’insuffisance rénale.
Tableau 22.5 Ajustement des doses d’héparine IV.
| TCA (s) | Dose de charge (UI/24 h) | Action supplémentaire |
|---|---|---|
| < 45 | + 6 000 | Bolus 5 000 U |
| 46–54 | + 3 000 | / |
| 55–85 | 0 | / |
| 86–110 | –3 000 | Stop SAP 1 h |
| > 110 | –6 000 | Stop SAP 1 h |
SAP : seringue autopousseuse ; TCA : temps de céphaline activée.
E Indications
Les héparines sont des anticoagulants d’action rapide, utilisés dans toutes situations où une anticoagulation urgente est nécessaire, soit :
• thromboses veineuses profondes et embolie pulmonaire ;
• troubles du rythme nécessitant un traitement anticoagulant, le plus souvent en attente de l’efficacité des anticoagulants oraux ;
• syndrome coronarien aigu.
Les HBPM sont largement utilisées en prévention de la thrombose veineuse en contexte chirurgical ou médical à risque thromboembolique.
F Effets indésirables
Le principal effet indésirable lié à l’effet recherché reste les complications hémorragiques.
Les thrombopénies induites par l’héparine (TIH) (cf. VI. Accidents des anticoagulants) sont une complication classique mais rare de l’héparinothérapie, il s’agit d’un phénomène immunoallergique.
![]() Une ostéoporose, une alopécie, une élévation des transaminases, un priapisme, une insuffisance surrénalienne aiguë sont des complications rares mais possibles des héparines.
Une ostéoporose, une alopécie, une élévation des transaminases, un priapisme, une insuffisance surrénalienne aiguë sont des complications rares mais possibles des héparines.
G Héparinoïdes et apparentés
1 Danaparoïde : Orgaran®
Il est essentiellement utilisé chez les patients présentant ou ayant présenté une TIH et qui ont besoin de traitement anticoagulant.
Le principe est de substituer l’héparine, qui a induit la TIH, par un autre anticoagulant SC ou IV non allergisant afin de couvrir la période à risque de complications thrombotiques et/ou en attendant l’efficacité des AVK (antivitamines K) qui auraient été introduites.
2 Bivalirudine
C’est un anticoagulant IV essentiellement utilisé lors des angioplasties coronariennes. Ce médicament est très peu utilisé en France.
III Antivitamines K
A Médicaments
![]() Les antivitamines K sont des anticoagulants administrables par voie orale et utilisables pour des traitements de longue durée.
Les antivitamines K sont des anticoagulants administrables par voie orale et utilisables pour des traitements de longue durée.
• Le plus utilisé dans le monde est la warfarine (Coumadine®) qui devrait rester l’AVK de référence.
• La fluindione (Préviscan®) est très utilisée en France, mais son instauration est déconseillée par l’ANSM (Agence nationale de sécurité du médicament et des produits de santé) depuis 2017 en raison d’un risque immunoallergique rare mais grave d’insuffisance rénale. Ces complications surviennent en règle dans les 6 mois, aussi il n’est pas recommandé de remplacer la fluindione chez des patients bien équilibrés depuis longtemps.
• L’acénocoumarol (Sintrom®) doit s’administrer en 2 fois/j et n’est pas l’AVK recommandée.
B Mode d’action
Les antivitamines K bloquent au niveau hépatique la synthèse des facteurs II – VII – IX et X de la coagulation. Ils inhibent aussi la synthèse de la protéine C et de la protéine S qui sont deux anticoagulants physiologiques circulants (cf. tableau 22.6).
Tableau 22.6 ![]() Propriétés des facteurs de coagulation inhibés par les antivitamines K.
Propriétés des facteurs de coagulation inhibés par les antivitamines K.
| Facteurs vitamine K-dépendants | Demi-vie (h) | |
|---|---|---|
| II | Prothrombine | 50–120 |
| VII | Proconvertine | 4–6 |
| IX | Hémophilie B | 24 |
| X | Stuart | 36–48 |
| Protéine C | 6–10 | |
| Protéine S | 40 | |
Les AVK ont un délai d’action long, inhérent à la longue demi-vie de certains cofacteurs vitamine K-dépendants. Leur pleine efficacité nécessite donc 3 à 5 jours de prise.
La warfarine (Coumadine®) et la fluindione (Préviscan®) sont des AVK de demi-vie longue. Ceci n’est pas un inconvénient pour leur équilibre. L’acénocoumarol (Sintrom®) est une AVK de demi-vie courte (cf. tableau 22.7).
Tableau 22.7 ![]() Pharmacologie des principaux médicaments antivitamines K.
Pharmacologie des principaux médicaments antivitamines K.
| Molécule – Nom commercial | Demi-vie (h) | Durée de l’effet (h) | Dosage des cp (mg) |
|---|---|---|---|
| Warfarine Coumadine® |
35–45 | 96–120 | 2 et 5 |
| Fluindione Préviscan® |
30 | 48 | 20 |
| Acénocoumarol | 8–9 | 36–48 | |
| Sintrom® | 4 | ||
| Mini-Sintrom® | 1 |
C Relais héparine – AVK
Les AVK ne pouvant être efficaces rapidement, elles doivent être dans la majorité des cas précédées par un traitement par héparine (HNF, HBPM ou fondaparinux).
Sauf exception, l’introduction de l’AVK doit se faire précocement dès J1, sachant qu’elle n’est pas effective avant 4 à 6 jours (cf. fig. 22.3).
Cette introduction précoce de l’AVK permet de :
• raccourcir la durée du chevauchement par héparine, et donc l’hospitalisation ;
• diminuer l’incidence des TIH.
Les deux conditions d’arrêt de l’héparine sont :
• au moins 4 à 5 jours de chevauchement ;
• 2 INR (International Normalized Ratios) efficaces à 24 heures d’intervalle.
Fig. 22.3 ![]() Bonne conduite du traitement anticoagulant dans l’embolie pulmonaire.
Bonne conduite du traitement anticoagulant dans l’embolie pulmonaire.
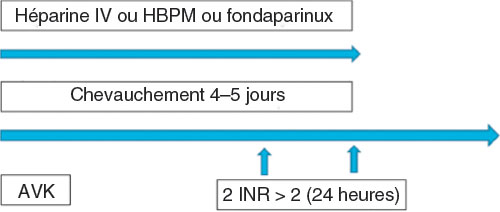
AVK : antivitamine K ; HBPM : héparine de bas poids moléculaire ; INR : International Normalized Ratio ; IV : intraveineux.
D Surveillance au long cours
La surveillance de l’effet thérapeutique des AVK se fait par la mesure de l’INR. L’INR est le rapport des temps de Quick témoin/patient et prend en compte l’indice du réactif utilisé (thromboplastine) ; il a remplacé le TP (taux de prothrombine), trop aléatoire. La valeur normale sans traitement de l’INR est de 1, la valeur cible de l’INR pour un patient qui est correctement anticoagulé par AVK se situe pour la plupart des indications entre 2 et 3. Il existe de rares indications où l’INR doit être plus élevé mais ceci est du domaine des spécialistes (prothèses valvulaires mécaniques en position mitrale par exemple).
La surveillance de l’INR doit être très rigoureuse lors de l’instauration du traitement afin d’éviter un sous et surtout un surdosage. Elle est espacée au fur et à mesure de l’équilibration du traitement puis doit se faire au minimum 1 fois/mois lors des traitements au long cours (cf. fig. 22.4).
On dit qu’un patient est correctement équilibré lorsqu’au moins 70 % de ses INR sont dans la cible fixée.
Une éducation thérapeutique pour faire participer le malade à son traitement est indispensable (éviter les coprescriptions, connaître les seuils d’alerte des résultats d’INR, faire appel en cas de saignement, prévenir tout médecin de ce traitement au long cours, etc.).
La surveillance des INR peut se faire par des appareils d’automesures (très semblables à ceux de la glycémie) : Coagucheck® INRange, etc. En France, la prise en charge (remboursement) n’est établie que pour les enfants et chez les porteurs de valves mécaniques.
Les AVK possèdent deux antidotes qui sont :
• le PPSB (initiale des 4 facteurs de la coagulation vitamine K-dépendants déprimés par les AVK) qui agit très rapidement ;
• la vitamine K qui antagonise leurs effets en quelques heures.
Les AVK sont tératogènes et donc contre-indiquées lors de la première partie du 1er trimestre de la grossesse.
Fig. 22.4 ![]() Fréquence de surveillance des INR (International Normalized Ratios).
Fréquence de surveillance des INR (International Normalized Ratios).
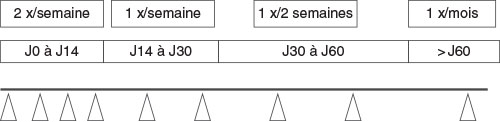
E Posologie
Il n’existe pas de dose prédéfinie pour obtenir l’efficacité thérapeutique recherchée.
La dose de départ est une dose « d’approche » qui doit être plus faible chez les personnes âgées.
Les AVK sont très liées aux protéines plasmatiques.
Le métabolisme des AVK peut être accéléré ou ralenti par d’autres coprescriptions.
Certaines coprescriptions sont strictement contre-indiquées telles que le miconazole (Daktarin®).
| Exemple de la warfarine Posologie Coumadine® 5 mg : boîte bleue, cp bisécables Coumadine® 2 mg : boîte rose, cp bisécables pour adaptation posologique – 1re prise J0 : 1 cp (soit 5 mg) le soir – 2e prise J1 : 1 cp (soit 5 mg) le soir – 3e prise J2 : 1 cp (soit 5 mg) le soir Adaptations posologiques (INR cible entre 2,0 et 3,0) • 1er contrôle impératif le matin de J4 (lendemain de la 3e prise) pour adapter la 4e prise du soir : – INR < 1,3 augmenter la posologie à 8 mg – 1,3 ≤ INR < 1,5 augmenter la posologie à 7 ou 6 mg – 1,5 ≤ INR < 1,75 pas de modification à 5 mg – 1,75 ≤ INR < 2 diminuer la posologie à 4 ou 3 mg – 2 ≤ INR < 2,5 diminuer la posologie à 3 ou 2,5 mg – INR ≥ 2,5 saut d’une prise (à adapter), puis 2,5 mg • 2e contrôle à J6 ± 1 : – INR ≤ 1,6 augmenter la posologie de 30 à 20 % – 1,6 < INR ≤ 2,5 continuer sans modifier la posologie – 2,5 < INR ≤ 3,5 diminuer la posologie de 20 à 40 % – INR ≥ 3,5 cf. infra B. Accidents hémorragiques liés aux antivitamines K • Contrôles suivants : toutes les 48 à 72 heures, jusqu’à l’obtention de l’équilibre (2 INR successifs entre 2,0 et 3,0). Si INR < 2, augmenter la posologie de 10 %, attendre une semaine pour décider d’une nouvelle augmentation. |
F Indications
Les AVK sont indiquées :
• dans la fibrillation atriale ;
• dans le traitement et la prévention des TVP et de l’EP ;
• chez les patients porteurs de valve cardiaque mécanique ;
• pour certaines complications de l’infarctus du myocarde (anévrisme du ventricule gauche, thrombus) ou de l’insuffisance cardiaque.
En dehors des porteurs de valves mécaniques et de l’insuffisance rénale sévère, les AOD (cf. infra) se substituent de plus en plus et sont préférés aux AVK.
G Situations à risque hémorragique
Les patients traités par AVK peuvent avoir besoin de bénéficier d’un geste à risque hémorragique.
Dans ces conditions, les règles sont les suivantes (cf. tableau 22.8) :
Tableau 22.8 ![]() Conduite à tenir pour des actes programmés à risque hémorragique chez des patients sous antivitamines K.
Conduite à tenir pour des actes programmés à risque hémorragique chez des patients sous antivitamines K.
| Actes programmés nécessitant l’interruption des AVK (objectif : INR au moment de l’intervention < 1,5 ou < 1,2 si neurochirurgie) |
|
|---|---|
| FA sans antécédent embolique MTEV à risque modéré |
Valves mécaniques (tout type) FA avec antécédent embolique MTEV à haut risque1 |
| Arrêt des AVK sans relais préopératoire par héparine Reprise des AVK dans les 24–48 heures ou, si elle n’est pas possible, héparine à dose curative si le risque hémorragique est contrôlé2 |
Arrêt des AVK et relais préopératoire par héparine à dose curative Reprise des AVK dans les 24–48 heures ou, si elle n’est pas possible, héparine à dose curative si le risque hémorragique est contrôlé2 |
AVK : antivitamine K ; EP : embolie pulmonaire ; FA : fibrillation atriale ; INR : International Normalized Ratio ; MTEV : maladie thromboembolique veineuse ; TVP : thrombose veineuse profonde.
1TVP proximale et/ou EP < 3 mois, MTEV récidivante idiopathique (n ≥ 2, au moins un accident sans facteur déclenchant). La mise en place d’un filtre cave en préopératoire est discutée au cas par cas.
2L’héparinothérapie à dose curative ne doit pas être reprise avant la 6e heure postopératoire. Si le traitement par héparine à dose curative n’est pas repris à la 6e heure, dans les situations où elle est indiquée, la prévention postopératoire précoce de la MTEV doit être réalisée selon les modalités habituelles.
HAS. Prise en charge des surdosages en antivitamines K, des situations à risque hémorragique et des accidents hémorragiques chez les patients traités par antivitamines K en ville et en milieu hospitalier. Synthèse des recommandations professionnelles, avril 2008. Nous remercions la Haute Autorité de santé de nous avoir autorisés à reproduire ce tableau. Il est également consultable sur le site www.has-sante.fr rubrique Toutes nos publications.
• la plupart des gestes à risque hémorragique modéré peuvent se faire sans interruption de l’AVK (petite chirurgie/soins dentaires/certaines ponctions-biopsies, etc.) en vérifiant préalablement que l’INR soit dans la limite basse de la fourchette ;
• lorsque le risque hémorragique est plus important, on peut :
• arrêter l’AVK pendant 3 à 4 jours afin de tendre à normaliser l’INR le jour de la procédure et reprendre le traitement le soir même. Ceci est indiqué pour une TVP ou une EP au-delà du 3e mois du traitement ou pour une FA à faible risque embolique,
• faire un relais par héparine en arrêtant l’AVK 4 à 5 jours avant et en le reprenant après l’acte (sous couverture par héparine le temps que l’INR soit efficace). Ceci est indiqué pour une TVP ou une EP récente (< 3 mois), pour une FA à risque embolique élevé ou chez les porteurs de valves mécaniques ;
• les relais par héparines, s’ils peuvent paraître rassurants, sont en fait source de complications tant hémorragiques que thrombotiques.
IV Anticoagulants oraux directs
A Mode d’action
Les anticoagulants oraux directs sont des antithrombotiques qui inhibent soit le facteur II (anti-IIa), soit le facteur X (anti-Xa).
Leur développement a été favorisé par les difficultés de la gestion des AVK.
B Médicaments
Actuellement, trois de ces nouveaux anticoagulants oraux sont disponibles en France : le dabigatran (Pradaxa®), le rivaroxaban (Xarelto®), l’apixaban (Eliquis®) (cf. tableau 22.9).
Tableau 22.9 ![]() Propriétés des anticoagulants oraux directs.
Propriétés des anticoagulants oraux directs.
| DCI | Dabigatran | Rivaroxaban | Apixaban |
| Spécialité | Pradaxa® | Xarelto® | Eliquis® |
| Dosages (mg) | 75, 110, 150 | 10, 15, 20 | 2,5, 5 |
| Activité | Anti-lla | Anti-Xa | Anti-Xa |
DCI : dénomination commune internationale.
Leur élimination rénale est respectivement de 80 % pour le dabigatran, de 33 % pour le rivaroxaban, et de 25 % pour l’apixaban. Il est capital de s’enquérir de la fonction rénale du sujet pour une bonne prescription.
Une accumulation peut rapidement se produire en cas d’insuffisance rénale. L’évaluation de la fonction rénale (par la formule de Cockcroft) est un impératif à l’institution du traitement puis régulièrement dans le suivi. Il est interdit ou déconseillé de les prescrire quand la clairance de la créatinine en Cockcroft est inférieure à 30 à 25 mL/min.
Le nombre de prises par jour diffère en fonction de leur demi-vie et des indications : 2 fois/j pour le dabigatran et l’apixaban, 1 fois/j pour le rivaroxaban dans la plupart des indications mais 2 fois/j en début de traitement de la TVP ou de l’EP et dans le traitement de la coronaropathie.
Des interférences médicamenteuses existent avec tous les AOD et doivent être connues, d’autant plus qu’il n’y a pas, contrairement aux AVK, de moyen biologique simple de quantifier une variation de leur effet thérapeutique.
L’efficacité de ces AOD est rapide (environ 2 heures après la 1re ingestion).
Un patient vu en consultation pour une indication établie (TVP ou EP ou FA) peut recevoir le médicament et est, de fait, tout de suite anticoagulé efficacement, sans nécessité de relais par héparine. Il s’agit d’un bouleversement de l’institution d’un traitement anticoagulant qui ne doit pour autant pas faire galvauder leurs indications.
C Surveillance
Il n’existe pas actuellement de test biologique pour vérifier l’efficacité thérapeutique des anticoagulants oraux. Mais ces médicaments ont été validés sans test. Le dosage du médicament est possible mais est réservé à la gestion des situations hémorragiques (patient sous AOD qui présente un saignement grave) ou à risque hémorragique (patient sous AOD qui doit bénéficier en urgence d’un acte avec risque hémorragique).
La plupart des tests de coagulation standards (TCA/TP/INR, etc.) sont perturbés par la prise d’un AOD. Ceci est important à savoir pour éviter de fausses interprétations. Ces tests usuels ne peuvent pas servir à connaître l’efficacité d’un traitement par AOD (cf. tableau 22.10).
Tableau 22.10 ![]() Généralités sur les AOD – Influence des anticoagulants sur les tests de coagulation.
Généralités sur les AOD – Influence des anticoagulants sur les tests de coagulation.
| AVK | Dabigatran | Rivaroxaban | Apixaban | |
|---|---|---|---|---|
| INR | ↑ ↑ ↑ | ↑ | ↑ | Effet très limité |
| TCA (ratio) | ↑ | ↑ | ↑ | N |
| TT (ratio) | Effet très limité | ↑ ↑ ↑ | Aucune influence | Aucune influence |
| Anti-Xa (UI/mL) | Effet très limité | Aucune influence | ↑ ↑ | ↑ ↑ |
AVK : antivitamine K ; INR : International Normalized Ratio ; TCA : temps de céphaline activée, TT : temps de thrombine.
Un antidote spécifique existe déjà pour le dabigatran (idarucizumab : Praxbind®) et est en cours de commercialisation pour les anti-Xa.
Les AOD sont comparés aux AVK dans le tableau 22.11.
Tableau 22.11 ![]() Avantages et inconvénients des AOD par rapport aux AVK.
Avantages et inconvénients des AOD par rapport aux AVK.
| Avantages des AOD versus AVK | Inconvénients des AOD versus AVK |
|---|---|
| Action rapide per os | Accumulation possible si insuffisance rénale |
| Pas de surveillance biologique de l’effet thérapeutique | Vérification difficile de l’observance |
| Beaucoup moins d’hémorragies globales et surtout intracrâniennes | Un peu plus d’hémorragies digestives et génitales |
| Simplicité d’instauration du traitement |
AOD : anticoagulant oral direct ; AVK : antivitamine K.
D Indications et posologies
Les indications actuelles sont différentes en fonction de chaque molécule et évolutives.
Les posologies sont très variables en fonction de chaque indication (cf. tableau 22.12).
Il est important de savoir que les valves cardiaques mécaniques sont une contre-indication absolue à l’usage des AOD ainsi que le RM serré. En revanche, en situation de FA, toute autre valvulopathie associée n’est pas une contre-indication aux AOD (évolution par rapport à l’indication initiale des AOD dans la « FA dite non valvulaire »).
Tableau 22.12 ![]() Propriétés, posologies et indication des anticoagulants oraux directs.
Propriétés, posologies et indication des anticoagulants oraux directs.
| Dabigatran Pradaxa® |
Rivaroxaban Xarelto® |
Apixaban Eliquis® |
|
|---|---|---|---|
| Mode d’action | Anti-IIa | Anti-Xa | Anti-Xa |
| Élimination rénale (%) | 80 | 33 | 25 |
| Posologie en prévention TVP-EP en orthopédie | 110 mg × 2/j ou 75 mg × 2/j |
10 mg × 1/j | 2,5 mg × 2/j |
| Posologie pour la FA « non valvulaire »1 | 110 ou 150 mg × 2/j (adapter sur fonction rénale et âge) |
15 ou 20 mg/j × 1/j (adapter sur fonction rénale et âge) |
2,5 ou 5 mg × 2/j (adapter sur fonction rénale, âge et poids) |
| Posologie pour la TVP-EP | 110 ou 150 mg × 2/j Après 5 à 7 jours d’héparine |
Dose de charge de 15 mg × 2 pendant 21 jours, puis 20 mg × 1/j Sans héparine préalable obligatoire |
Dose de charge de 10 mg × 2 pendant 7 jours, puis 5 mg × 2/j Sans héparine préalable obligatoire |
| Posologie en post-SCA | Pas d’indication | 2,5 mg × 2/j | Pas d’indication |
EP : embolie pulmonaire ; FA : fibrillation atriale ; SCA : syndrome coronarien aigu ; TVP : thrombose veineuse profonde.
1Rétrécissement mitral ou valve mécanique.
V Thrombolytiques
A Médicaments et mode d’action
Les thrombolytiques sont des médicaments qui ont pour objectif de lyser les caillots déjà constitués. Ce sont des activateurs de la fibrinolyse physiologique et en particulier du plasminogène.
La streptokinase et l’urokinase sont les premiers thrombolytiques qui ont été commercialisés. La streptokinase n’est plus commercialisée. L’urokinase comporte un risque allergique.
L’altéplase (Actilyse®) et la ténectéplase (Métalyse®) sont des thrombolytiques de nouvelle génération. La demi-vie de la ténectéplase est relativement longue, permettant une administration simplifiée en un seul bolus intraveineux.
B Indications
Ces médicaments sont administrés par voie intraveineuse dans des conditions très précises :
• l’infarctus du myocarde datant de moins de 6 à 12 heures lorsqu’il n’y a pas de possibilité d’angioplastie (essentiellement en France par les SAMU en préhospitalier) ;
• l’accident vasculaire cérébral vu dans les 4 h 30 après exclusion d’une cause hémorragique ;
• l’embolie pulmonaire grave.
C Surveillance
Leur efficacité s’accompagne d’un risque hémorragique important qui doit faire « peser » leur indication. Le risque d’hémorragie intracérébrale est de l’ordre de 0,7 à 2 %.
Lors d’un traitement thrombolytique, les tests classiques de la coagulation (TCA/TP) sont perturbés pendant toute la durée de l’effet du médicament (environ 24 heures).
La surveillance des saignements cliniques et infracliniques est de rigueur (point de ponction artérielle/voie veineuse/sonde urinaire, etc.).
Un groupage sanguin systématique est justifié afin d’éviter une perte de temps en cas de saignement grave.
D Contre-indications
Elles sont particulièrement importantes à respecter. Elles correspondent logiquement à toute circonstance qui pourrait accentuer le risque de saignement : certaines de ces situations peuvent être « contournées » lorsque le risque vital est en jeu (EP massive). Les contre-indications sont les suivantes :
• allergie connue au produit ;
• patients ayant un risque hémorragique accru : trouble de la coagulation congénitale ou acquis, thrombopathie sévère, thrombopénie sévère, etc. ;
• poussée ulcéreuse (< 6 mois) ;
• intervention de chirurgie générale (< 10 jours) ;
• intervention de chirurgie vasculaire (< 1 mois) ; • traumatisme grave ou ponction récente de gros vaisseaux non compressibles ; • réanimation cardiopulmonaire prolongée ; • anévrisme ou malformation artérielle ou veineuse, malformation vasculaire cérébrale ; • HTA non contrôlée (> 200 mmHg) ;
• AVC étendu (< 6 mois) ;
• traitement associé par AVK ;
• insuffisance hépatique sévère ;
• péricardite aiguë ;
• endocardite aiguë ou subaiguë ;
• grossesse.
VI Accidents des anticoagulants
A Accidents liés à l’administration d’héparines
1 Accidents hémorragiques liés à l’héparine
Fréquence
La fréquence des accidents hémorragiques au cours d’un traitement par héparine varie de 1 à 4 % lors d’un traitement curatif et de 1 à 2 % lors d’un traitement préventif.
Les facteurs associés à la survenue d’un accident hémorragique sont l’âge, le sexe féminin, un faible poids corporel, l’intensité et la durée de l’anticoagulation.
Les comorbidités suivantes sont également susceptibles de favoriser la survenue d’un accident hémorragique :
• pathologie digestive ou cérébrale à risque hémorragique ;
• insuffisance hépatocellulaire ;
• traumatisme ou chirurgie récente ;
• thrombopénie ;
• troubles congénitaux de la coagulation à risque hémorragique ;
• insuffisance rénale surtout pour les HBPM.
L’administration associée d’un autre antithrombotique (AVK, antiagrégants plaquettaires) mais aussi d’un AINS augmente le risque.
Tableau clinique
Il peut s’agir :
• d’un surdosage biologique asymptomatique : TCA > 3 fois le témoin ou héparinémie élevée pour les HNF, la conduite à tenir consiste à adapter les doses (cf. supra) ;
• d’une anémie typiquement microcytaire ferriprive sans hémorragie apparente (d’où la nécessité de pratiquer une NFS régulière lors des traitements de longue durée) ;
• d’un hématome ou une hémorragie extériorisée grave ou non.
Traitement préventif
Le respect des règles de prescription des héparines est l’élément fondamental de la prévention des accidents hémorragiques liés aux héparines :
• bien peser l’indication ;
• adapter les doses en fonction du poids pour les HBPM ;
• surveiller quotidiennement la biologie (TCA) en cas de traitement par HNF ;
• respecter la contre-indication des HBPM en cas d’insuffisance rénale sévère ;
• prescrire prudemment les HBPM chez les sujets âgés du fait de leur fonction rénale souvent altérée.
Conduite à tenir en cas d’accident
Elle consiste à :
• évaluer la gravité : examen clinique, mesure de la PA et de la FC, recherche de signes de choc hémorragique, dosage de l’hémoglobine et de l’hématocrite ;
• en cas d’accident mineur : adapter les posologies et assurer une surveillance clinique et biologique rapprochée ;
• en cas d’accident majeur :
– mettre en balance le risque hémorragique et celui induit par l’arrêt du traitement anticoagulant (chez les porteurs de valve mécanique, par exemple),
– procéder à un remplissage intraveineux par des macromolécules, puis compenser les pertes sanguines par transfusion de concentrés de culots globulaires si nécessaire,
– évaluer l’intérêt de l’administration de l’antidote de l’héparine : le sulfate de protamine.
2 Thrombopénies induites par les héparines
Définition et généralités
On distingue deux types de thrombopénies survenant chez des patients traités par HNF ou HBPM :
• la thrombopénie de type I (thrombopénie précoce), bénigne, d’origine non immune et d’apparition précoce sans complication thrombotique et régressant malgré la poursuite du traitement par l’héparine ;
• la thrombopénie de type II, potentiellement grave, d’origine immune et en règle générale d’apparition plus tardive vers J7-J10, qui est la thrombopénie immunoallergique à l’héparine (TIH).
La TIH est induite par des anticorps qui reconnaissent dans la plupart des cas le facteur 4 plaquettaire (PF4) modifié par l’héparine. En découle une activation plaquettaire intense ainsi qu’une activation de la coagulation pouvant aboutir paradoxalement à des thromboses veineuses et/ou artérielles.
Le risque de la TIH est donc thrombotique et non hémorragique (sauf en cas de CIVD [coagulation intravasculaire disséminée] associée).
Épidémiologie
• ![]() La véritable incidence de la TIH est méconnue : de l’ordre de 0,05 à 3 % pour les plus pessimistes, beaucoup plus fréquente avec l’HNF qu’avec les HBPM. Sa gravité mérite néanmoins qu’elle soit bien connue.
La véritable incidence de la TIH est méconnue : de l’ordre de 0,05 à 3 % pour les plus pessimistes, beaucoup plus fréquente avec l’HNF qu’avec les HBPM. Sa gravité mérite néanmoins qu’elle soit bien connue.
• La fréquence est plus élevée en milieu chirurgical qu’en milieu médical, et haute en chirurgie cardiaque et orthopédique.
• ![]() Le délai de survenue de la TIH est typiquement de 5 à 8 jours, après le début de l’héparinothérapie. Attention : ce délai peut être plus court (dès le 1er jour du traitement) chez des patients ayant été exposés à l’héparine dans les 3 mois précédents. Il peut aussi être plus long, notamment avec les HBPM (pouvant atteindre plus de 3 semaines).
Le délai de survenue de la TIH est typiquement de 5 à 8 jours, après le début de l’héparinothérapie. Attention : ce délai peut être plus court (dès le 1er jour du traitement) chez des patients ayant été exposés à l’héparine dans les 3 mois précédents. Il peut aussi être plus long, notamment avec les HBPM (pouvant atteindre plus de 3 semaines).
Selon l’HAS, le diagnostic de TIH doit être évoqué devant les signes suivants :
• numération plaquettaire < 100 000/mm3 (100 G/L) et/ou chute relative des plaquettes sur deux numérations successives (de 30 à 50 % selon les recommandations) sous traitement par héparine, d’où l’impérative nécessité d’une numération plaquettaire avant ou dans les 24 heures de l’introduction d’un traitement par héparine ;
• apparition de thromboses ou extension du processus thrombotique initial sous héparine ;
• résistance biologique à l’HNF (le TCA ne décroche pas pour des doses importantes) ;
• placards inflammatoires au site d’injection des héparines SC ;
• rarement insuffisance surrénalienne aiguë sur une nécrose des surrénales.
![]() Dans la TIH, chez 80 % des patients la thrombopénie est comprise entre 30 et 70 G/L.
Dans la TIH, chez 80 % des patients la thrombopénie est comprise entre 30 et 70 G/L.
Une coagulopathie de consommation (CIVD) est rapportée dans 10 à 20 % des cas.
Lorsque la TIH se complique de thrombose :
• les thromboses veineuses profondes sont plus fréquentes (80 %) que les artérielles ;
• les thromboses artérielles peuvent toucher l’aorte abdominale et ses branches avec alors un aspect de thrombus blanc (riche en plaquettes) très caractéristique ;
• des complications neurologiques surviennent chez 9,5 % des patients (AVC ischémiques, thromboses veineuses cérébrales, etc.).
La crainte de la survenue d’une TIH est à l’origine de la surveillance de la numération plaquettaire (avant traitement ou au plus tard 24 heures après le début du traitement, puis 2 fois/semaine à partir du 5e jour).
Cette surveillance n’ayant pas fait la preuve de son efficacité est actuellement remise en question au moins avec les HBPM (incidence de TIH beaucoup plus faible).
Les dernières recommandations de l’HAS/Afssaps n’imposent plus la surveillance plaquettaire lorsque l’HBPM est donnée en contexte médical mais la préconisent encore en milieu chirurgical ou traumatique et chez les patients à risque (antécédent d’exposition à l’HNF ou HBPM dans les 6 mois précédents ou comorbidités importantes).
Conduite à tenir devant une suspicion de TIH
• ![]() Confirmer la thrombopénie par prélèvement sur tube citraté et/ou prélèvement capillaire et contrôle sur lame (éliminer une thrombo-agglutination).
Confirmer la thrombopénie par prélèvement sur tube citraté et/ou prélèvement capillaire et contrôle sur lame (éliminer une thrombo-agglutination).
• ![]() Utilise le score T4 qui permet d’estimer la probabilité d’une TIH (cf. tableau 22.13).
Utilise le score T4 qui permet d’estimer la probabilité d’une TIH (cf. tableau 22.13).
• ![]() Éliminer une autre cause de thrombopénie (infectieuse, médicamenteuse, CEC [circulation extracorporelle]).
Éliminer une autre cause de thrombopénie (infectieuse, médicamenteuse, CEC [circulation extracorporelle]).
• Pratiquer un test immunoenzymatique (Elisa) à la recherche d’anticorps anti-PF4 (dont la valeur prédictive négative est meilleure que la valeur prédictive positive) ou tests fonctionnels d’activation plaquettaire avec des plaquettes de volontaires sains.
• Demander un avis spécialisé afin d’éviter d’arrêter une héparine sans argument.
| La décision d’arrêter l’héparine et de la remplacer par un autre antithrombotique d’action immédiate doit être prise dès qu’il y a suspicion forte de la TIH et ne peut attendre les résultats de la biologie. |
![]() La conduite à tenir est la suivante :
La conduite à tenir est la suivante :
• hospitalisation : rechercher une complication thrombotique infraclinique ;
• en cas de survenue d’une TIH :
– déclaration obligatoire au centre régional de pharmacovigilance,
– délivrance d’une « carte de TIH » au patient qui notifie cet antécédent ;
• arrêt de toute source d’héparine (attention aux flushs héparinés des cathéters artériels) ;
• si le patient ne présente pas d’indication de traitement anticoagulant à doses dites curatives :
– traitement par danaparoïde sodique (Orgaran®) systématique au moins à dose prophylactique et au minimum jusqu’à correction de la numération plaquettaire,
– relais possible par :
– AVK (début à petite dose) envisagé en cas de prévention prolongée,
– le fondaparinux (Arixtra®) mais aussi les AOD,
– numération plaquettaire au moins 1 fois/j jusqu’à normalisation de la numération plaquettaire,
| La cinétique de la numération des plaquettes (dont la normalisation doit intervenir en quelques jours) après arrêt de l’héparine est le meilleur argument pour confirmer la TIH. |
• si le patient présente une thrombose artérielle ou veineuse :
– traitement par danaparoïde sodique à doses curatives,
– idem pour le reste.
| Points | 0 | 1 | 2 |
|---|---|---|---|
| Thrombopénie | ↓ < 30 % ou plaquettes < 10 G/L |
↓ 30–50 % ou plaquettes 10–20 G/L |
↓ > 50 % ou plaquettes 20–100 G/L |
| Timing | Autre que 1 et 2 | ↓ après plus de 10 jours d’héparine ou dans les 24 heures si héparinothérapie dans les 30 à 100 jours auparavant | ↓ 5–10 jours d’héparine ou dans les 24 heures si héparinothérapie dans les 30 jours auparavant |
| Thrombose | Pas de thrombose | Extension d’une thrombose existante ou suspicion de thrombose non confirmée ou érythème cutané après injection d’héparine | Nouvelle thrombose ou réaction systémique à l’injection d’héparine ou nécrose cutanée |
| Autres causes | Certaines | Possibles | Aucune possible |
0–3 : risque faible ; 4–5 : risque intermédiaire (≥ 4 : doit faire poursuivre les investigations) ; 6–8 : risque élevé.© Lo GK, Juhl D, Warkentin TE, Sigouin CS, Eichler P, Greinacher A. Evaluation of pretest clinical score (4 T’s) for the diagnosis of heparin-induced thrombocytopenia in two clinical settings. J Thromb Haemost. 2006 ; 4 (4) : 759–65.
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
Prévention
![]() La prévention primaire des TIH repose sur trois principes :
La prévention primaire des TIH repose sur trois principes :
• durée d’utilisation des héparines la plus courte possible ;
• relais précoce par AOD ou AVK lorsque possible ;
• utilisation préférentielle des HBPM ou du fondaparinux dans les indications démontrées.
B Accidents hémorragiques liés aux antivitamines K
1 Fréquence
• ![]() Six cent mille patients environ sont traités par AVK en France, soit 1 % de la population.
Six cent mille patients environ sont traités par AVK en France, soit 1 % de la population.
• Les AVK sont la 1re cause iatrogène d’hospitalisation avec 13 % des hospitalisations pour effets indésirables médicamenteux.
![]() Il faut distinguer les surdosages constatés par la surveillance biologique (sans saignement) et ceux qui se démasquent par un saignement.
Il faut distinguer les surdosages constatés par la surveillance biologique (sans saignement) et ceux qui se démasquent par un saignement.
2 Conduite à tenir en cas de surdosage asymptomatique
• Le plus souvent, la prise en charge est ambulatoire.
• Elle est fonction de l’INR mesuré et de l’INR cible (cf. tableau 22.14).
• La cause du surdosage doit être recherchée et prise en compte dans l’adaptation éventuelle de la posologie.
• Un contrôle de l’INR doit être réalisé le lendemain.
• En cas de persistance d’un INR au-dessus de la fourchette thérapeutique, les recommandations précédentes restent valables et doivent être reconduites.
• La surveillance ultérieure de l’INR doit se calquer sur celle habituellement réalisée lors de l’instauration du traitement.
Tableau 22.14 Conduite à tenir en cas de surdosage en AVK chez un patient asymptomatique.
| INR mesuré | INR cible | |
|---|---|---|
| INR cible 2,5 (fenêtre entre 2 et 3) |
INR cible 3 (fenêtre 2,5–3,5 ou 3–4,5) |
|
| INR < 4 | Pas de saut de prise Pas d’apport de vitamine K Adaptation de la posologie |
|
| 4 < INR < 6 | Saut d’une prise Pas d’apport de vitamine K Adaptation de la posologie lors de la reprise du traitement |
Pas de saut de prise Pas d’apport de vitamine K Adaptation de la posologie |
| 6 < INR < 10 | Arrêt du traitement par AVK 1 à 2 mg de vitamine K per os Adaptation de la posologie lors de la reprise du traitement |
Saut d’une prise Avis spécialisé (ex : cardiologue si le patient est porteur d’une prothèse valvulaire mécanique) recommandé pour discuter un traitement éventuel par 1 à 2 mg de vitamine K per os Adaptation de la posologie lors de la reprise du traitement |
| INR > 10 | Arrêt du traitement par AVK 5 mg de vitamine K per os (½ ampoule buvable forme adulte) Adaptation de la posologie lors de la reprise du traitement |
Avis spécialisé sans délai ou hospitalisation recommandé |
HAS. Prise en charge des surdosages en antivitamines K, des situations à risque hémorragique et des accidents hémorragiques chez les patients traités par antivitamines K en ville et en milieu hospitalier. Synthèse des recommandations professionnelles, avril 2008. Nous remercions la Haute Autorité de santé de nous avoir autorisés à reproduire ce tableau. Il est également consultable sur le site www.has-sante.fr rubrique Toutes nos publications.
3 Conduite à tenir en cas d’hémorragies spontanées ou traumatiques
| Définition d’une hémorragie grave • Hémorragie extériorisée non contrôlable par les moyens usuels. • Instabilité hémodynamique (collapsus). • Nécessité d’un geste hémostatique (ou chirurgical). • Nécessité de transfusion de culots globulaires. • Hémorragie de localisation menaçant le pronostic vital ou fonctionnel. |
S’il n’existe aucun de ces critères, l’hémorragie est considérée comme non grave.
Le principe de la gestion initiale d’une hémorragie est le même et fait appel à des moyens qui dépendent de la localisation et de l’importance du saignement :
• compression mécanique : suture d’une plaie vasculaire ;
• application locale d’agent hémostatique (colle à la fibrine ou à la thrombine) ;
• injection locale de vasoconstricteurs (adrénaline), en particulier lors des fibroscopies digestives pour hémorragie digestive ;
• embolisation par radiologie interventionnelle.
Conduite à tenir en cas d’hémorragie non grave
• Une prise en charge ambulatoire est le plus souvent réalisable en cas d’hémorragie rapidement contrôlable.
• La mesure de l’INR est réalisée en urgence.
• En cas de surdosage, les mêmes mesures de correction de l’INR que celles décrites précédemment sont recommandées (cf. tableau 22.13).
• La cause du saignement doit être recherchée.
Conduite à tenir en cas d’hémorragie grave
• ![]() La prise en charge est hospitalière. Les AVK sont arrêtés.
La prise en charge est hospitalière. Les AVK sont arrêtés.
• La mesure de l’INR est réalisée en urgence. Le traitement est instauré sans attendre le résultat.
• On utilise des antidotes :
– la vitamine K qui nécessite quelques heures de délai d’action ;
– les concentrés de complexes prothrombiniques (CCP, aussi appelés PPSB : Kanokad®, Confidex®, Octaplex®), de délai d’action très bref mais de durée d’action courte, nécessitant donc concomitamment de la vitamine K.
• On assure le traitement habituel d’une hémorragie massive (correction de l’hypovolémie, transfusion de culots globulaires, etc.). La nécessité d’un geste hémostatique chirurgical ou endoscopique doit être rapidement évaluée.
• La surveillance biologique est la suivante :
– réalisation d’un INR 30 minutes après administration du CCP ;
– si l’INR reste > 1,5, une administration complémentaire de CCP adaptée à la valeur de l’INR est recommandée ;
– mesure de l’INR 6 à 8 heures plus tard, puis 1 fois/j pendant la période critique.
• L’indication ultérieure des AVK doit être à nouveau pesée. En cas de nécessité de traitement anticoagulant impératif, un relais par héparine est entrepris en attendant.
4 Conduite à tenir chez le polytraumatisé
• ![]() La mesure de l’INR est réalisée en urgence.
La mesure de l’INR est réalisée en urgence.
• La même conduite est recommandée que celle à tenir devant les hémorragies graves ou non graves selon la gravité et la nature du traumatisme.
• En cas de traumatisme crânien : une hospitalisation au moins 24 heures et la réalisation d’un scanner cérébral en urgence sont requises.
5 Intérêt de la prévention de ces accidents
Il fait appel à :
• l’éducation des patients ;
• l’attention portée aux interactions médicamenteuses ;
• l’utilisation de l’automesure de l’INR (dispositif semblable à ceux utilisés pour la mesure de la glycémie capillaire dans le diabète mais non remboursé en France, sauf chez l’enfant et chez les patients porteurs de prothèse valvulaire), qui peut diminuer le risque hémorragique.
C Accidents liés aux anticoagulants oraux directs
Les principes qui les gèrent sont les suivants :
• les AOD ont une demi-vie courte : le meilleur antidote est le temps que l’on peut gagner après la dernière prise ;
• le dabigatran a déjà un antidote commercialisé disponible dans certains hôpitaux ;
• les anti-X sont à ce jour antagonisés par des concentrés de PPSB ou de Feiba® (mélange de PPSB et de facteur VIII) mais l’arrivée prochaine probable d’un antidote anti-X pourra modifier ces stratégies ;
• le dosage du médicament peut être fait pour tous les AOD commercialisés (dans des laboratoires spécialisés) ;
• si ce dosage permet, en situation à risque de saignement, de gérer au mieux la situation, en cas de saignement actif, la conduite à tenir ne peut attendre le résultat du dosage de la concentration du médicament dans le sang.
Le GIHP (Groupe d’intérêt en hémostase périopératoire) a proposé des règles de conduite générales, de bon sens (cf. encadré 22.1).
Encadré 22.1 Conduite à tenir lors d’un accident hémorragique lié aux AOD proposée par le GIHP (Groupe d’intérêt en hémostase périopératoire)
• Noter : âge, poids, nom du médicament, dose, nombre de prises par jour, heure de la dernière prise, indication
• Prélever :
– créatinine (clairance d’après Cockroft)
– dosage spécifique du médicament
• Contacter le laboratoire d’hémostase
• Interrompre le traitement
© GIHP (Groupe d’intérêt en hémostase périopératoire)
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
Points-clés
| Antiagrégants • L’aspirine, le clopidogrel, le prasugrel et le ticagrélor sont les principaux antiagrégants plaquettaires actuellement disponibles. • On ne surveille pas en routine l’activité antiagrégante de ces différents traitements. • Après un SCA et/ou la mise en place d’un stent, on prescrit une double antiagrégation plaquettaire associant toujours de l’aspirine pour l’un d’entre eux, classiquement pendant 12 mois. • Après un SCA et/ou mise en place d’un stent, il faut retarder d’au moins 1 à 3 mois la réalisation d’un geste invasif hémorragique, pour ne pas interrompre trop précocement les antiplaquettaires qui exposent les patients à une thrombose de stent et à un infarctus du myocarde. • Pour de nombreux actes à risque hémorragique modéré (fibroscopie avec biopsie, stomatologie, etc.), il ne faut pas interrompre l’aspirine chez le patient en prévention secondaire. • Si le risque hémorragique est important, l’arrêt de l’aspirine doit être le plus bref possible (5 jours). Héparines • Les héparines (HNF, HBPM, fondaparinux) sont utilisées lorsque l’on souhaite obtenir un effet anticoagulant rapide. Les HBPM et le fondaprinux sont contre-indiqués en cas d’insuffisance rénale sévère. • L’efficacité thérapeutique de l’HNF se mesure par le TCA (2 à 3 fois le témoin) ou par l’activité anti-Xa (entre 0,5 et 0,8). Sauf situation particulière, il n’est pas nécessaire de mesurer l’efficacité thérapeutique des HBPM. Antivitamines K • Les AVK s’utilisent par voie orale pour un traitement anticoagulant prolongé. Leur efficacité thérapeutique se mesure par l’INR, dont la cible est différente en fonction des indications. Ils ne sont pas efficaces immédiatement et donc, lorsqu’ils sont utilisés en relais des héparines, les deux traitements doivent se chevaucher quelques jours jusqu’à l’obtention d’un INR efficace. L’éducation thérapeutique est cruciale pour le patient sous AVK. • Si un geste à risque hémorragique doit être envisagé, on peut souvent le faire sans arrêter les AVK si le risque hémorragique est faible ou en arrêtant le traitement temporairement si le risque hémorragique est plus important et si le risque de thrombose ne l’est pas trop. • Les relais par héparines sont sources de complication hémorragique ou thrombotique et sont réservés aux situations à risque thrombotique élevé (EP récente, prothèse valvulaire mécanique, FA à risque embolique élevé). AOD • Ils sont efficaces très rapidement (2 heures après la prise) et ne nécessitent pas de surveillance biologique. • On adapte leur posologie en fonction de l’âge, de la fonction rénale et du poids. Ils sont contre-indiqués en cas d’insuffisance rénale sévère. • Leurs indications actuelles sont réservées au traitement curatif de la MTEV (anti-Xa), au traitement préventif de la FA et pour certains d’entre eux (anti-Xa) à la prévention et au traitement de la MTEV. • Ils ne peuvent être prescrits chez les patients porteurs de prothèses mécaniques ou en cas de RM. Fibrinolytiques • Ils sont utilisés aujourd’hui dans l’infarctus du myocarde, l’AVC et l’EP grave. • Leur efficacité s’accompagne d’un risque d’hémorragie significatif, notamment cérébrale. Accidents des anticoagulants • Les anticoagulants sont responsables d’une iatrogénie importante. • Il peut s’agir d’accidents hémorragiques parfois liés à un surdosage. • Le sulfate de protamine est un antidote de l’héparine, la vitamine K est l’antidote des AVK et un AOD (le dabigatran) a aussi déjà un antidote, les autres peuvent être antagonisés par du PPSB ou du Feiba®. • Il est important de dépister rapidement des accidents et de bien connaître leur prise en charge qui dépend de la gravité du tableau hémorragique et du risque thrombotique sous-jacent. • Il faut aussi savoir dépister et prendre en charge une thrombopénie induite par l’héparine. |
Notions indispensables et inacceptables
Notions indispensables
• Ne pas oublier l’éducation du patient sous AVK et sous AOD.
• Pas d’AOD dans les prothèses valvulaires mécaniques ou dans le RM.
• Savoir faire un relais héparine –AVK.
Notions inacceptables
• Prescrire une HBPM ou un AOD en cas d’insuffisance rénale sévère.
• Prescrire un AOD dans les prothèses valvulaires mécaniques ou dans le rétrécissement mitral.
Partagez cette publication
Written by : SFC
Plus de publications de la SFC

CARDIOLOGIE PÉDIATRIQUE Perinatal Exercise and Cardiovascular Disease Risk | Lire l'article JACC CARDIO-ONCOLOGIE Blood [...]

Archives of Cardiovascular Diseases | Article du mois - Mai 2025 Patrick Henry, Sophie [...]


